Наслідки переходу на монотерапію тикагрелором невдовзі після коронарного стентування порівняно з продовженням ПАТ: систематичний огляд і метааналіз результатів рандомізованих дослідженьРічна подвійна антитромбоцитарна терапія (ПАТ) комбінацією інгібітора P2Y12-рецептора тромбоцитів (іP2Y12) і ацетилсаліцилової кислоти (АСК) на цей час є рекомендованою стандартною схемою антитромбоцитарної терапії (АТТ), яку призначають пацієнтам після імплантації коронарних стентів із лікарським покриттям (СЛП), особливо після гострого коронарного синдрому (ГКС) [1, 2]. Проте результати низки досліджень показали, що альтернативна стратегія з раннього (від кількох тижнів до кількох місяців після початку ПАТ) скасування АСК із переходом на монотерапію іP2Y12 дає змогу знизити ризик кровотеч без збільшення ішемічного ризику порівняно з продовженням стандартної ПАТ [3–11]. Утім, результати цих окремих досліджень складно інтерпретувати, оскільки вони різняться за дизайном, досліджуваними популяціями й типом іP2Y12, а деякі також не мають достатньої статистичної потужності для точної оцінки ефекту лікування на важливі окремі кінцеві точки, як-от смертність або ризик тромбозу стента, або для проведення аналізів у підгрупах. Метааналізи, проведені з метою подолання зазначених обмежень, також є недостатньо інформативними через відсутність аналізу індивідуальних даних пацієнтів (ІДП) або через включення в аналіз не всіх доступних досліджень [12–16]. Із метою розширення знань про результати застосування стратегії деескалації АТТ Valgimigli et al. розглянули й проаналізували всі доступні докази з рандомізованих контрольованих досліджень (РКД) щодо деескалації ПАТ до монотерапії іP2Y12 і провели метааналіз ІДП, отриманих у пацієнтів із ГКС або без нього після імплантації коронарного СЛП [17]. З огляду на мізерність і неповноту даних щодо переходу на монотерапію прасугрелем і клопідогрелем, а також на нещодавнє завершення нових досліджень монотерапії тикагрелором, до метааналізу ввійшли тільки РКД, які вивчали монотерапію тикагрелором. Основна інформація про цей метааналіз стисло подана в статті.

Методологія метааналізу Valgimigli et al. Метою представленого систематичного огляду й метааналізу ІДП РКД була оцінка ефективності та безпеки переходу на монотерапію тикагрелором (90 мг 2 рази на день) після короткострокової (від 2 тижнів до 3 місяців) ПАТ порівняно зі стандартною 12-місячною ПАТ у пацієнтів, які перенесли черезшкірне коронарне втручання (ЧКВ) з імплантацією СЛП. Окрім досліджень, у яких як іP2Y12 використовували тільки тикагрелор, до аналізу ввійшли РКД, що порівнювали стандартну ПАТ із монотерапією різними іP2Y12, у яких рандомізацію стратифікували за типом іP2Y12, і з цих досліджень вилучали лише дані пацієнтів, рандомізованих для отримання тикагрелору або стандартної ПАТ. Дослідження, що допускали участь пацієнтів із показаннями до довгострокового приймання пероральних антикоагулянтів, в аналіз не включали. Інші додаткові обмеження при відборі РКД не застосовували. Пошук досліджень проводили в базах даних Ovid MEDLINE, Embase, Сardiovascular Research Foundation's Transcatheter Cardiovascular Therapeutics Platform і платформах Європейського товариства кардіологів станом на 20 травня 2024 року [17]. Трьома ранжованими первинними кінцевими точками метааналізу були тяжкі несприятливі серцево-судинні (СС) або цереброваскулярні події (major adverse cardiovascular or cerebrovascular events, MACCE – комбінація інфаркту міокарда [ІМ], інсульту й смерті від СС причин), кровотеча 3 або 5 типу за класифікацією Академічного консорціуму з вивчення кровотеч (Bleeding Academic Research Consortium, BARC) і загальна смертність. У кожному включеному дослідженні незалежний комітет із клінічних подій централізовано оцінював несмертельні компоненти кінцевих точок і випадки СС смерті. Valgimigli et al. спочатку перевірили гіпотезу про не меншу ефективність схеми деескалації (переходу на монотерапію тикагрелором після короткотермінової ПАТ) порівняно з продовженням ПАТ за впливом на MACCE у вибірці, що виконала вимоги протоколу (per-protocol population, РР вибірка: виключала пацієнтів, які не відповідали критеріям відбору в дослідження або не отримували призначену терапію), а потім ієрархічно перевірили гіпотезу про перевагу переходу на монотерапію тикагрелором перед продовженням ПАТ за впливом на ризик кровотеч 3 й 5 типу за BARC і за впливом на загальну смертність у вибірці рандомізованих пацієнтів (intention-totreat population, вибірка ITT). Автори прицільно вивчали події, що розвинулися з моменту переходу на монотерапію тикагрелором в експериментальній групі або продовження ПАТ у контрольній групі і до кінця періоду спостереження. Тому для чотирьох РКД, у яких усі учасники після рандомізації проходили загальну початкову ПАТ [3–5, 7], дані, зібрані впродовж цього початкового періоду, виключали з метааналізу. Ефекти лікування оцінювали у вигляді відношень ризиків (ВР) і 95% довірчих інтервалів (ДІ). Для оцінки гетерогенності даних про ефект лікування з різних досліджень використовували критерій τ2. Збір даних для аналізу тривав до найвіддаленішого контрольного моменту, у який учасники з експериментальної групи отримували монотерапію тикагрелором, а учасники в контрольній групі отримували ПАТ. Усі результати подано у вигляді оцінок Каплана-Майєра. Згідно з планом ієрархічного тестування, друга (кровотечі 3 і 5 типу за BARC) і третя (загальна смертність) первинні кінцеві точки мали б аналізуватися тільки в тому разі, якщо на першому етапі тестування було б доведено не меншу ефективність монотерапії тикагрелором порівняно з ПАТ щодо впливу на ризик MACCE. Після аналізу всієї сукупності даних автори провели послідовні аналізи кожного дослідження, щоб визначити їхній внесок у результати метааналізу загалом і після розподілу учасників на когорти з урахуванням клінічної картини (ГКС або хронічний коронарний синдром [ХКС]). Також було проведено аналізи в підгрупах, виділених з урахуванням основних вихідних характеристик учасників.
Результати метааналізу Valgimigli et al. Загалом у перерахованих вище базах даних було виявлено 8361 унікальну публікацію, із яких, за результатами перевірки відповідності критеріям відбору, для метааналізу було обрано шість досліджень: GLASSY, SMARTCHOICE, TICO, TWILIGHT, T-PASS і ULTIMATE-DAPT [3–8]. Спочатку до вибірки для аналізу увійшли ІДП 24 562 учасників, із яких 155 (0,6%) були виключені через дострокове припинення участі в дослідженні або смерть до моменту початку періоду експериментального лікування. Отже, до вибірки ITT увійшли 24 407 пацієнтів, зокрема 12 199 (50,0%) пацієнтів, рандомізованих для отримання монотерапії тикагрелором, і 12 208 (50,0%) пацієнтів, рандомізованих для продовження ПАТ (АСК + тикагрелор у 10 492 [85,9%] пацієнтів або АСК + клопідогрель у 1716 [14,1%] пацієнтів). Під час формування РР вибірки з вибірки ITT було виключено ще 1151 (4,7%) учасника, який порушив вимоги протоколу, що в підсумку дало вибірку з 23 256 пацієнтів (11 505 у групі монотерапії тикагрелором і 11 751 у групі продовження ПАТ). Медіанна тривалість ПАТ до початку монотерапії становила 78 днів (міжквартильний розмах [МКР] 31–92 дні, діапазон 12–97 днів). Медіанна тривалість лікування в групах монотерапії тикагрелором або ПАТ після рандомізації становила 334 дні (МКР 329–365) [17]. Отримані групи пацієнтів були добре збалансовані за вихідними клінічними характеристиками й демографічними даними (табл. 1). Медіанний вік становив 64 роки (МКР 56– 71), 5525 (22,6%) пацієнтів були жінками. У 3232 (13,8%) із 23 394 пацієнтів, щодо яких були зібрані відповідні дані, був високий ризик кровотечі, який визначали як оцінку за шкалою PRECISE DAPT ≥25. Аналіз процедурних характеристик показав, що у 3555 (14,6%) пацієнтів під час ангіографії був визначений коронарний тромбоз, 5820 (23,8%) пацієнтів перенесли складне ЧКВ, медіана довжини встановленого стента становила 30 мм, і в 5270 (30,5%) пацієнтів проводили установлення стентів унапустку. [17].
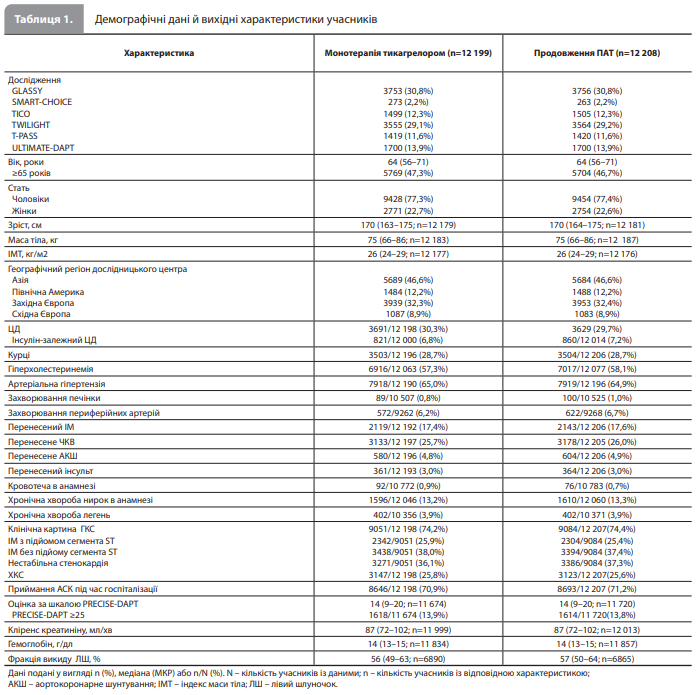
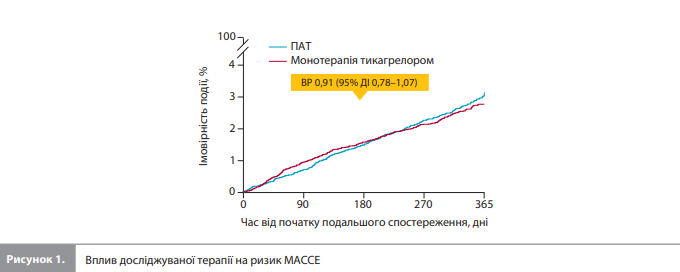
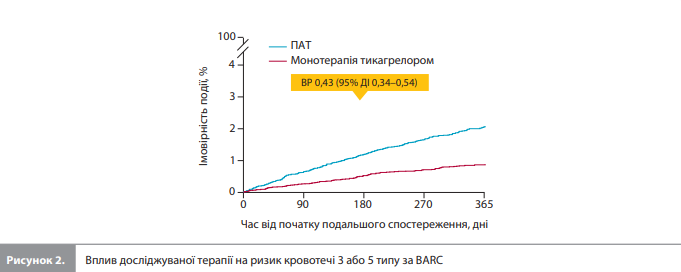
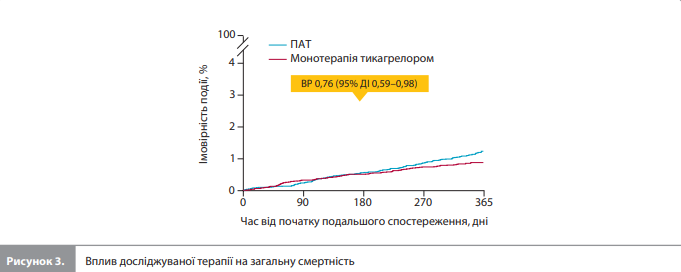
Первинну комбіновану кінцеву точку MACCE (ІМ, інсульт або смерть від будь-якої причини) було зареєстровано у 297 (оцінка Каплана-Майєра 2,8%) із 11 505 пацієнтів у групі монотерапії тикагрелором і в 332 (оцінка Каплана-Майєра 3,2%) із 11 751 пацієнта в групі продовження ПАТ (РР вибірка: ВР 0,91, 95% ДІ 0,78–1,07, рдля не меншої ефективності=0,0039; τ2<0,0001; рис. 1, табл. 2) [17]. Кровотечі 3 або 5 типу за класифікацією BARC були зареєстровані в 102 пацієнтів (оцінка Каплана-Майєра 0,9%) у групі монотерапії тикагрелором і у 237 пацієнтів (оцінка Каплана-Майєра 2,1%) у групі продовження ПАТ (вибірка ITT: ВР 0,43, 95% ДІ 0,34–0,54; pдля переваги<0,0001; τ2=0,079; рис. 2, табл. 2) [17]. Загалом померли 102 (оцінка Каплана-Майєра 0,9%) пацієнти в групі монотерапії тикагрелором і 135 (оцінка Каплана-Майєра 1,2%) пацієнтів у групі продовження ПАТ (вибірка ITT: ВР 0,76, 95% ДІ 0,59–0,98, рдля переваги=0,034; τ2<0,0001; рис. 3, табл. 2) [17].
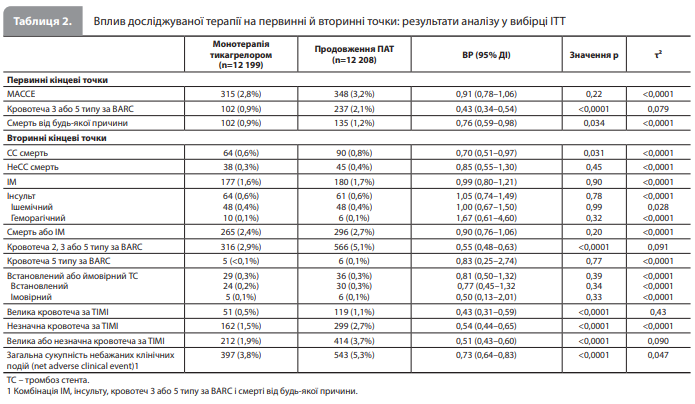
Послідовні аналізи включених досліджень підтвердили не меншу ефективність монотерапії тикагрелором порівняно з продовженням ПАТ для кінцевої точки MACCE і перевагу монотерапії за впливом на ризик кровотеч 3 або 5 типу за BARC; докази переваги монотерапії тикагрелором над ПАТ у зниженні загальної смертності, отримані в цьому аналізі, були розцінені як непереконливі [17]. Аналізи в підгрупах показали, що для всіх трьох аналізованих первинних кінцевих точок вік, ризик кровотечі, складність ЧКВ, час рандомізації (≤30 днів vs >30 днів) і географічний регіон не впливали на ефект лікування; водночас для МАССЕ спостерігали взаємодію між ефектом лікування та статтю (менший ризик МАССЕ під час монотерапії тикагрелором у жінок [ВР 0,67, 95% ДІ 0,49–0,93], але не в чоловіків [ВР 0,99, 95% ДІ 0,83–1,18; pдля взаємодії=0,041]) і між ефектом лікування та статусом цукрового діабету (ЦД; менший ризик МАССЕ за монотерапії тикагрелором у пацієнтів із ЦД [ВР 0,76, 95% ДІ 0,60–0,96], але не у хворих без ЦД [ВР 1,03, 95% ДІ 0,84–1,26; pдля взаємодії=0,043; рис. 4]) [17].
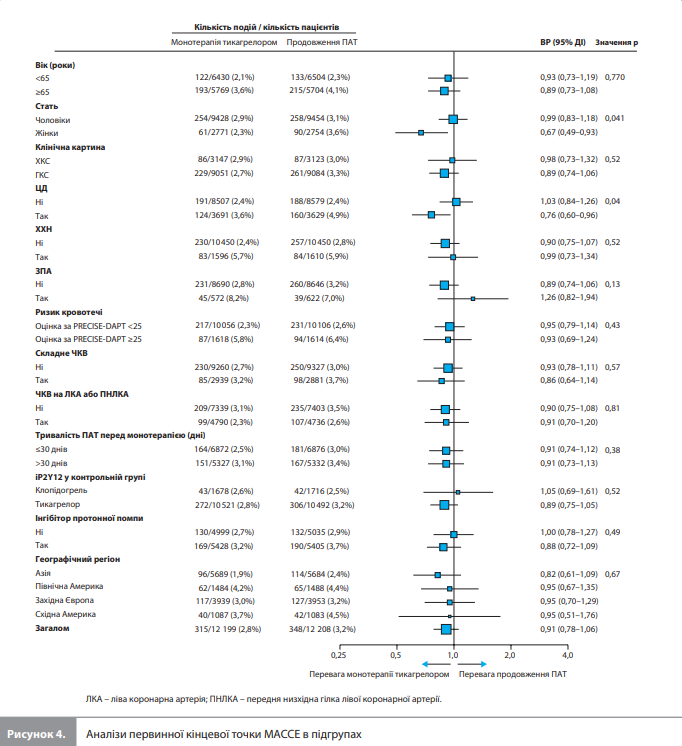
Аналіз у когортах, виділених з урахуванням клінічної картини, показав відсутність взаємодії між клінічною картиною та ефектом монотерапії тикагрелором порівняно з продовженням ПАТ для МАССЕ (ВР 0,89 [95% ДІ 0,74–1,06] у пацієнтів із ГКС і 0,98 [95% ДІ 0,73–1, 32] у пацієнтів із ХКС) і виявив таку взаємодію для кровотечі 3 або 5 типу за BARC (ВР 0,34 [95% ДІ 0,26–0,45] у пацієнтів із ГКС і 0,86 [95% ДІ 0,55–1,36] у пацієнтів із ХКС) і для смерті від будь-яких причин (ВР 0,74 [95% ДІ 0,55–0,99] для пацієнтів із ГКС і 0,82 [95% ДІ 0,50–1,35] для пацієнтів із ХКС) (табл. 3) [17]. Послідовні аналізи включених досліджень підтвердили не меншу ефективність монотерапії тикагрелором (порівняно з продовженням ПАТ) для MACCE і перевагу – для кровотечі 3 або 5 типу за BARC у хворих на ГКС, але не в пацієнтів із ХКС [17].
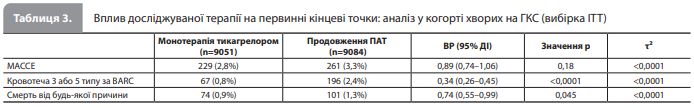
Обговорення результатів метааналізу Valgimigli et al. У цьому метааналізі ІДП оцінка сукупного набору даних із РКД, які порівнювали стратегію переходу на монотерапію тикагрелором після короткострокової ПАТ (медіана тривалості ПАТ – 78 днів, діапазон – від 2 тижнів до 3 місяців) зі стандартною 12-місячною ПАТ після ЧКВ з імплантацією СЛП, надала переконливі докази не меншої ефективності монотерапії тикагрелором порівняно з продовженням ПАТ за впливом на ризик MACCE у загальній досліджуваній вибірці та в когорті хворих із ГКС, але не в когорті хворих із ХКС. Також монотерапія тикагрелором перевершувала стандартну ПАТ із точки зору ризику великих кровотеч у загальній досліджуваній вибірці та в когорті хворих із ГКС, але не в когорті хворих із ХКС. За даними аналізу загальної досліджуваної вибірки монотерапія тикагрелором була також пов'язана зі значним зниженням загальної смертності, хоча послідовний аналіз включених досліджень показав непереконливі результати. І, нарешті, було виявлено гетерогенність ефекту лікування на MACCE залежно від статі, що виявлялася можливою перевагою монотерапії тикагрелором перед продовженням ПАТ у жінок, але не в чоловіків [17]. Результати метааналізу Valgimigli et al. принципово відрізняються від результатів досліджень стратегії деескалації АТТ із переходом на монотерапію АСК або клопідогрелем. Зокрема, раніше було показано, що перехід на монотерапію АСК після 3–6-місячної ПАТ у пацієнтів із ГКС був пов'язаний зі зниженням ризику кровотеч і, водночас, збільшенням ризику несприятливих ішемічних подій порівняно з продовженням ПАТ [18]. За даними трьох азійських РКД перехід на монотерапію клопідогрелем після короткого курсу ПАТ викликав побоювання, пов'язані з можливим збільшенням смертності порівняно з річною ПАТ [4, 9, 10]. Що стосується прасугрелю, його застосування в рамках деескалації ПАТ після імплантації СЛП вивчали тільки в спостережних дослідженнях [19]. Метааналіз, проведений Valgimigli et al., важливий тим, що на цей момент є єдиним метааналізом ІДП, у якому проводили як аналіз усієї сукупності даних із шести РКД, так і послідовний аналіз цих досліджень з оцінкою кінцевих точок як у загальній вибірці, так і в когортах, отриманих унаслідок стратифікації даних з урахуванням клінічної картини (ГКС vs ХКС). Автори також проаналізували ефект монотерапії тикагрелором у різних підгрупах пацієнтів, зокрема серед пацієнтів із хронічною хворобою нирок і без неї, у хворих після складного ЧКВ, імплантації стента в стовбур лівої коронарної артерії (ЛКА) або проксимальний відділ передньої низхідної гілки ЛКА, а також у пацієнтів із високим ризиком кровотечі, і не виявили жодних доказів підвищеного ризику MACCE після переходу на монотерапію тикагрелором ані у загальній вибірці, ані у вибірці пацієнтів із ГКС. У такій же спосіб, пацієнти літнього віку (≥70 років) із групи монотерапії тикагрелором, у яких більш раннє дослідження виявило можливі ознаки небажаних наслідків такого переходу [20], за даними Valgimigli et al. не піддавалися вищому ризику MACCE порівняно з пацієнтами, що продовжували ПАТ. Водночас у хворих на ЦД, для яких характерний підвищений СС ризик, монотерапія тикагрелором сильніше знижувала ризик MACCE порівняно з продовженням ПАТ, ніж в учасників без ЦД. Слід зазначити, що не менша ефективність тикагрелору за впливом на ризик MACCE порівняно з продовженням ПАТ зберігалася і була послідовною, незалежно від терміну переходу з ПАТ на монотерапію тикагрелором (протягом першого місяця після ЧКВ або пізніше) [17]. Також дуже важливо, що згідно з деякими аналізами, проведеними під час метааналізу Valgimigli et al., загальна і СС смертність були нижчими за монотерапії тикагрелором, ніж за продовження ПАТ. Це неостаточний результат, але він чітко показує, що перехід на монотерапію тикагрелором не пов'язаний із надмірною кількістю смертельних подій порівняно зі стандартною річною ПАТ. Нижчий ризик смерті на тлі монотерапії тикагрелором у загальній досліджуваній вибірці був сильніше помітний серед жінок, ніж серед чоловіків, однак жінки були недостатньо представлені у всіх включених РКД. Статеві відмінності в ефектах тикагрелору на смертність, що спостерігалися, мабуть, не пояснюються нижчим ризиком великих кровотеч у жінок, оскільки і відносне, і абсолютне зниження ризику великих кровотеч у чоловіків і жінок було однаковим. Отже, необхідні подальші дослідження, щоб підтвердити виявлену перевагу монотерапії тикагрелором перед стандартною ПАТ у плані впливу на смертність і її залежність від статі, а також прояснити механізм, що лежить в основі статевих відмінностей у прояві / вираженості цього ефекту [17]. Valgimigli et al. показали значне зниження ризику великих кровотеч за монотерапії тикагрелором порівняно зі стандартною ПАТ у загальній досліджуваній вибірці та в когорті пацієнтів із ГКС, але не виявили подібної різниці в меншій за розміром когорті хворих на ХКС. Цей результат, імовірно, відображає різницю в схемах ПАТ, які застосовували в контрольній групі, а саме використання комбінації АСК + тикагрелор у пацієнтів із ГКС і комбінації АСК + клопідогрель у пацієнтів із ХКС, а також нижчу статистичну потужність аналізу через меншу кількість учасників із ХКС. Загалом накопичені дані показують, що монотерапія тикагрелором має перевагу перед стандатною ПАТ у пацієнтів із ГКС, але не обов'язково перевершить ПАТ у пацієнтів із ХКС через невизначеність щодо збереження антиішемічного ефекту й зниження ризику кровотеч [12, 17]. Навпаки, у хворих на ГКС рання деескалація АТТ із переходом на монотерапію тикагрелором асоціюється з більш ніж 60% зниженням відносного ризику великої кровотечі як серед хворих із групи високого ризику кровотечі, так і у хворих без такого ризику, тому ранній перехід на монотерапію тикагрелором потрібно розглядати в усіх пацієнтів із ГКС, а не тільки у хворих із високим геморагічним ризиком [21, 22]. При інтерпретації представленого метааналізу необхідно враховувати низку обмежень. Найбільш значущими з них автори вважають: включення в аналіз 4 відкритих досліджень, особливості лікування хворих на ХКС у контрольній групі, яка отримувала стандартну ПАТ (вищеописана можливість отримання тикагрелору або клопідогрелю на додачу до АСК, а також використання річної ПАТ попри рекомендовану в практичних настановах 6-місячну ПАТ після ХКС), той факт, що в 4 із 6 включених РКД брали участь винятково пацієнти азіатського походження (хоча до досліджуваної вибірки ввійшло 13 034 [53,4%] неазіатських і 11 373 [46,6%] азіатських пацієнти, і, до того ж, аналіз у підгрупах засвідчив відсутність залежності ефектів лікування від географічного регіону), а також низьку (порівняно з іншими дослідженнями) абсолютну частоту ішемічних або смертельних подій у включених дослідженнях. Також слід зазначити, що за відсутності поправки на множинність порівнянь, результати оцінювання вторинних кінцевих точок та аналізів у підгрупах слід вважати даними, що генерують гіпотези, а оскільки послідовний аналіз досліджень було заздалегідь визначено лише для трьох первинних кінцевих точок у загальній досліджуваній вибірці, відповідні аналізи в когортах пацієнтів із ГКС і ХКС носять апостеріорний характер. Не менш важливо, що проведений аналіз не дає змоги віддати перевагу ранній (протягом першого місяця після ЧКВ) або пізнішій (через 1–3 місяці після ЧКВ) деескалації АТТ, оскільки обидва варіанти були пов'язані з незбільшенням ризику МАССЕ і зі зниженням ризику великих кровотеч. І, нарешті, цей аналіз не дає змоги порівнювати перехід на монотерапію тикагрелором з іншими варіантами деескалації АТТ або з ПАТ комбінацією АСК + прасугрель [17].
Висновки Отже, цей метааналіз ІДП довів, що в пацієнтів із ГКС деескалація АТТ у вигляді переходу з ПАТ на монотерапію тикагрелором через нетривалий час (від кількох тижнів до кількох місяців) після імплантації коронарних СЛП не збільшує ризик смертельних і несмертельних ішемічних подій, але суттєво знижує ризик великих кровотеч порівняно зі стандартною однорічною ПАТ. Було відзначено значну перевагу тикагрелору у вигляді зниження смертності, особливо виражену серед жінок, проте цей результат потребує додаткового підтвердження. Водночас у пацієнтів із ХКС переваги та ризики, пов'язані з досліджуваною схемою деескалації АТТ порівняно з продовженням ПАТ, залишаються невстановленими.
Список літератури знаходиться в редакції
Автор огляду Олена Грибова Medicine Review 2024; 8 (81): 17 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2025. Усі права захищені.
|
мапа сайту корисні посилання |