Оцінка впливу перенесеного інфаркту міокарда на ефекти дапагліфлозину в пацієнтів із серцевою недостатністю і різними значеннями ФВ ЛШ: новий об'єднаний аналіз досліджень DAPA-HF і DELIVERІшемічна хвороба серця (ІХС) широко поширена серед пацієнтів із серцевою недостатністю (СН) і має винятково несприятливий вплив на прогноз, збільшуючи тяжкість проявів і прискорюючи прогресування СН [1, 2]. Серед проявів ІХС зв'язок із СН найочевидніший для інфаркту міокарда (ІМ), оскільки до його наслідків крім розвинених de novo епізодів клінічно значущої СН зі зниженою фракцією викиду (ФВ) також належать більш легкі форми систолічної дисфункції, механічна диссинхронія, клапанна патологія та погіршення діастолічної функції, що навіть у разі відсутності значного зниження систолічної функції істотно погіршує наслідки СН [3, 4]. Отже, при СН перенесений ІМ – це фактор підвищеного ризику повторних коронарних подій, прогресування СН і смерті, незалежно від величини ФВ лівого шлуночка (ЛШ) [5–7], що вимагає від клініцистів підвищеної уваги до пацієнтів із поєднанням СН + перенесений ІМ. Проте досі фармакологічна корекція зазначених ризиків у цій популяції хворих на СН є значною клінічною проблемою [8, 9], хоча результати деяких досліджень інгібіторів натрійзалежного котранспортера глюкози 2 типу (іНЗКТГ2) вселяють певний оптимізм. Так, було показано, що іНЗКТГ2 знижують ризик подій, пов’язаних із СН, і смерті від серцево-судинних (СС) причин у широкого кола хворих на СН, при цьому результати метааналізів рандомізованих клінічних досліджень (РКД) іНЗКТГ2 при цукровому діабеті (ЦД) 2 типу вказують на зіставне поліпшення цих наслідків за наявності й за відсутності ІХС [10]. Однак загалом дані про здатність іНЗКТГ2 впливати на перебіг СН у пацієнтів із різним статусом ЦД і раніше перенесеним ІМ досі вкрай обмежені. Для вивчення цього дуже важливого питання Peikert et al. провели об'єднаний аналіз досліджень DAPA-HF (Dapagliflozin and Prevention of Adverse Outcomes in Heart Failure) і DELIVER (Dapagliflozin Evaluation to Improve the LIVEs of Patients With PReserved Ejection Fraction Heart Failure), спрямований на оцінку впливу перенесеного ІМ на ефективність і безпеку іНЗКТГ2 дапагліфлозину в пацієнтів із СН і різними значеннями ФВ ЛШ [11]. Основна інформація про цей аналіз стисло представлена в цій статті.
Методологія аналізу Peikert et al. DAPA-HF і DELIVER – це завершені міжнародні рандомізовані подвійні сліпі дослідження, які порівнювали терапію дапагліфлозином у дозі 10 мг/добу з плацебо в пацієнтів із симптоматичною СН. У дослідженні DAPA-HF брали участь пацієнти віком від 18 років із СН II–IV функціонального класу (ФК) за класифікацією Нью-Йоркської кардіологічної асоціації (New York Heart Association, NYHA), ФВ ЛШ (ФВЛШ) ≤40% і підвищеними рівнями N-термінального попередника мозкового натрійуретичного пептиду (NTproBNP). У дослідження DELIVER зараховували пацієнтів віком >40 років із СН II–IV ФК за NYHA, ФВ ЛШ >40%, підвищеними рівнями NT-proBNP і ознаками структурного захворювання серця (збільшення лівого передсердя або гіпертрофія ЛШ). Основними критеріями виключення в обох дослідженнях були ЦД 1 типу, симптоматична гіпотензія або систолічний артеріальний тиск (АТ) <95 мм рт. ст., а також знижена розрахункова швидкість клубочкової фільтрації (рШКФ) (<30 мл/хв/1,73м2 у дослідженні DAPA-HF та <25 мл/хв/1,73м2 у дослідженні DELIVER). В обох дослідженнях лікарі-дослідники реєстрували відомості про перенесений раніше ІМ у спеціальних електронних звітах [11]. Первинною кінцевою точкою в обох дослідженнях була комбінація СС смерті та погіршення перебігу СН (тобто незапланованої госпіталізації або термінового візиту до лікаря у зв'язку із СН, що потребує внутрішньовенної терапії). Також додатково оцінювали: окремі компоненти первинної кінцевої точки; комбінацію всіх подій, пов'язаних із СН (госпіталізації з приводу СН [гСН] і термінові візити до лікаря у зв'язку із СН), і СС смерті; комбінацію ІМ, інсульту і СС смерті (серйозні несприятливі СС події [major adverse cardiac events, MACE]); смерть від будь-якої причини; зміну балів за Канзаським опитувальником для хворих на кардіоміопатію (Kansas City Cardiomyopathy Questionnaire, KCCQ), зокрема загальної оцінки симптомів (total symptom score, TSS), клінічної сумарної оцінки (clinical summary score, CSS) і загальної сумарної оцінки (overall summary score, OSS), за період від вихідного рівня до закінчення 8-го місяця лікування.

Із метою оцінки безпеки терапії в обох дослідженнях вивчали серйозні небажані явища (СНЯ), небажані явища (НЯ), що призвели до припинення лікування, випадки ампутації кінцівок, діабетичного кетоацидозу, тяжкої гіпоглікемії, а також пов'язані з нирками й гіповолемією СНЯ і НЯ, що призвели до припинення лікування [11]. Вихідні характеристики пацієнтів узагальнювали у вигляді середнє значення ± стандартне відхилення (СВ), медіана (міжквартильний розмах [МКР]) або частота (%). Статистичні критерії, які використовували для порівняння вихідних характеристик пацієнтів з анамнезом і без анамнезу ІМ, залежали від розподілу (нормальний або відмінний від нормального) показників: для безперервних змінних це були t-критерій Стьюдента або ранговий критерій Вілкоксона відповідно, для категоріальних змінних – хі-квадрат і точний критерій Фішера відповідно. Зв'язки між статусом перенесеного ІМ (так vs ні) і клінічними подіями оцінювали за допомогою моделей пропорційних ризиків Кокса, стратифікованих з урахуванням дослідження, з поправкою на досліджуваний препарат, вік, стать, географічний регіон, систолічний АТ, частоту серцевих скорочень (ЧСС), індекс маси тіла (ІМТ), тривалість СН, попередні гСН, ФК за NYHA, ФВ ЛШ, наявність фібриляції (ФП) / тріпотіння (ТП) передсердь, артеріальної гіпертензії (АГ), інсульту, хронічної обструктивної хвороби легень, величину рШКФ і рівень NT-proBNP. Потім зв'язок між статусом перенесеного ІМ і частотою клінічних подій оцінювали в аналізі з використанням ФВ ЛШ як безперервної змінної за допомогою моделей регресії Пуассона. Для порівняння ефектів дапагліфлозину і плацебо використовували моделі пропорційних ризиків Кокса, стратифіковані за статусом ЦД 2 типу. Після чого оцінювали зв'язок між ефектом лікування і статусом ІМ в аналізі з використанням ФВ ЛШ як безперервної змінної за допомогою моделей регресії Пуассона. Результати порівнянь представлені у вигляді відношень ризиків (ВР) і відповідних 95% довірчих інтервалів (95% ДІ). При оцінці зміни балів за опитувальником KCCQ обчислювали частки учасників із клінічно значущим покращенням (збільшення на ≥5 балів) і погіршенням (зменшення на ≥5 балів) відповідних оцінок. Зв'язок між зміною оцінок KCCQ і статусом перенесеного ІМ оцінювали за допомогою моделей логістичної регресії. Ці ж моделі використовували для аналізу кінцевих точок безпеки. Результати порівнянь зі значеннями р <0,05 вважали статистично значущими [11].
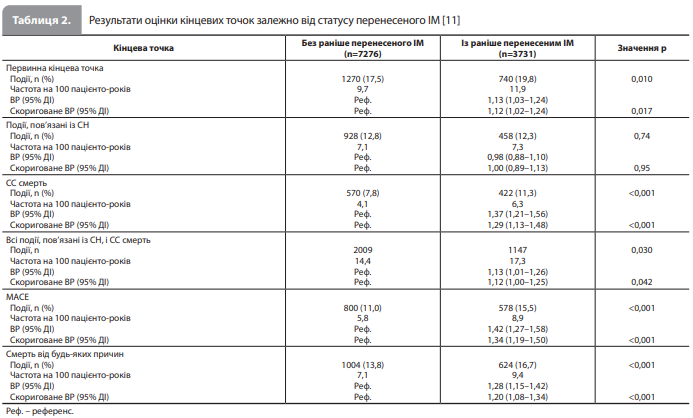
Результати аналізу Peikert et al. Вихідні характеристики учасників залежно від статусу перенесеного ІМ. З 11007 пацієнтів, рандомізованих у DAPA-HF і DELIVER, у 3731 (34%) в анамнезі був перенесений ІМ (у 44% пацієнтів із ФВ ЛШ ≤40% і у 26% із ФВ ЛШ >40%). Порівняно з хворими без ІМ в анамнезі пацієнти з перенесеним ІМ були молодшими, частіше були чоловіками, європеоїдами й пацієнтами європейських дослідницьких центрів, мали нижчі значення ІМТ, систолічного АТ, діастолічного АТ, ЧСС, ФВ ЛШ, рідше демонстрували ФП або ТП під час рандомізації та мали вищі рівні креатиніну, глікованого гемоглобіну і NT-proBNP. Пацієнти з раніше перенесеним ІМ мали в середньому тривалішу СН, серед них були більш поширені перенесений інсульт, дисліпідемія, ЦД 2 типу, АГ, паління, гСН в анамнезі, ІХС, черезшкірні коронарні втручання та аортокоронарне шунтування, тоді як ФП або ТП в анамнезі траплялися рідше, ніж у хворих без анамнезу ІМ. За ФК (NYHA) і балами за опитувальником KCCQ підгрупи пацієнтів з анамнезом і без анамнезу ІМ були зіставними. Що стосується фармакотерапії, пацієнти з перенесеним ІМ частіше отримували інгібітори ангіотензинперетворювального ферменту, комбінацію блокатора рецепторів ангіотензину та інгібітора неприлізину, бета-адреноблокатори, антагоністи мінералокортикоїдних рецепторів, нітрати, антиагреганти, гіполіпідемічну терапію і рідше приймали блокатори рецепторів ангіотензину та антикоагулянти, ніж учасники без анамнезу ІМ. І, нарешті, перенесений ІМ асоціювався з більшою ймовірністю перенесеної імплантації кардіовертера-дефібрилятора і з меншою ймовірністю використання кардіостимулятора порівняно з відсутністю ІМ в анамнезі (табл. 1) [11].

Клінічні наслідки залежно від статусу перенесеного ІМ. Частота всіх клінічних наслідків збільшувалася зі зниженням ФВ ЛШ в обох підгрупах пацієнтів, виділених з урахуванням статусу перенесеного ІМ (рис. 1). Пацієнти з перенесеним ІМ демонстрували вищий ризик первинної комбінованої кінцевої точки (погіршення перебігу СН або СС смерть) за усім спектром значень ФВ ЛШ (ВР 1,13, 95% ДІ 1,03–1,24), у тому числі після коригування на вихідні демографічні дані та прогностичні змінні (ВР 1,12, 95% ДІ 1,02–1,24) (рис. 1, табл. 2). У такий же спосіб, перенесений раніше ІМ був пов’язаний із вищим ризиком СС смерті, комбінації всіх подій, пов’язаних із СН, і СС смерті, ризиком MACE і смерті від усіх причин у моделях із коригуванням і без коригування на коваріати. Водночас статус перенесеного ІМ не впливав на ризик гСН ні до, ні після коригування з урахуванням коваріат, що може пояснюватися відносною давністю перенесеного ІМ у пацієнтів із відповідним анамнезом (давність ІМ ≥3 міс відповідно до критеріїв відбору) і, як наслідок, стабілізацією ризику в осіб із СН, що стала ускладненням ІМ, у зв'язку із завершенням періоду постінфарктного ремоделювання міокарда й проведенням науково обґрунтованої терапії [11].
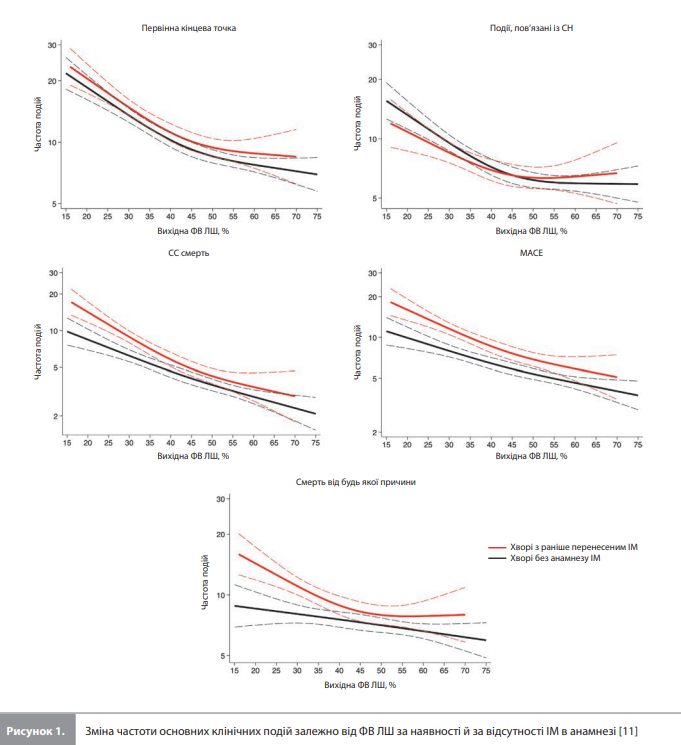
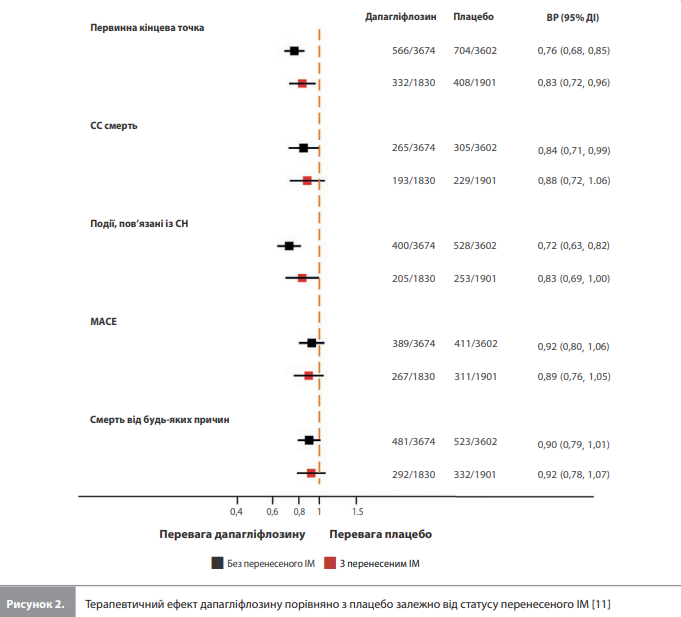
Ефекти дапагліфлозину на клінічні наслідки залежно від статусу перенесеного ІМ. Терапевтичні ефекти дапагліфлозину на ризик первинної комбінованої кінцевої точки не залежали від статусу перенесеного ІМ (у пацієнтів з анамнезом ІМ ВР становило 0,83, 95% ДІ 0,72–0,96, у пацієнтів без анамнезу ІМ – 0,76, 95% ДІ 0,68–0,85; pдля взаємодії 0,36) (табл. 3, рис. 2) [11]. Також статус ІМ не змінював ефекти дапагліфлозину на ризики погіршення перебігу СН, СС смерті, ризик комбінації всіх подій, пов'язаних із СН, і СС смерті, ризик MACE та смертність від усіх причин (рдля взаємодії ≥0,15 для всіх наслідків) (табл. 3, рис. 2) [11]. Покращення (збільшення на ≥5 балів) оцінок KCCQTSS, KCCQ-CSS і KCCQ-OSS було більш розповсюдженим при застосуванні дапагліфлозину порівняно з плацебо як за наявності анамнезу ІМ, так і без нього, при цьому в підгрупі хворих з ІМ в анамнезі, що отримували дапагліфлозин, спостерігали найменшу частку пацієнтів із клінічно значущим погіршенням (зменшення на ≥5 балів) оцінки KCCQ-CSS (табл. 3) [11]. В аналізі з використанням ФВ ЛШ як безперервної змінної значення ФВ ЛШ не впливало на зв’язок між ефектами дапагліфлозину на клінічні наслідки і статусом ІМ (pдля взаємодії ≥0,24 для всіх наслідків) [11].
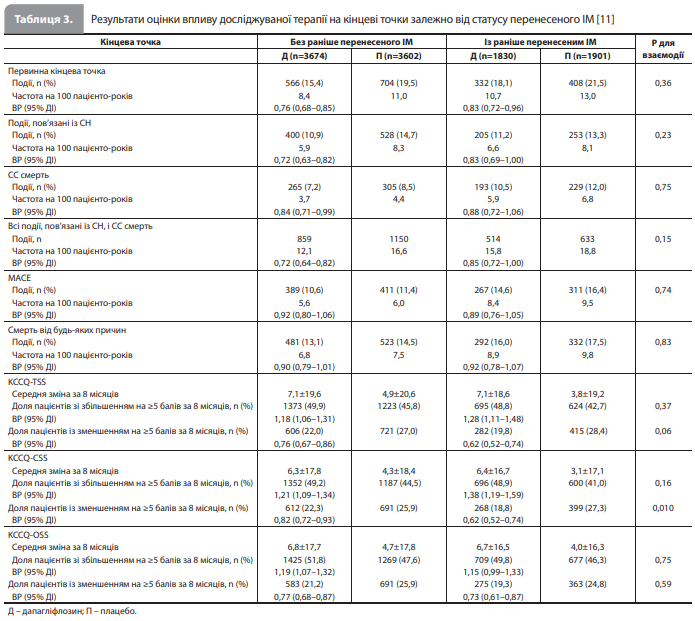
Безпека. Показники частоти припинення лікування з будь-якої причини або через НЯ, а також показники частоти СНЯ, діабетичного кетоацидозу, гіпоглікемії та інших досліджуваних проблем із безпекою (зокрема пов'язаних із нирками та гіповолемією СНЯ і НЯ, що призвели до припинення лікування), були зіставними в групах дапагліфлозину й плацебо, незалежно від статусу перенесеного ІМ [11].
Висновки за результатами аналізу Peikert et al. У цьому заздалегідь запланованому об'єднаному вторинному аналізі даних 11 007 хворих на СН, які взяли участь у дослідженнях DAPA-HF і DELIVER, третина учасників мала ІМ в анамнезі, що значно підвищувало ризик несприятливих СС наслідків за різних значень ФВ ЛШ, навіть у пацієнтів зі збереженою ФВ. Водночас терапевтична ефективність дапагліфлозину у вигляді полегшення симптомів СН і зниження ризику клінічних наслідків, і передусім комбінації погіршення перебігу СН і СС смерті (первинної кінцевої точки), проявлялася однаково в пацієнтів з анамнезом і без анамнезу ІМ; також статус перенесеного ІМ не впливав на безпеку дапагліфлозину. Слід зазначити, що серед учасників досліджень DAPA-HF і DELIVER не було пацієнтів із давністю ІМ менше ніж 3 місяці (критерій виключення з обох цих досліджень), тому в популяції пацієнтів із СН і раніше перенесеним ІМ результати, отримані Peikert et al., стосуються тільки хворих із тривалішим постінфарктним періодом [11]. Проте представлені результати доповнюють отримані раніше дані про істотні корисні ефекти й сприятливий профіль безпеки дапагліфлозину при СН із різними значеннями ФВ ЛШ і підтримують його застосування в групі високого ризику, до якої належать пацієнти з СН і раніше перенесеним ІМ.
Список літератури знаходиться в редакції
Автор огляду Наталія Генш Medicine Review 2024; 7 (80): 11 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2026. Усі права захищені.
|
мапа сайту корисні посилання |