Оптимальний антиагрегант для пацієнтів з ІМпST, які пройшли тромболізис: нові результати дослідження TRЕATНезважаючи на активне впровадження черезшкірного коронарного втручання (ЧКВ) в практику ведення пацієнтів з інфарктом міокарда (ІМ), фібринолітична терапія залишається важливою стратегією лікування хворих з ІМ з підйомом сегмента ST (ІМпST) в умовах, коли неможливо вчасно виконати первинне ЧКВ [1]. Важливим доповненням до тромболітичного агенту в цій ситуації є антиагрегантна терапія комбінацією ацетилсаліцилової кислоти (АСК) і клопідогрелю, що забезпечує зниження ризику серцево-судинних (СС) явищ і загальної смертності в даній вибірці пацієнтів [1–3]. З появою в арсеналі лікарів тикагрелору, зворотного прямого перорального антагоніста рецепторів аденозиндифосфата (P2Y12-рецепторів), що забезпечує більш виражене і стабільне пригнічення рецепторів тромбоцитів і більш швидкий розвиток ефекту порівняно з клопідогрелем [4, 5], постало питання про можливість використання цього нового антиагреганта (замість клопідогрелю) разом з АСК у пацієнтів з ІМпST, які проходять фібриноліз. У дослідженні PLATO (Platelet Inhibition and Patient Outcomes) – основному дослідженні тикагрелору при гострому коронарному синдромі – тикагрелор перевершив клопідогрель зі здатності знижувати частоту великих СС явищ [6], проте в це дослідження включалися лише пацієнти, які проходили первинне ЧКВ, у той час як фібриноліз, проведений протягом останніх 24 год, був критерієм виключення. Тому сприятливі для тикагрелору результати PLATO не можуть автоматично поширюватися на хворих з ІМпST, яким проводиться тромболітична терапія. Згодом для вирішення питання про можливість використання тикагрелору в поєднанні з фібринолітичним агентом при ІМпST було організовано дослідження TREAT (TicagRElor in pAtients with STelevation myocardial infarction treated with pharmacological Thrombolysis). Первинною кінцевою точкою цього дослідження була 30-денна частота великих кровотеч, і первинний аналіз результатів показав, що застосування тикагрелору з досліджуваного показання можна вважати безпечним, оскільки показники частоти великих кровотеч у групах тикагрелору і клопідогрелю були порівнянними [7–9]. У зв'язку з цим великий інтерес представляють дані вторинних аналізів результатів TREAT, які оцінювали 12-місячні показники ефективності й безпеки досліджуваних варіантів антиагрегантної терапії и які будуть коротко представлені в цьому огляді [10].
Дизайн і основні характеристики дослідження TREAT Дослідження TREAT – це академічне, міжнародне, багатоцентрове, рандомізоване, відкрите дослідження фази 3 з оцінкою наслідків експертами, які не мали доступу до кодів лікування. У дослідженні взяли участь дослідницькі центри 10 країн (Аргентина, Австралія, Бразилія, Канада, Китай, Колумбія, Нова Зеландія, Перу, Росія і Україна). Учасниками були пацієнти, які надійшли до стаціонару протягом 24 год після появи симптомів гострого ІМ з підйомом сегмента ST на електрокардіограмі (як мінімум на 2 мм в 2 суміжних периферичних або прекардіальних відведеннях у чоловіків і на 1,5 мм в відведеннях V1–V3 у жінок і на 1 мм у відведеннях від кінцівок). Всі учасники були молодші ніж 75 років і отримували фібринолітичну терапію. Основними критеріями виключення були: наявність будь-яких протипоказань до застосування досліджуваних препаратів, отримання пероральних антикоагулянтів, підвищений ризик брадикардії і супутня терапія сильним інгібітором або індуктором цитохрому P450 3A. Пацієнтів рандомізували (у співвідношенні 1:1) для отримання тикагрелору (навантажувальна доза 180 мг) або клопідогрелю (навантажувальна доза 300– 600 мг) у найкоротші можливі терміни після розвитку індексного явища, але не більше ніж через 24 год після розвитку ІМ. Пацієнти, які отримували клопідогрель до рандомізації, також відповідали критеріям відбору; якщо при рандомізації вони потрапляли в групу тикагрелору, їм була рекомендована навантажувальна доза препарату (180 мг), якщо в групу клопідогрелю, то могли отримати додатково 300 мг клопідогрелю при проходженні ЧКВ, на розсуд дослідника і відповідно до місцевих протоколів. Згодом пацієнти отримували підтримуючу терапію антиагрегантами: тикагрелором у дозі 90 мг 2 рази на добу або клопідогрелем у дозі 75 мг 1 раз на добу відповідно до результатів рандомізації. Усі учасники дослідження отримували АСК в дозі 75–100 мг/доба протягом усього періоду спостереження (за винятком випадків непереносимості АСК). При надходженні до стаціонару пацієнти, які раніше не вживали АСК, отримували навантажувальну дозу 162–325 мг препарату. Решта аспектів ведення пацієнтів відповідали діючим керівництвам з тактики ведення ІМпST [11, 12]. Рішення про застосування інших препаратів і методів для лікування гострого ІМпST, а також рішення про проведення подальших процедур реваскуляризації залишалися на розсуд лікарів. Дотримання рекомендацій учасниками дослідження оцінювалося дослідниками і координаторами досліджень за кількістю прийнятих таблеток і за повідомленнями пацієнтів. Первинною кінцевою точкою дослідження TREAT була 30-денна частота великих кровотеч за визначенням з дослідження TIMI (Thrombolysis In Myocardial Infarction) [7]. Кінцевими точками ефективності, які є предметом вторинних аналізів, що розглядаються у цій публікації, були комбінація ІМ, інсульту або смерті від судинних причин (аналогічно первинній кінцевій точці дослідження PLATO), а також комбінація цих трьох явищ з важкою рецидивною ішемією, транзиторною ішемічною атакою (ТІА) й іншими артеріальними тромботичними подіями через 12 міс спостереження. Крім того, автори оцінили 12-місячну частоту окремих компонентів зазначених кінцевих точок ефективності й річний рівень загальної смертності. Вторинні кінцеві точки оцінки безпеки включали великі кровотечі, клінічно значущі невеликі кровотечі і невеликі кровотечі за визначенням TIMI, а також великі або невеликі кровотечі за визначенням дослідження PLATO і визначенням Академічного консорціуму з вивчення кровотеч (Bleeding Academic Research Consortium, BARC) [10].
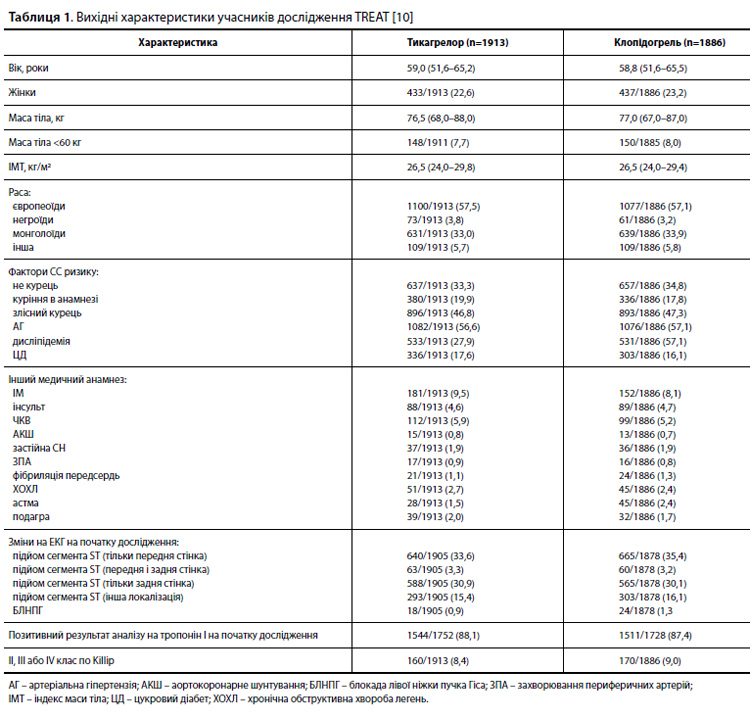
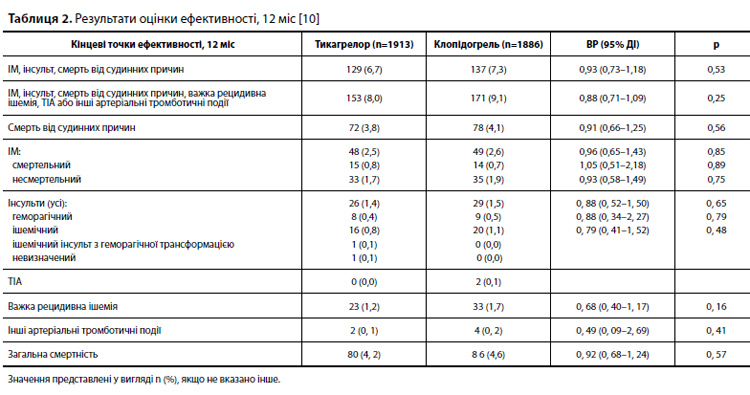
Оскільки обсяг вибірки учасників розраховувався для оцінки первинної кінцевої точки – 30-денної частоти великих кровотеч – і на початку не брав до уваги оцінку вторинних кінцевих точок ефективності, то вторинний аналіз частоти основних СС явищ вважається пошуковим. Водночас, усі аналізи ефективності були заздалегідь описані в плані статистичного аналізу [10]. Безперервні змінні були представлені у вигляді «середнє значення ± стандартне відхилення» або «медіана (міжквартильний розмах [МКР])», залежно від ситуації, а категоріальні змінні – як показники частоти. Усі рандомізовані пацієнти були включені до вибірки intention-totreat (ITT). Результати аналізували за допомогою моделі пропорційних ризиків Кокса. Для кожної кінцевої точки розраховували відношення ризиків (ВР) і двобічний 95% довірчий інтервал (ДІ). Крім аналізу даних ITT вибірки проводили аналіз показників ефективності в підгрупах пацієнтів, виділених з урахуванням приналежності до певної статі, наявності цукрового діабета, часу від розвитку індексної події до рандомізації (>12 або ≤12 год), оцінки ризику за Killip, прийому клопідогрелю до рандомізації, використання для тромболізису фібрин-специфічного або фібрин-неспецифічного препарату і виконання ЧКВ. Для всіх аналізів обчислювалися двобічні значення р [10].
Результати За період з листопада 2015 по листопад 2017 року в дослідження були зараховані 3799 пацієнтів з 152 центрів в 10 країнах. Період подальшого спостереження тривав 12 міс і закінчився в листопаді 2018 року; на той час була доступна інформація про всіх пацієнтів, за винятком 55 осіб. Вихідні характеристики учасників представлені в таблиці 1, а саме: середній вік – 58±9,5 років, чоловіки – 77,1%, курці – 47,1%, наявність в анамнезі ІМ – 8,8%. У цілому 99,9% пацієнтів отримували фібринолітики, з яких 75,9% – фібрин-специфічний препарат. Групи лікування (тикагрелор vs клопідогрель) були добре збалансовані за вихідними і демографічними характеристиками. В обох групах медіана часу від появи болю в грудях до проведення фібринолітичної терапії становила 2,6 год (МКР 1,5–4,3 год), а медіана часу від фібринолітичної терапії до рандомізації – 11,4 год (МКР 5,8–18,1 год). В обох групах 89,4% пацієнтів отримали клопідогрель до рандомізації, як правило, у дозі 300 мг. АСК отримували в цілому 98,8% пацієнтів. Загальний рівень прихильності до прийому досліджуваних препаратів через 12 міс становив 90,4% [10].
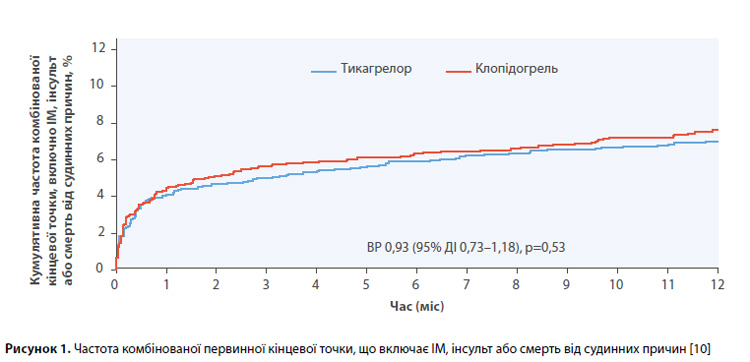
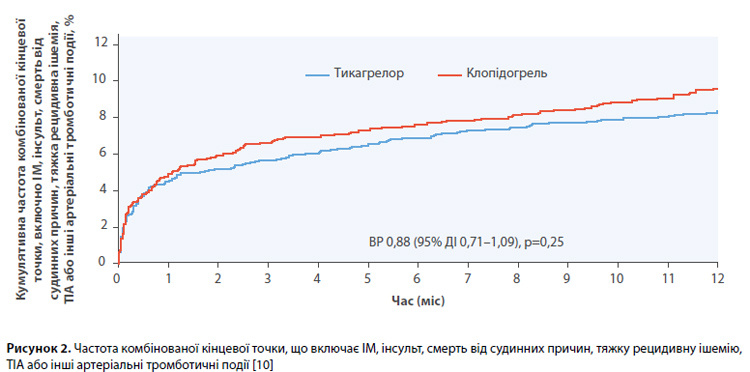
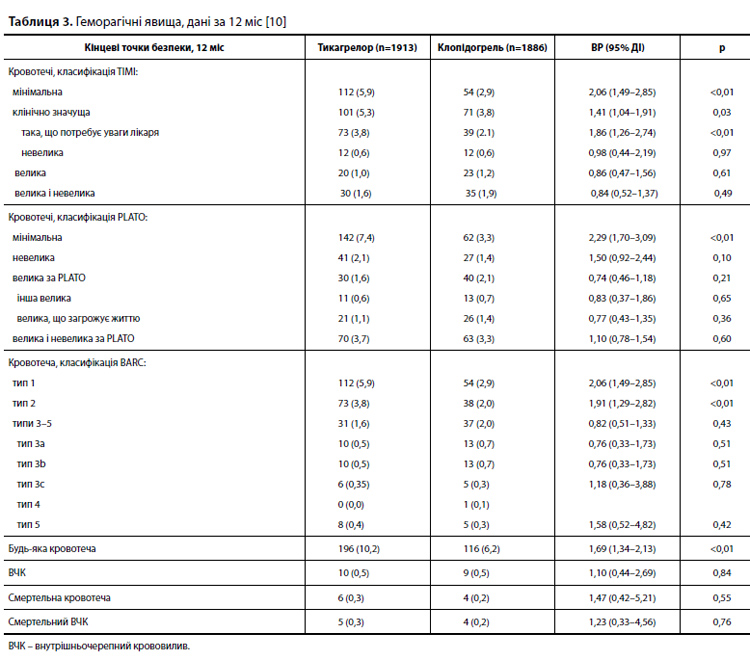
Результати оцінки ефективності через 12 міс лікування представлені в таблиці 2. Комбінована кінцева точка, що включає ІМ, інсульт або смерть від судинних причин, була зареєстрована у 129 з 1913 пацієнтів (6,7%), які отримували тикагрелор, і у 137 з 1886 пацієнтів (7,3%), які отримували клопідогрель (ВР 0,93; 95% ДІ 0,73–1,18; p=0,53) (рис. 1). Друга комбінована кінцева точка, що включає інсульт, ІМ, смерть від судинних причин, важку рецидивну ішемію, ТІА або інші артеріальні тромботичні події, була зареєстрована у 153 з 1913 пацієнтів (8,0%), які отримували тикагрелор, і у 171 з 1886 пацієнтів (9,1%), які отримували клопідогрель (ВР 0,88; 95% ДІ 0,71–1,09; p=0,25) (рис. 2). Показники частоти індивідуальних компонентів кінцевих точок, рівні загальної і СС смертності, а також показники частоти ІМ були порівнянними в групах тикагрелору та клопідогрелю; проте для інсульта, важкої рецидивної ішемії та інших артеріальних тромботичних подій показники були чисельно (але статистично не значимо) нижчими в групі тикагрелору [10]. У таблиці 3 представлені результати оцінки безпеки; 12-місячна частота великих кровотеч за критеріями TIMI становила 1,0% у групі тикагрелору і 1,2% – у групі клопідогрелю (ВР 0,86; 95% ДІ 0,47–1,56; p=0,61). Частота великих кровотеч за критеріями PLATO становила 1,6 і 2,1% відповідно (ВР 0,74; 95% ДІ 0,46–1,18; p=0,21), а частота кровотеч 3–5 типів за критеріями BARC – 1,6 і 2,0% відповідно (ВР 0,82; 95% ДІ 0,51–1,33; p=0,43). Показники частоти смертельних кровотеч (0,3 vs 0,2%; p=0,55) і внутрішньочерепних крововиливів (0,3 vs 0,2%; p=0,76) були порівнянними в групах тикагрелору і клопідогрелю. Водночас мінімальні кровотечі за критеріями TIMI (5,9 vs 2,9%; p<0,01), а також кровотечі, що вимагають уваги лікаря, за критеріями TIMI (3,8 vs 2,1%; p<0,01), розвивалися частіше на тлі прийому тикагрелору, ніж клопідогрелю [10]. Частота припинення прийому досліджуваного препарату внаслідок серйозних небажаних явищ була порівнянною в групах тикагрелору і клопідогрелю (0,7 vs 0,3%; p=0,24). Задишка частіше реєструвалася в групі тикагрелору, ніж у групі клопідогрелю (23,9 vs 13,7% пацієнтів відповідно). Кілька пацієнтів припинили прийом тикагрелору через задишку (1,9% пацієнтів у групі тикагрелору, 0 пацієнтів у групі клопідогрелю). За іншими серйозними небажаними явищам досліджувані групи були порівнянними. Порівняння препаратів у підгрупах показало співмірні результати оцінки ефективності лікування [10].
Обговорення і висновки Незважаючи на те що первинне ЧКВ вважається пріоритетним методом реперфузії міокарда у пацієнтів з ІМпST [12], можливості фібринолітичної терапії як і раніше широко використовуються лікарями у всьому світі [13]. Діючі керівництва з ведення пацієнтів з гострим коронарним синдромом/ІМ рекомендують призначення подвійної антиагрегантної терапії комбінацією АСК + клопідогрель у якості доповнення до фібринолітику для поліпшення клінічних результатів у пацієнтів з ІМпST. Ті самі керівництва (опубліковані в 2016–2018 рр.) не рекомендують вводити тикагрелор протягом 24 год після фібринолітичної терапії через відсутність даних, що підтверджують безпеку такого підходу [14, 15]. Дослідження TREAT було заплановано, щоб заповнити пробіл у цій галузі медичних знань, і тому основною його метою було порівняти 30-денну безпеку терапії із застосуванням тикагрелору і клопідогрелю у пацієнтів з ІМпST, що перенесли фібриноліз [7]. Цю мету було досягнуто, оскільки аналіз первинної кінцевої точки показав порівнянну частоту великих кровотеч в учасників TREAT у групах тикагрелору і клопідогрелю. Внаслідок особливостей дизайну дослідження, результати вторинних аналізів, які проводилися для оцінки кінцевих точок ефективності і безпеки, є пошуковими, однак без розгляду цих даних загальна інтерпретація результатів дослідження буде неповною. Як наслідок, результати вторинного аналізу 12-місячних даних дослідження TREAT, що представлені в цьому огляді, також потрібно брати до уваги і враховувати у разі вибору тактики лікування [10]. Представлений аналіз показав, що у пацієнтів з ІМпST молодших ніж 75 років, які пройшли терапію тромболітичним препаратом у якості вихідної стратегії реперфузії, уведення тикагрелору не призвело до зниження 12-місячної частоти великих СС явищ порівняно з клопідогрелем, незважаючи на більш сильне пригнічення функції тромбоцитів під дією тикагрелору, яке підтверджується більш високою частотою невеликих кровотеч у пацієнтів, що отримували тикагрелор [10]. Слід зазначити, що порівнянна ефективність антиагрегантів у дослідженні TREAT (за даними оцінки комбінованої кінцевої точки, що включає ІМ, інсульт або смерть від судинних причин) вочевидь суперечить результатам дослідження PLATO, включаючи результати аналізу в підгрупі PLATO-STEMI. Проте, цю різницю потрібно інтерпретувати з обережністю з огляду на відмінність між PLATO і TREAT із статистичної потужності для оцінки кінцевих точок ефективності. Між тим, результати оцінки другої кінцевої точки ефективності (комбінація ІМ, інсульту, смерті від судинних причин, важкої рецидивної ішемії, ТІА та інших артеріальних тромботичних подій) були порівнянними в дослідженнях TREAT (ВР 0,88) і PLATO (ВР 0,88 в основному аналізі і ВР 0,87 в аналізі підгрупи PLATO-STEMI) [10]. При інтерпретації результатів дослідження TREAT також слід враховувати низку інших обмежень, у тому числі неможливість екстраполяції даних на пацієнтів віком 75 років і понад (які виключалися з дослідження) і відкритий режим лікування (унаслідок неможливості використання дизайну подвійного сліпого дослідження). Водночас, нині TREAT є найбільшим рандомізованим дослідженням з оцінки тикагрелору у пацієнтів з ІМпST, які отримували лікування фібринолітиками, а також найбільшим дослідженням з оцінки ефектів подвійної антиагрегантної терапії через 12 міс після фібринолітичної терапії, оскільки в попередніх дослідженнях аналогічної тематики період спостереження був обмежений 30 днями [2, 3]. Тому результати дослідження TREAT дозволяють підвищити рівень інформаційної підтримки лікарських рішень і вказують на те, що тикагрелор може бути безпечним альтернативним антиагрегантом, який можна використовувати при ІМпST після фібринолітичної терапії. Крім того, отримані результати можуть і зобов'язані стати основою для подальших досліджень антитромботичної терапії в контексті застосування фібринолізу у пацієнтів з ІМпSТ, у тому числі рандомізованих досліджень і досліджень в умовах реальної клінічної практики [10].
Підсумки Отже, результати вторинного аналізу даних, отриманих за 12 міс спостереження в дослідженні TREAT, показали, що у пацієнтів з ІМпST віком <75 років введення тикагрелору після фібринолітичної терапії не забезпечує значного зниження 12-місячної частоти СС явищ порівняно з використанням клопідогрелю. Водночас, не зважаючи на велику частоту невеликих кровотеч і задишки в групі тикагрелора, отримані результати в цілому підтверджують безпеку застосування тикагрелору упродовж 12 міс після ІМпST/ фібринолізу, аналогічну безпеці терапії клопідогрелем. Література 1. Ibanez B., James S. et al. 2017 ESC Guidelines for the management of acute myocardial infarction in patients presenting with ST-segment elevation. The Task Force for the management of acute myocardial infarction in patients presenting with ST-segment elevation of the European Society of Cardiology (ESC). European Heart Journal (2018) 39, 119-177. 2. Chen Z., Jiang L., Chen Y. et al.COMMIT (ClOpidogrel and Metoprolol in Myocardial Infarction Trial) Collaborative Group. Addition of clopidogrel to aspirin in 45,852 patients with acute myocardial infarction: randomised placebo-controlled trial. Lancet 2005; 366 (9497): 1607-1621. 3. Sabatine M., Cannon C., Gibson C. et al. CLARITY-TIMI 28 Investigators. Addition of clopidogrel to aspirin and fibrinolytic therapy for myocardial infarction with ST-segment elevation. N Engl J Med 2005; 352 (12): 1179-1189. 4. Husted S., Emanuelsson H., Heptinstall S. et al. Pharmacodynamics, pharmacokinetics, and safety of the oral reversible P2Y12 antagonist AZD6140 with aspirin in patients with atherosclerosis : a double-blind comparison to clopidogrel with aspirin. Eur Heart J 2006; 27: +1038-47. 5. Husted S., van Giezen J. Ticagrelor: the first reversibly binding oral P2Y12 receptor antagonist. Cardiovascu Ther 2009 року; 27: 259-74. 6. Wallentin L., Becker R., Budaj A. et al. Ticagrelor versus clopidogrel in patients with acute coronary syndromes. N Engl J Med 2009 року; 361: 1045-57. 7. Berwanger O., Nicolau J., Carvalho A. et al. Ticagrelor vs clopidogrel after fibrinolytic therapy in patients with ST-elevation myocardial infarction : a randomized clinical trial. JAMA Cardiol 2018; 3: 391-9. 8. Kheiri B., Osman M., Abdalla A. et al. Ticagrelor versus clopidogrel after fibrinolytic therapy in patients with ST-elevation myocardial infarction: a systematic review and meta-analysis of randomized clinical trials. J Thromb Thrombolysis 2018; 46: 299-303. 9. Berwanger O., Abdelhamid M., Alexander T. et al. Use of ticagrelor alongside fibrinolytic therapy in patients with ST-segment elevation myocardial infarction : practical perspectives based on data from the TREAT study. Clin Cardiol 2018; 41: 1 322-7. 10. Berwanger O., Lopes R., Moia D. et al. Ticagrelor Versus Clopidogrel in Patients With STEMI Treated With Fibrinolysis. TREAT Trial. J Am Coll Cardiol 2019; 73: 2819-28. 11. O’Gara P., Kushner F., Ascheim D. et al. 2013 ACCF/AHA guideline for the management of ST-elevation myocardial infarction: executive summary: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines: developed in collaboration with the American College of Emergency Physicians and Society for Cardiovascular Angiography and Interventions. J Am Coll Cardiol 2013; 61: 485-510. 12. Ibanez B., James S., Agewall S. et al. 2017 ESC guidelines for the management of acute myocardial infarction in patients presenting with ST-segment elevation: the Task Force for the Management of Acute Myocardial Infarction in Patients Presenting With ST-Segment Elevation of the European Society of Cardiology (ESC). Eur Heart J 2018; 39: 119-77. 13. Bates E. Evolution from fibrinolytic therapy to a fibrinolytic strategy for patients with STsegment-elevation myocardial infarction. Circulation 2014; 130: +1133-5. 14. Valgimigli M., Bueno H., Byrne R. et al. 2017 ESC focused update on dual antiplatelet therapy in coronary artery disease developed in collaboration with EACTS: The Task Force for dual antiplatelet therapy in coronary artery disease of the European Society of Cardiology (ESC) and of the European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J 2018; 39: 213-60. 15. Levine G., Bates E., Bittl J. et al. 2016 ACC/AHA guideline focused update on duration of dual antiplatelet therapy in patients with coronary artery disease: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. J Am Coll Cardiol 2016 року; 68: 1082-115. Автор огляду Микола Горін  Medicine Review 2020; 4 (59): 35 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2025. Усі права захищені.
|
мапа сайту корисні посилання |