Порівняння ефективності, безпеки та вартості терапії із застосуванням еноксапарину і НФГ у пацієнтів з гострим коронарним синдромом: аналіз бази реальних клінічних данихЯк відомо, гострий коронарний синдром (ГКС), що представляє гостру форму ішемічної хвороби серця, є комбінацією трьох клінічних синдромів: інфаркту міокарда (ІМ) з підйомом сегмента ST (ІМпST), ІМ без підйому сегмента ST (ІМбпST) і нестабільної стенокардії (НС), за яких застосовуються багато в чому порівнянні тактики ведення пацієнтів [1]. При цьому, незважаючи на істотне зростання ефективності медичних втручань, значна кількість хворих з ГКС віком понад 40 років (близько 18–23%) вмирають протягом року після першої коронарної катастрофи [2, 3]. Крім того, в західних країнах ГКС є одним з найдорожчих захворювань: наприклад, в США, щорічні витрати на лікування цих синдромів становлять близько 85 млрд дол. [3], що в поєднанні з високим рівнем смертності робить подальшу оптимізацію стратегій ведення ГКС пріоритетною проблемою охорони здоров'я. Сучасна фармакотерапія гострої фази ГКС включає застосування антиішемічниїх, антиагрегантних і антикоагулянтних препаратів. Серед останніх найбільшої уваги заслуговують нефракціонований гепарин (НФГ), як традиційний антикоагулянт для лікування ГКС, і еноксапарин – як низькомолекулярний гепарин (НМГ), найбільш часто використовуваний для лікування пацієнтів з ГКС і профілактики ішемічних ускладнень [4–6]. Порівняно з НФГ еноксапарин має більш передбачувану фармакокінетику, не викликає розвитку гепариніндукованої тромбоцитопенії (ГІТ), не вимагає частого моніторингу функції системи згортання крові і корекції дози [7]. Діючі керівництва Американської кардіологічної асоціації та (AHA)/Американського коледжу кардіологів (АСС) і Європейського товариства кардіологів (ESC) рекомендують використовувати еноксапарин і НФГ як основні парентеральні антикоагулянти для лікування НС та ІМбпST незалежно від обраної стратегії лікування (консервативна або інвазивна), а також на додаток до фибринолізу або до первинного черезшкірного коронарного втручання (ЧКВ) при ІМпST [8]. З моменту завершення досліджень, що підтримують ці рекомендації, пройшло 10–20 років, і за цей час сталося чимало змін в арсеналі лікарських препаратів і тактиці ведення пацієнтів з ГКС, зокрема стали широко використовуватися нові антиагрегантні препарати (тикагрелор і прасугрел). З огляду на те що згортання крові є загальною мішенню для антиагрегантів і антикоагулянтів, які використовуються при ГКС, дуже важливо оцінити можливий вплив нових антиагрегантів і нових стратегій лікування на ефективність і безпеку НФГ і еноксапарину у сучасних пацієнтів з ГКС. Для вивчення цього питання Rosenthal et al. провели аналіз відомостей про реальних хворих з бази даних Premier Healthcare Database (PHD), зробивши акцент на порівнянні клінічних результатів, безпеки і вартості застосування еноксапарину й НФГ в умовах сучасної клінічної практики [9]. Автори вивчили дані про використання та предиктори призначення того чи іншого антикоагулянту під час стаціонарного лікування ГКС, відомості про ефективність еноксапарину і НФГ у профілактиці внутрішньолікарняної смертності та ішемічних ускладнень й пов'язаний з лікуванням ризик великої кровотечі протягом 30 днів після виписки зі стаціонару. Також було проведено порівняння загальних витрат на лікування еноксапарином і НФГ у пацієнтів у зазначеній вибірці.
Методологія аналізу та досліджувана вибірка На момент аналізу база даних PHD містила відомості про більш ніж 750 млн звернень пацієнтів (стаціонарних і амбулаторних за направленням зі стаціонару) з більш ніж 850 клінік і лікарень, тобто охоплювала приблизно 25% усіх госпіталізацій, які відбулися в США в період між 2000 і 2018 рр. В PHD зберігаються дані зі стандартних виписних епікризів, у тому числі демографічні характеристики і відомості про стан пацієнта, інформація про всі оплачувані послуги (наприклад, лікарські препарати, лабораторні аналізи, діагностичні і терапевтичні процедури), а також інформація про лікарні, у яких лікувався пацієнт. Досліджувана вибірка складалася з пацієнтів віком ≥18 років, госпіталізованих у період 2010–2016 рр. у зв'язку з НС, ІМбпST або ІМпST, для яких у базі PHD були дані, що охоплюють 90-денний період до і 30-денний період після індексної госпіталізації з приводу ГКС. З вибірки виключали пацієнтів, які відповідають таким критеріям: 1) наявність гострого ІМ або НС протягом 90 днів до індексної госпіталізації; 2) смерть пацієнта під час індексної госпіталізації; 3) наявність геморагічних синдромів або тромбофілій (наприклад, дефіцит антитромбіну, протеїнів C або S, наявність фактора V Лейден, мутація протромбіну G20210A), антифосфоліпідного синдрома, тромбоцитопенії, а також інших протипоказань до застосування антикоагулянтів, у тому числі активна шлунково-кишкова виразка, а також гастрит або дуоденіт з кровотечею, аневризма аорти або головного мозку, цироз печінки, перикардит, вагітність або післяпологовий період протягом 90 днів до або під час індексної госпіталізації [9]. Первинними кінцевими точками дослідження були загальна внутрішньолікарняна смертність, нефатальний ІМ (включно ІМбпST, ІМпST) і рецидивуюча стенокардія, а також комбінація цих подій (комбінована ішемічна кінцева точка) під час будь-якого візиту в лікарню протягом 30 днів після завершення індексної госпіталізації (виписки зі стаціонару). Вторинними кінцевими точками були поширеність використання антикоагулянту, вартість лікування еноксапарином і НФГ, загальні витрати на медикаменти, загальні витрати на індексну госпіталізацію і загальні витрати на всі госпіталізації за період спостереження, загальна тривалість стаціонарного лікування і 30-денний ризик повторної госпіталізації. Ризик великих кровотеч (включно субарахноїдальний крововилив, внутрішньомозковий крововилив, інший і неуточнений внутрішньочерепний крововилив, неуточнена кровотеча, шлунково-кишкова кровотеча і кровохаркання) та ГІТ оцінювали за період стаціонарного лікування і 30-денного подальшого спостереження [9]. У якості предикторів призначення еноксапарину оцінювали характеристики пацієнта (стать, вік, раса, етнічна приналежність, тип страхування), характеристики лікарні (розмір, академічний статус, населення, яке обслуговується, географічний регіон), а також характеристики візиту й клінічні характеристики (тип госпіталізації, статус при виписці, перебування у відділенні інтенсивної терапії [ВІТ], індекс коморбідності Чарлсона, тяжкість захворювання згідно з індексом All patientrefined diagnosisrelated groups [APRDRG], період застосування антикоагулянту [у днях], використання антиагрегантів, крім ацетилсаліцилової кислоти [АСК], використання антиішемічних препаратів [бетаблокаторів, інгібіторів ангіотензинперетворювальго ферменту, блокаторів кальцієвих каналів], виконання коронарної ангіографії і коронарної ангіопластики під час індексної госпіталізації). Ці предикторні змінні також використовувались як коваріати в багатофакторному моделюванні для оцінки відмінностей між еноксапарином і НФГ за первинними кінцевим точкам [9]. Безперервні дані були представлені у вигляді середніх значень і стандартних відхилень (СВ) або медіан і міжквартильних розмахів (МКР). Для виявлення статистично значимих предикторів використання еноксапарину і порівняння груп монотерапії еноксапарином і монотерапії НФГ за ризиком досягнення кінцевих точок використовували багатофакторний логістичний регресійний аналіз. Рівень статистичної значимості був встановлений рівним 0,05 [9].
Результати аналізу Rosenthal et al. Використання антикоагулянтів. Із 1 048 053 унікальних пацієнтів з ГКС, які відповідали критеріям відбору, під час індексної госпіталізації у 219 259 (20,9%) осіб була діагностована НС, у 582 134 (55,6%) – ІМбпST і у 246 660 (23,5%) – ІМпST. Із загальної вибірки пацієнтів з ГКС 11,4% хворих отримали монотерапію еноксапарином і 47,4% – монотерапію НФГ. Інформація про розподіл антикоагулянтів за трьома когортам пацієнтів з різними типами ГКС представлена в таблиці 1. Зокрема, з таблиці видно, що серед пацієнтів з НС 12,0% отримували монотерапію еноксапарином і 45,1% – монотерапію НФГ. Серед пацієнтів з ІМбпST еноксапарин використовували дещо частіше (13,9%), а НФГ – рідше (43,1%), ніж при НС, у той час як при ІМпST еноксапарин використовували значно рідше (5,1%), а НФГ – істотно частіше (59,8%) порівняно з пацієнтами з НС або ІМбпST [9].
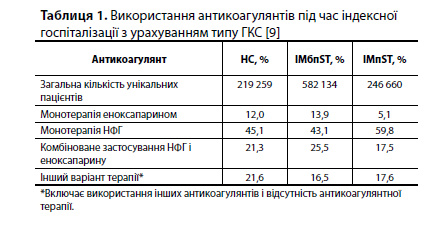
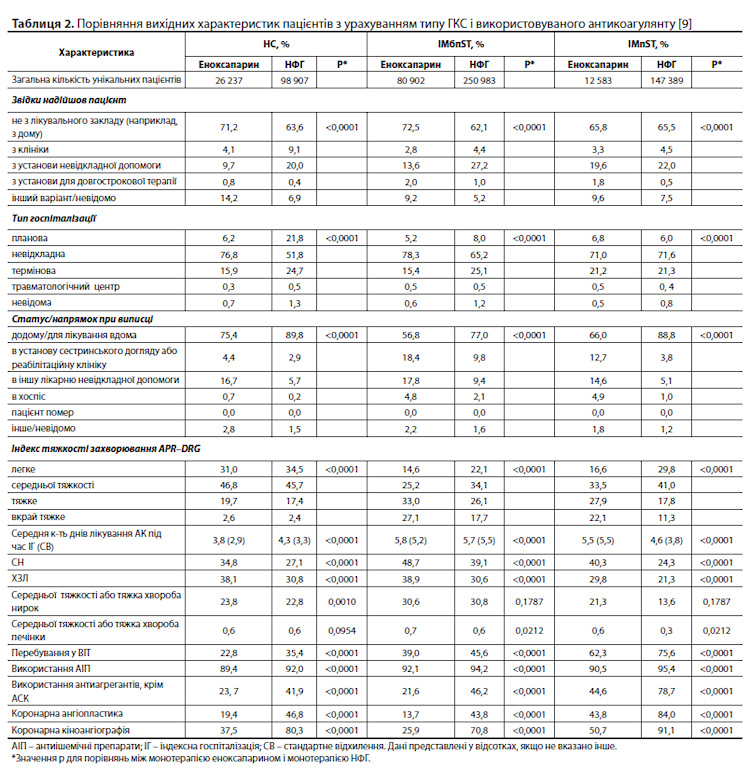
Характеристики пацієнтів залежно від типу антикоагулянту. Вихідні характеристики пацієнтів і лікарень значно різнилися в групах монотерапії еноксапарином і монотерапії НФГ в умовах НС, ІМбпST і ІМпST. У когортах хворих з НС і ІМбпST пацієнти, які отримували еноксапарин, були старші за віком, більшість – жінки, частіше страхувалися за програмою Мedicare в якості основного платника і лікувалися в невеликих, неуніверситетських, сільських лікарнях порівняно з пацієнтами, які отримували НФГ (усі значення р<0,001). У когорті хворих з ІМпST пацієнти, які отримували еноксапарин, рідше були жінками порівняно з пацієнтами на НФГ (57,6 vs 71,6%; р<0,0001). Порівняно з пацієнтами, які отримували НФГ, пацієнти на еноксапарині частіше виписувалися в установу сестринського догляду або реабілітаційну клініку або переводилися в іншу лікарню невідкладної допомоги і при цьому частіше входили до груп тяжкого або вкрай тяжкого стану відповідно до індексу APRDRG; ця закономірність спостерігалася незалежно від типу ГКС. Серед пацієнтів, які отримували еноксапарин, була вищою поширеність серцевої недостатності (СН) та хронічних захворювань легенів (ХЗЛ), але при цьому вони рідше потрапляли у ВІТ, рідше використовували антиішемічні препарати і антиагреганти, крім АСК, рідше проходили коронарну ангіопластику і коронарну кіноангіографію, незалежно від типу ГКС (усі р<0,001) (табл. 2) [9].
Предиктори використання еноксапарину. Після коригування з урахуванням відомих впливових чинників підвищення шансів на лікування еноксапарином у пацієнтів з будь-яким типом ГКС було пов'язане з жіночою статтю, відсутністю страховки, лікуванням у невеликих і сільських лікарнях, наявністю СН або ХЗЛ. Пацієнти з будь-яких регіонів, крім півдня країни, із середньотяжким або тяжким захворюванням нирок, які лікувалися у ВІТ, приймали антиагреганти, крім АСК, які пройшли коронарну ангіопластику і коронарну ангіографію, мали значно менші шанси отримувати лікування еноксапарином за будь-якого варіанту ГКС. Вік, раса, етнічна приналежність, наявність/тип медичного страхування, лікування в університетській клініці, тип госпіталізації, тяжкість стану за індексом APRDRG і використання антиішемічних препаратів чинили різний вплив на використання еноксапарину за різних типів ГКС [9].
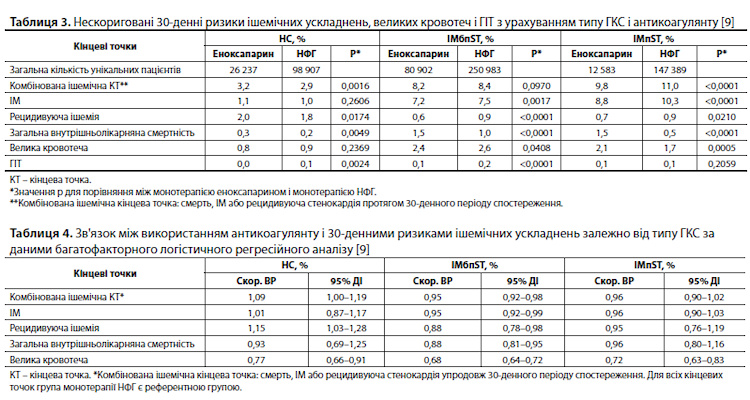
Нескориговані ризики. Нескореговані 30-денні ризики комбінованої ішемічної кінцевої точки, ІМ і рецидивуючої стенокардії були нижчими у пацієнтів, які отримували еноксапарин, у когортах ІМбпST і ІМпST, але не в когорті НС (порівняно з НФГ). Нескорегована 30-денна загальна смертність була вищою, а ризик ГІТ був нижчим у разі використання еноксапарину порівняно з НФГ за всіх типів ГКС. І, нарешті, еноксапарин підвищував ризик великих кровотеч при ІМпST, знижував – при ІМбпST і не змінював показник – при НС порівняно із застосуванням НФГ (табл. 3) [9].
Скориговані ризики. Після коригування на відомі впливові чинники виявили наступне (табл. 4) [9]:
Вартість лікування. Незалежно від типу ГКС, хворі, які отримували еноксапарин, демонстрували вищий нескоригований рівень витрат на використання антикоагулянту (НС – 180 vs 82 дол., ІМбпST – 247 vs 115 дол.; ІМпST – 203 vs 76 дол., усі р<0,0001), але більш низький загальний рівень витрат на медикаменти (НС – 821 vs 1266 дол.; ІМбпST – 1248 vs 1545 дол.; ІМпST – 1503 vs 1801 дол.; усі p<0,0001) і нижчу загальну вартість госпіталізації (НС – 8369 vs 14 750 дол; ІМбпST – 11 889 vs 16 925 дол.; ІМпST – 14 753 vs 17 780 дол.; усі р<0,0001) з приводу ГКС порівняно з пацієнтами на НФГ. Відмінності між антикоагулянтами (еноксапарин vs НФГ) за нескорегованим 30-денним ризиком повторної госпіталізації за всіма причинами варіювалися залежно від типу ГКС (НС – 3,2 vs 2,9%, p=0,0016; ІМбпST – 8,2 vs 8,4%, р=0,097; ІМпST – 9,8 vs 11,0%, р<0,0001). Нескоригована середня тривалість перебування в лікарні за 30-денний період спостереження була трохи більшою у групі еноксапарину, ніж у групі НФГ при всіх трьох типах ГКС (НС – 0,40 vs 0,36 дня, p=0,1790; ІМбпST – 0,71 vs 0,56 дня, р<0,0001; ІМпST – 0,63 vs 0,35 дня, р<0,0001) [9].
Після коригування з урахуванням відомих впливових чинників лікування еноксапарином було пов'язане з більшими середніми витратами на антикоагулянти, але з меншими середніми витратами на медикаменти, меншими загальними витратами на індексну госпіталізацію, а також меншими загальними витратами на госпіталізації протягом 30-денного періоду спостереження порівняно з НФГ, незалежно від типу ГКС. Скоригований ризик 30-денної повторної госпіталізації з усіх причин був нижчим у групі еноксапарину у пацієнтів з ІМпST і ІМбпST, але вищим у пацієнтів з НС, порівняно із застосуванням НФГ. У цілому, за період, що охоплює індексну госпіталізацію і 30 днів після виписки зі стаціонару, загальна економія в групі еноксапарину порівняно з НФГ становила 2972 дол. для пацієнта з НС, 2475 дол. – для пацієнта з ІМбпST і 3050 дол. – для пацієнта з ІМпST [9].
Обговорення і висновки Аналіз реальних даних більш ніж 1 млн пацієнтів з 859 американських лікарень показав, що в когорті пацієнтів з ІМбпST монотерапія еноксапарином асоціюється зі значним зниженням 30-денного ризику комбінованої ішемічної кінцевої точки, нефатального ІМ, рецидивуючої стенокардії, загальної внутрішньолікарняної смертності, а також ризику великих кровотеч порівняно з НФГ, що узгоджується з результатами більшості опублікованих клінічних досліджень і метааналізів [4, 10–14]. При цьому в когорті пацієнтів з НС захисний ефект еноксапарину не був настільки виражений, за винятком зниження ризику великих кровотеч. Водночас, при об'єднанні когорт НС і ІМбпST захисні ефекти еноксапарину були аналогічні тим, що спостерігалися в клінічних дослідженнях, які разом вивчали обидва ці типи ГКС. Аналіз даних пацієнтів з ІМпST показав зіставні рівні 30-денних ризиків ішемічних ускладнень і внутрішньолікарняної смертності у разі використання обох антикоагулянтів, але на 28% менший ризик великої кровотечі у групі еноксапарину порівняно з НФГ. Ці результати дещо відрізняються від результатів клінічних досліджень за участю пацієнтів з гострим ІМ, які пройшли первинне ЧКВ і отримували внутрішньовенно еноксапарин або НФГ, які показали більш низький ризик смерті й ІМ у групі еноксапарину [12, 14]. Такі відмінності можуть бути пов'язані з тим, що пацієнти, які увійшли в аналіз Rosenthal et al., були старшими за віком, мали більше супутніх захворювань і більш тяжкий перебіг основної патології порівняно з учасниками клінічних досліджень, які пройшли ретельний відбір. Результати аналізу Rosenthal et al. також показали, що незважаючи на більш високу вартість еноксапарину порівняно з НФГ, середні витрати на медикаменти, загальна вартість індексної госпіталізації, а також загальна вартість госпіталізацій за 30-денний період спостереження були нижчими у разі використання еноксапарину порівняно з НФГ. Як результат, застосування еноксапарину було пов'язане зі значною загальною економією коштів за весь період спостереження (індексна госпіталізація + 30 днів подальшого спостереження), яка варіювалася в діапазоні від 2475 до 3050 дол. на пацієнта залежно від типу ГКС. Ці результати узгоджуються з даними дослідження ESSENCE [13], що проводилося за участю пацієнтів з НС і ІМбпSТ у 1998 р. (30-денна сукупна економія при використанні еноксапарину порівняно з НФГ – 1172 дол. на пацієнта), і, з огляду на велику щорічну кількість госпіталізацій з приводу ГКС, указують на можливість значної сукупної економії коштів за рахунок більш активного використання еноксапарину. Крім інших результатів, аналіз Rosenthal et al. показав, що, незважаючи на доведену в цьому аналізі і попередніх клінічних дослідженнях ефективність у профілактиці ішемічних ускладнень і смерті серед пацієнтів з ГКС, а також значну економію коштів, еноксапарин використовується значно рідше, ніж НФГ при всіх формах ГКС [5, 10–1 5]. За даними цього аналізу, 5,1–13,9% пацієнтів з ГКС отримували еноксапарин порівняно з 43,1–59,8%, що отримували НФГ. Виявлений Rosenthal et al. факт більш частого використання еноксапарину в невеликих і сільських лікарнях, швидше за все пов'язаний з більш простим і зручним способом уведення препарату і відсутністю потреби в моніторингу антикоагулянтного ефекту еноксапарину. Виявлені відмінності у використанні цих двох основних парентеральних антикоагулянтів у пацієнтів з ГКС вимагають ретельної оцінки механізму прийняття рішення у разі вибору того чи іншого антикоагулянту в реальній клінічній практиці. До переваг аналізу Rosenthal et al. відноситься оцінка моделей використання двох різних антикоагулянтів і порівняння їх ефективності в профілактиці ішемічних подій з використанням великого обсягу реальних даних, отриманих з лікарень різного розміру і географічного положення. Досліджувана вибірка пацієнтів з ГКС більш репрезентативна, ніж вибірки з більш ранніх аналізів, які використовували результати клінічних досліджень або дані окремих медичних центрів. Другою важливою перевагою цього аналізу є можливість оцінки важливих чинників, що мають вплив, при вивченні відмінностей між антикоагулянтами з ефективності і вартості терапії, що стало можливим завдяки великому обсягу і надійності даних, зібраних у базі PHD [9]. У свою чергу, аналіз Rosenthal et al. має обмеження, властиві всім ретроспективним аналізам лікарняних баз даних, наприклад неможливість враховувати вплив прихильності лікаря і клінічної картини при надходженні хворого на вибір конкретного антикоагулянту (ці дані неможливо зареєструвати в базі адміністративних даних), а також неможливість обліку випадків переходу одного варіанта ГКС в інший (від ІМбпST до ІМпST, або від НС до ІМбпST), що може привести до зміни спочатку призначеного лікування [9].
Висновок Як показав аналіз великої бази даних американських пацієнтів з ГКС за 2010–2018 рр., терапія еноксапарином (порівняно з НФГ) асоціюється зі значним зниженням 30-денного ризику ішемічних ускладнень і смерті у пацієнтів з ІМбпST, і зі зниженням ризику великих кровотеч, незалежно від типу ГКС. Також при будь-якому варіанті ГКС застосування еноксапарину було пов'язане зі значною економією коштів за період, що охоплює індексну госпіталізацію і 30 днів після виписки зі стаціонару, порівняно з НФГ. Крім того, було виявлено суттєве недовикористання еноксапарину в клінічних ситуаціях, пов'язаних з лікуванням ГКС, що вимагає ретельного вивчення діючого підходу до призначення еноксапарину і пошуку шляхів подальшої оптимізації вибору антикоагулянтів для пацієнтів з ГКС з метою домогтися максимально сприятливих клінічних результатів з використанням найбільш економічно ефективних стратегій. Література 1. Braunwald E. Unstable angina and nonST elevation myocardial infarction. Am J Respir Crit Care Med. 2012; 185(9): 924–32. 2. Kolansky D. Acute coronary syndromes: morbidity, mortality, and pharmacoeconomic burden. Am J Manag Care. 2009; 15(2Suppl): S36–41. 3. Benjamin E., Virani S., Callaway C. et al. Heart Disease and Stroke Statistics2018 Update: A Report From the American Heart Association. Circulation. 2018; 137(12): e67–492. 4. Cohen M., Demers C., Gurfinkel E. et al. A comparison of lowmolecularweight heparin with unfractionated heparin for unstable coronary artery disease. Efficacy and Safety of Subcutaneous Enoxaparin in NonQWave Coronary Events Study Group. N Engl J Med. 1997; 337(7): 447–52. 5. Ferguson J., Califf R., Antman E. et al. Enoxaparin vs unfractionated heparin in highrisk patients with nonSTsegment elevation acute coronary syndromes managed with an intended early invasive strategy: primary results of the SYNERGY randomized trial. JAMA. 2004; 292(1): 45–54. 6. Michalis L., Katsouras C., Papamichael N. et al. Enoxaparin versus tinzaparin in nonSTsegment elevation acute coronary syndromes: the EVET trial. Am Heart J. 2003; 146(2): 304–10. 7. Merli G., Groce J. Pharmacological and clinical differences between lowmolecularweight heparins: implications for prescribing practice and therapeutic interchange. P & T. 2010; 35(2): 95–105. 8. Yancy C., Jessup M., Bozkurt B. et al. 2013 ACCF/AHA guideline for the management of heart failure: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol. 2013; 62(16): e147–239. 9. Rosenthal N., Xiao Z., Kartashov A. et al. Comparative Effectiveness and Costs of Enoxaparin Monotherapy Versus Unfractionated Heparin Monotherapy in Treating Acute Coronary Syndrome. Am J Cardiovasc Drugs. 2020 Jun 23. doi: 10.1007/s40256020004199. Online ahead of print. 10. Cohen M., Demers C., Gurfinkel E. et al. Lowmolecularweightheparins in nonSTsegment elevation ischemia: the ESSENCE trial. Efficacy and Safety of Subcutaneous Enoxaparin versus intravenous unfractionated heparin, in nonQwave Coronary Events. AM J Cardiol. 1998; 82(5b): 19l–24l. 11. Cohen M., Theroux P., Borzak S. et al. Randomized doubleblind safety study of enoxaparin versus unfractionated heparin in patients with nonSTsegment elevation acute coronary syndromes treated with tirofiban and aspirin: the ACUTE II study. The Antithrombotic Combination Using Tirofiban and Enoxaparin. Am Heart J. 2002; 144(3): 470–7. 12. Collet J., Huber K., Cohen M. et al. A direct comparison of intravenous enoxaparin with unfractionated heparin in primary percutaneous coronary intervention (from the ATOLL trial). An J Cardiol. 2013; 112(9): 1367–72. 13. Mark D., Cowper P., Berkowitz S. et al. Economic assessment of lowmolecularweight heparin (enoxaparin) versus unfractionated heparin in acute coronary syndrome patients: results from the ESSENCE randomized trial. Efficacy and Safety of Subcutaneous Enoxaparin in NonQ wave Coronary Events [unstable angina or nonQwave myocardial infarction]. Circulation. 1998; 97(17): 1702–7. 14. Silvain J., Beygui F., Barthelemy O. et al. Efficacy and safety of enoxaparin versus unfractionated heparin during percutaneous coronary intervention: systematic review and metaanalysis. BMJ (Clin Res Ed). 2012; 344: e553. 15. Fanari Z., Weiss S., Weintraub W. Cost effectiveness of antiplatelet and anti-thrombotic therapy in the setting of acute coronary syndrome: current perspective and literature review. Am J Cardiovasc Drugs. 2015; 15(6): 415–27. Автор огляду Наталія Генш  Medicine Review 2020; 3 (58): 28 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2025. Усі права захищені.
|
мапа сайту корисні посилання |