Ефективність і безпечність еплеренону в пацієнтів з гострою серцевою недостатністю: огляд результатів дослідження EARLIERЗа останні десятиліття в кардіологічній практиці розвинених країн і країн, що розвиваються, відмічається неухильне зростання частки пацієнтів із серцевою недостатністю (СН), як гострою (ГСН), так і хронічною (ХСН), що пов’язано з дією різних соціальних і біологічних чинників, зокрема з прогресуючим старінням суспільства й поліпшенням результатів лікування серцево-судинних (СС) захворювань (ССЗ), насамперед гострого інфаркту міокарда (ГІМ) [1]. Така зміна структури кардіологічної захворюваності змушує вчених і лікарів приділяти дедалі більшу увагу методам лікування СН як симптоматичним, так і таким, що поліпшують прогноз, у цієї категорії пацієнтів. У терапії ХСН зміщення фокусу із симптоматичного лікування на захист внутрішніх органів, і перш за все на кардіопротекцію, вже принесло позитивні результати у вигляді зниження захворюваності й смертності, тоді як у гострій фазі декомпенсованої СН основні зусилля, як і раніше, спрямовано на усунення гемодинамічних порушень за допомогою діуретиків, вазодилататорів та інотропних препаратів без явного прагнення забезпечити кардіопротекцію [2, 3]. Такому зміщенню акцентів (із симптомів на прогноз) під час терапії ГСН значною мірою перешкоджає відсутність достатніх науково-обґрунтованих даних на підтримку застосування того чи іншого кардіопротекторного препарату за умов декомпенсованої СН, однак попередні дані привертають увагу до деяких лікарських засобів, що вже використовують при ХСН, зокрема до антагоністів мінералокортикоїдних рецепторів (АМР). Як відомо, в умовах ГСН альдостерон через свої рецептори в серці, мозку й кровоносних судинах чинить виражений несприятливий вплив на СС систему [4, 5], при цьому в гострій фазі СН відмічають значне підвищення рівня альдостерону в плазмі крові, яке пов’язане з прогресуючим ушкодженням міокарда й погіршенням прогнозу [6-10], що робить альдостерон потенційною терапевтичною мішенню при ГСН. З огляду на те що результати кількох клінічних досліджень продемонстрували сприятливий вплив АМР еплеренону на прогноз у пацієнтів із ХСН (СН зі зниженою фракцією викиду [ФВ] лівого шлуночка [ЛШ]) [11], було висунуто припущення, згідно з яким пригнічення надлишкових сигналів альдостерону під час гострої фази СН може стати успішною стратегією лікування ГСН, яка забезпечуватиме захист серця, судин та інших органів і покращуватиме прогноз. Для перевірки цієї гіпотези було проведене дослідження EARLIER з оцінки безпечності раннього початку терапії еплереноном та її прогностичної значущості для пацієнтів, госпіталізованих з приводу ГСН. Нижче наведено стислий опис дослідження EARLIER і його основні результати [12].
Методологія дослідження EARLIER Метою багатоцентрового рандомізованого подвійного сліпого плацебо-контрольованого дослідження EARLIER була порівняльна оцінка впливу раннього початку терапії еплереноном на події комбінованої кінцевої точки (СС смерть або перша повторна госпіталізація з приводу ССЗ) у пацієнтів з ГСН. У дослідження зараховували хворих віком ≥20 років із клінічними ознаками ГСН у вигляді вперше розвиненої (de novo) ГСН, гострої декомпенсації ХСН або постінфарктної (після ГІМ) СН із ФВ ЛШ ≤40%. На наявність ГСН вказувала присутність одного з таких симптомів: легеневі хрипи, застійні явища в легенях за даними рентгенографії органів грудної клітини або третій серцевий тон під час аускультації серця. До участі в дослідженні не допускали пацієнтів, які раніше отримували АМР, осіб, які пройшли планове черезшкірне коронарне втручання (ЧКВ) або аортокоронарне шунтування (АКШ) під час першої госпіталізації, також критеріями виключення були рівень калію в сироватці крові >5,0 ммоль/л, розрахункова швидкість клубочкової фільтрації (рШКФ) <30 мл/хв/1,73 м2 і клінічно значущі супутні захворювання [12]. Спочатку рандомізацію учасників проводили протягом 72 год після госпіталізації з приводу ГСН, але згодом (після зарахування перших 180 пацієнтів) цей період було збільшено до 14 днів. Пацієнтів рандомізували у співвідношенні 1:1 для отримання еплеренону або плацебо. Початкова доза еплеренону/плацебо становила 25 мг один раз на добу, через тиждень терапії доза збільшувалася до 50 мг 1 раз на добу (пацієнти з рШКФ від 30 до <50 мл/хв/1,73 м2 розпочинали лікування з дози 25 мг через день, а згодом збільшували дозу до 25 мг на добу) за умови, що рівень калію в сироватці крові був ≤5,0 ммоль/л. На кожному візиті в дослідницький центр проводили оцінку рШКФ і рівня калію, за результатами якої дослідники змінювали дозу або призупиняли приймання препарату. Протягом 72 год після зміни дози/призупинення приймання препарату проводили повторні оцінки рівня калію й рСКФ, після чого, якщо рівень калію був нижчим за 5,0 ммоль/л, пацієнта повертали до попередньої схеми лікування (дозу знову збільшували, або пацієнт поновлював використання досліджуваного препарату). Обстеження пацієнтів проводили через 48 год, 1 тиждень, 2 тижні лікування, під час виписки зі стаціонару (або через 4 тижні лікування), а потім через 8, 12, 16, 20 і 24 тижні терапії. Під час кожного візиту реєстрували й оцінювали всі небажані явища (НЯ) [12]. Первинною кінцевою точкою дослідження була комбінація СС смерті (у тому числі смерті внаслідок декомпенсації СН, ГІМ, аритмії, інсульту або інших причин, пов’язаних із ССЗ, та раптової смерті) і першої повторної госпіталізації з приводу будь-якого ССЗ (зокрема декомпенсації СН, ГІМ, інсульту, аритмії та іншого ССЗ) упродовж 6 місяців після включення в дослідження. Запланованими вторинними кінцевими точками були комбінація СС смерті й першої повторної госпіталізації з приводу СН, комбінація СС смерті й несмертельного ГІМ, перша повторна госпіталізація з приводу будь-якого ССЗ, смерть від будь-якого ССЗ, перша повторна госпіталізація з приводу СН, смерть з будь-якої причини, несмертельний ГІМ, раптова серцева смерть і проведення апаратної терапії СН, у тому числі серцевої ресинхронізуючої терапії або терапії із застосуванням пристрою підтримки шлуночків. Кінцевою точкою оцінки безпеки була частота НЯ (без урахування причинного зв'язку НЯ з досліджуваним препаратом). Також оцінювали прихильність пацієнтів до дотримання призначеної схеми лікування: осіб із рівнем приймання призначеної дози 80–120% за даними двох візитів вважали прихильними до лікування [12]. Запланований об’єм вибірки становив 300 пацієнтів. Статистичні аналізи для оцінки ефективності проводили відповідно до принципу intention to treat (ITT, з урахуванням лікування, призначеного під час рандомізації), для аналізів безпеки використовували дані всіх пацієнтів, які отримали щонайменше одну дозу досліджуваного препарату. Під час аналізів розраховували час до розвитку подій первинної та вторинних кінцевих точок, відношення ризиків (ВР) і відповідні 95% довірчі інтервали (ДІ) [12].
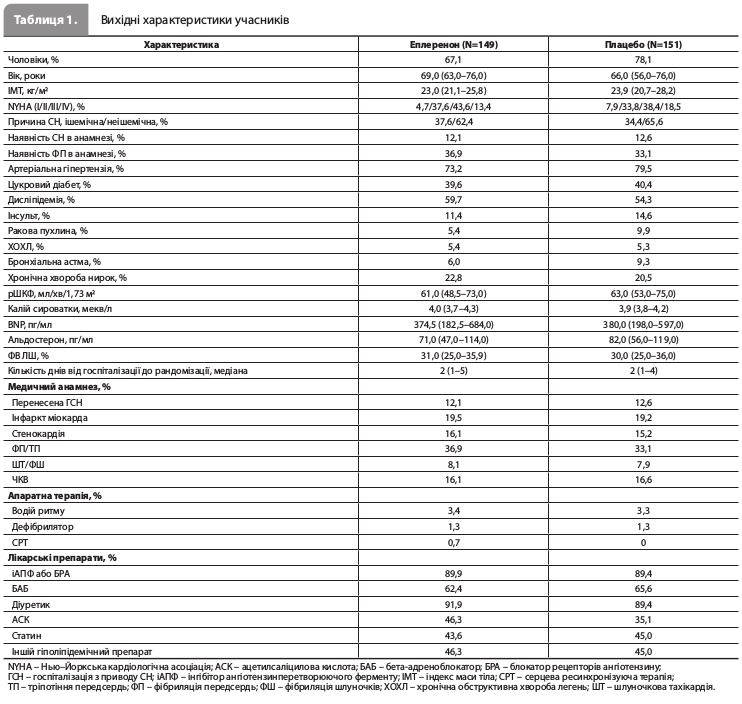
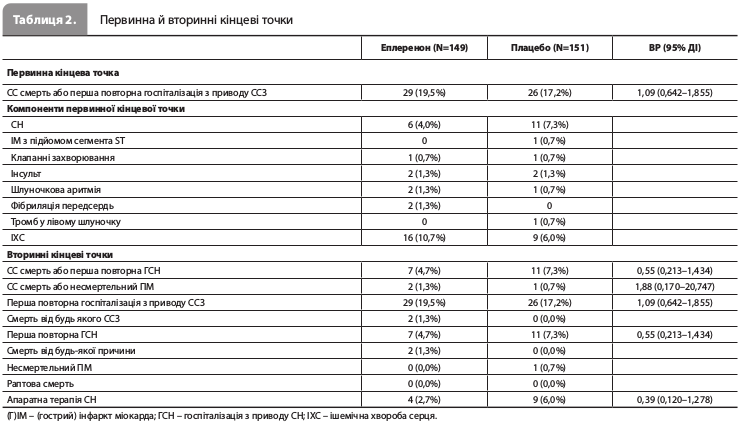
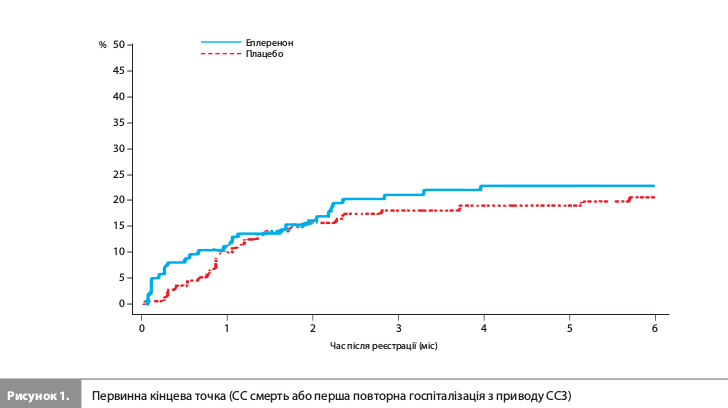
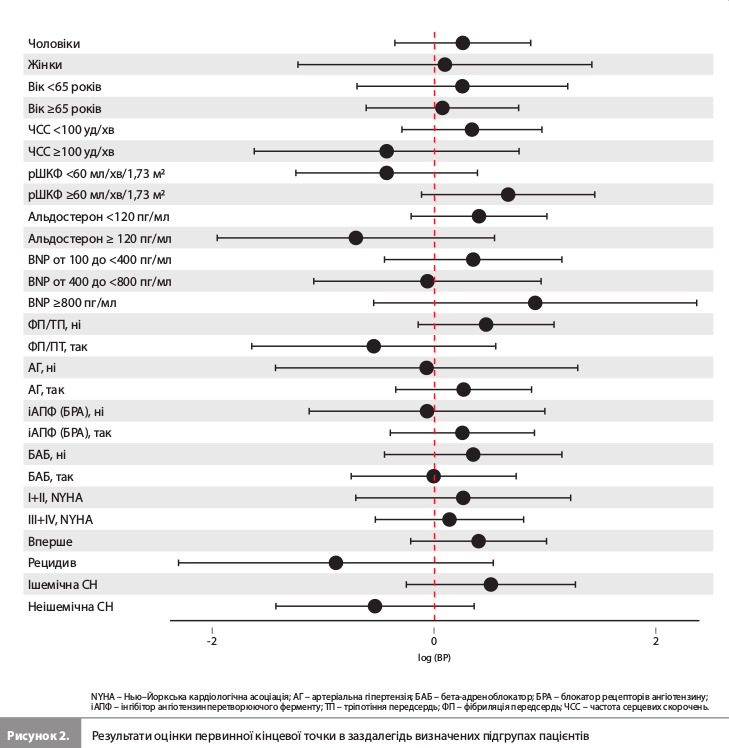
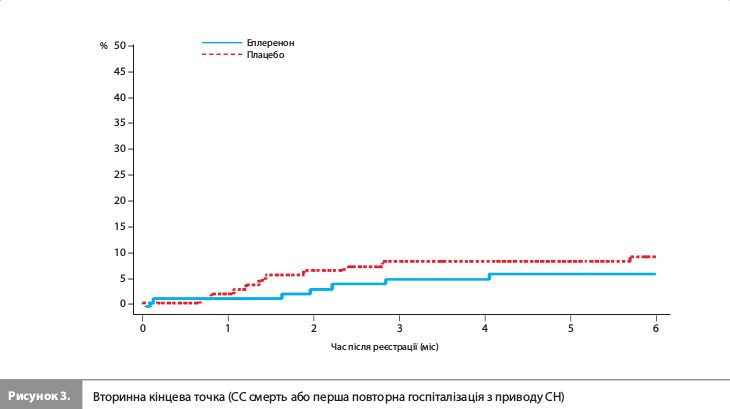
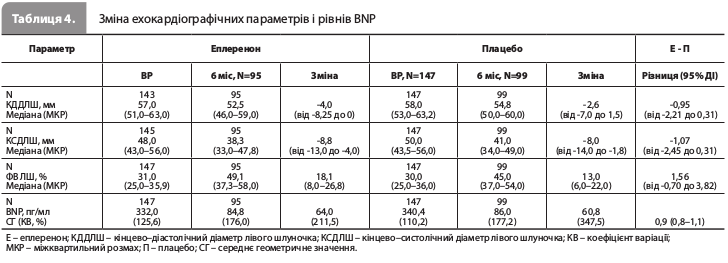
Результати дослідження EARLIER За період дослідження (з червня 2013 року по квітень 2018 року) було рандомізовано загалом 300 пацієнтів із 27 великих медичних центрів Японії: 149 – у групу еплеренону й 151 – у групу плацебо. Щонайменше одну дозу досліджуваного препарату отримали 148 і 149 пацієнтів у групах еплеренону й плацебо відповідно. Групи лікування були зіставними за такими вихідними характеристиками, як вік, медіана ФВ ЛШ, медіанний рівень мозкового натрійуретичного пептиду (BNP) і частки пацієнтів з різними значеннями рШКФ. Середня тривалість лікування досліджуваним препаратом становила 142,5 і 147,9 дня в групах еплеренону й плацебо відповідно. Кількість пацієнтів, що дотримувалися призначень лікаря, становила 143 (95,9%) і 148 (98,0%) у групах еплеренону й плацебо відповідно (табл. 1) [12]. Групи лікування не продемонстрували достовірних відмінностей за частотою реєстрації первинної комбінованої кінцевої точки (СС смерть або перша повторна госпіталізація внаслідок ССЗ протягом 6 місяців): 19,5 vs 17,2% у групах еплеренону й плацебо відповідно (ВР 1,09, 95% ДІ 0,64–1,86) (табл. 2 і рис. 1). Ефект еплеренону на первинну кінцеву точку був загалом узгодженим у всіх заздалегідь визначених підгрупах пацієнтів (рис. 2). Частота вторинної комбінованої кінцевої точки, що включала СС смерть або першу повторну ГСН упродовж 6 місяців, становила 4,7 vs 7,3% у групах еплеренону й плацебо відповідно (ВР 0,55, 95% ДІ 0,21–1,43) (рис. 3). Частота виникнення показань до проведення апаратної терапії СН становила 2,7 vs 6,0% (ВР 0,39, 95% ДІ 0,12–1,28), частота СС смерті – 1,3 і 0%, частота шлуночкової аритмії – 1,3 vs 0,7% відповідно [12]. За даними аналізу безпеки загальна частота НЯ становила 79,1 і 79,2%, частота небажаних лікарських реакцій – 24,3 і 18,8% (табл. 3), а частота серйозних НЯ – 23,0 і 20,8% у групах еплеренону й плацебо відповідно. Значущі міжгрупові відмінності за цими показниками були відсутні. Частота гіперкаліємії та гіпокаліємії становила 4,1 і 2,7% у групі еплеренону й 2,0% і 4,7% у групі плацебо. У групі еплеренону померли два пацієнти; обидві смерті були розцінені як не пов’язані з прийманням препарату. У групі плацебо не помер жоден пацієнт [12]. Оцінка ефектів терапії на ехокардіографічні параметри й рівень BNP у плазмі крові через 6 місяців показала зниження рівня BNP на 64,0 і 60,8 пг/мл, зменшення діастолічних розмірів ЛШ на 4,0 й 2,6%, а також збільшення ФВ ЛШ на 18,1 та 13,0% у групах еплеренону й плацебо відповідно (табл. 4) [12].

Обговорення результатів дослідження EARLIER Отже, результати дослідження EARLIER показали, що еплеренон не знижує 6-місячний ризик первинної кінцевої точки у вигляді комбінації СС смерті й першої повторної госпіталізації внаслідок ССЗ у пацієнтів із ГСН. Цей результат не узгоджується з висновком, зробленим у дослідженні EPHESUS, яке показало, що застосування еплеренону в пацієнтів із систолічною дисфункцією ЛШ і СН після ГІМ на 15% знижує відносний ризик смерті від усіх причин і на 13% – відносний ризик СС смерті/СС ускладнень порівняно з пацієнтами, які отримують стандартну терапію. На думку авторів дослідження EARLIER, цю розбіжність можна пояснити двома обставинами: по-перше, невеликою досліджуваною вибіркою, а по-друге, включенням до первинного результату EARLIER госпіталізацій у зв'язку з проведенням коронарних втручань (ЧКВ і АКШ). Таких госпіталізацій, за даними 6-місячного спостереження, виявилося більше в групі еплеренону, ніж у групі плацебо (16 vs 9 випадків), і хоча ця різниця була випадковою (оскільки еплеренон не спричиняє прогресування ішемічної хвороби серця), вона могла вплинути на загальний результат оцінки первинної кінцевої точки цього дослідження [12]. У зв’язку з цим на інтерес заслуговує результат, отриманий під час оцінки однієї з вторинних кінцевих точок дослідження, а саме комбінації смерті від СС причин і госпіталізації з приводу СН, ризик якої в групі еплеренону знизився на 45% (ВР 0,55). Слід зазначити, що ця вторинна кінцева точка відповідає первинній кінцевій точці дослідження EMPHASIS–HF, яке завершилося й було опубліковано після початку дослідження EARLIER, а тому не вплинуло на дизайн цього дослідження. Як наслідок, запланований об’єм досліджуваної вибірки в EARLIER був недостатнім для оцінки статистичної значущості міжгрупової різниці за цією вторинною кінцевою точкою. Серед результатів дослідження EARLIER слід відзначити зниження рівнів біомаркера важкості СН (BNP) у плазмі крові, зменшення систолічного/діастолічного розмірів ЛШ і збільшення ФВ ЛШ через 6 місяців після раннього початку лікування еплереноном порівняно з групою плацебо. Крім того, важливими результатами дослідження стали сприятливий профіль безпеки, продемонстрований еплереноном, у японських пацієнтів з ГСН, а також відсутність значущих відмінностей за прихильністю пацієнтів до лікування між групами плацебо й еплеренону [12]. Під час інтерпретації отриманих результатів слід враховувати низку обмежень дослідження EARLIER, а саме невеликий розмір вибірки й той факт, що всі учасники дослідження були японцями (хоча, за сучасними уявленнями, етнічна приналежність не впливає на патофізіологію й перебіг ГСН) [12].
Висновки Загалом попри те що через невеликий об'єм вибірки учасників дослідження EARLIER не вдалося достовірно довести прогностичні переваги ранньої терапії еплереноном у пацієнтів із ГСН, його результати, а саме зниження частоти подій вторинної кінцевої точки – комбінації смерті від СС причин і госпіталізації з приводу СН – у групі еплеренону все ж таки свідчать про наявність потенційних переваг у подібної терапії та доцільність проведення додаткових досліджень. Подальшу оцінку цієї стратегії підтримує зіставна частота небажаних явищ у групах еплеренону й плацебо, а також ідентичність профілю побічних ефектів еплеренону (включно з гіперглікемією) його профілям безпеки в інших дослідженнях при СН.
Список літератури знаходиться в редакції
Автор огляду Олена Грибова Джерело: |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2025. Усі права захищені.
|
мапа сайту корисні посилання |