Довгострокові ефекти емпагліфлозину на прогресування хронічної хвороби нирок: підсумкові результати дослідження EMPA-KIDNEYОчевидний зв'язок термінальної стадії хронічної хвороби нирок (ХХН), за якої виникають показання до хронічного діалізу / трансплантації нирки, з істотним зниженням якості життя, зростанням серцево-судинної (СС) захворюваності / смертності, а також високими економічними витратами [1, 2] робить профілактику прогресування ХХН клінічно й соціально значущим напрямом сучасної медицини. Одним з останніх клінічних досліджень на цю тему був проєкт EMPA-KIDNEY (The Study of Heart and Kidney Protection With Empagliflozin), присвячений оцінці ефективності й безпечності інгібітора натрійзалежного котранспортера глюкози 2 типу (іНЗКТГ2) емпагліфлозину в широкого кола хворих із ХХН і ризиком її прогресування. Результати активної фази цього дослідження показали, що емпагліфлозин значно знизив ризик прогресування ХХН і СС смерті порівняно з плацебо, що узгоджується з результатами інших досліджень іНЗКТГ2 [3–6]. Проте активна фаза дослідження EMPA-KIDNEY була порівняно короткою – медіана періоду оцінки ефективності становила 2 роки, у зв'язку із чим кількість подій первинної кінцевої точки (комбінація «прогресування ХХН / СС смерть») серед учасників із повільним прогресуванням ХХН була невеликою [3]. Це підвищило актуальність періоду подальшого спостереження (ПС) за пацієнтами після припинення дослідження EMPA-KIDNEY та лікування досліджуваним препаратом (емпагліфлозином або плацебо). Нещодавно дослідницька група EMPA-KIDNEY (Herrington et al.) представила звіт про підсумкові результати дослідження, об’єднавши дані, отримані під час активної фази й 2-річного ПС. Основна інформація із цього звіту стисло викладена в огляді [7].

Методологія дослідження Herrington et al. EMPA-KIDNEY проводилося в 2019–2024 рр. як подвійне сліпе плацебо-контрольоване багатоцентрове рандомізоване клінічне дослідження (РКД). Період ПС був організований як необов’язкове додаткове дослідження за участі 185 з 241 дослідницького центру (77%), що взяв участь в основному РКД. Учасниками EMPA-KIDNEY були дорослі пацієнти з ХХН і розрахунковою швидкістю клубочкової фільтрації (рШКФ) від ≥20 до <45 мл/хв/1,73 м2 незалежно від рівня альбумінурії або з рШКФ від ≥40 до <90 мл/хв/1,73 м2 при співвідношенні альбумін/креатинін у сечі (САК) ≥200 мг/г на момент відбору в активну фазу дослідження. Усі учасники за відсутності протипоказань або непереносимості повинні були приймати клінічно адекватну дозу інгібітора ренін-ангіотензинової системи (іРАС). Під час рандомізації учасників розподілили для отримання емпагліфлозину в дозі 10 мг/добу або відповідного плацебо. Після закінчення активної фази дослідники вилучили в учасників усі запаси досліджуваного препарату (емпагліфлозину або плацебо) і повідомили місцевим лікарям результати дослідження. Протягом усього ПС дослідники й учасники були не обізнані щодо того, який саме препарат отримував учасник в активній фазі дослідження. Під час періоду ПС місцеві лікарі могли вільно призначати доступні іНЗКТГ2 (зокрема емпагліфлозин) колишнім учасникам EMPA-KIDNEY за наявності показань і несли відповідальність за організацію стандартного моніторингу функції нирок відповідно до місцевої клінічної практики. Метою ПС був збір додаткових даних про ефективність емпагліфлозину й причини смерті колишніх учасників EMPA-KIDNEY. Основним методом спостереження був аналіз медичних карт і даних із реєстрів у Великій Британії та Малайзії. За відсутності медичних карт інформацію збирали шляхом контакту з пацієнтами, їхніми родичами, опікунами або місцевими лікарями. Інформацію збирали раз на 6 місяців з акцентом на детальних відомостях про виживаність пацієнта, статус замісної ниркової терапії, результати останніх вимірювань рівня креатиніну в крові й поточне застосування іНЗКТГ2, іРАС та антагоністів мінералокортикоїдних рецепторів [7]. Первинним результатом, який оцінювали Herrington et al., був вплив терапії емпагліфлозином в активній фазі дослідження на час до розвитку подій із комбінації «прогресування ХХН / СС смерть» за весь період дослідження (активна фаза EMPA-KIDNEY + ПС). Під прогресуванням ХХН розуміли стійке зниження рШКФ не менш ніж на 40% порівняно з показником на момент рандомізації, розвиток термінальної стадії ХХН, стійку рШКФ <10 мл/хв/1,73 м2 або смерть від ниркової недостатності [3]. Для підтвердження стійкості значення рШКФ була необхідна наявність зіставних результатів двох вимірювань, проведених з інтервалом не менше 30 днів. Зміна показника оцінювалася відносно значення рШКФ, отриманого на вихідному рівні активної фази дослідження. Також за результатами ПС оцінювали низку ключових вторинних точок, у тому числі прогресування ХХН, розвиток термінальної стадії ХХН і комбінацію «термінальна стадія ХХН / смерть від будь-якої причини». Третичними кінцевими точками були смерть від будь-якої причини, смерть від СС причин і смерть від неСС причин, яка також була кінцевою точкою безпеки періоду ПС. Крім того, проводили аналіз первинної кінцевої точки в підгрупах пацієнтів, виділених з урахуванням статусу цукрового діабету (ЦД), величини рШКФ, САК і захворювання, що призвело до розвитку ХХН [7]. Для статистичної обробки даних і розрахунку відношення ризиків (ВР; емпагліфлозин vs плацебо) і 95% довірчих інтервалів (ДІ) дослідники провели аналіз часу до настання подій із використанням моделей регресії пропорційних ризиків Кокса, скоригованих з урахуванням віку, статі, статусу ЦД, величини рШКФ, САК і географічного регіону. Дані учасників, які вижили і не перейшли в період ПС (через небажання або тому, що їхній дослідницький центр не брав участі в ПС), цензурували після закінчення активної фази дослідження. Статистики побудували криві Каплана-Майера для первинної та кожної вторинної кінцевих точок і розрахували показник абсолютної користі від терапії емпагліфлозином на 1000 пацієнтів. За допомогою коваріаційного аналізу також розрахували абсолютну міжгрупову різницю середніх значень рШКФ, отриманих при останньому вимірюванні, скориговану на вихідне значення показника [7].
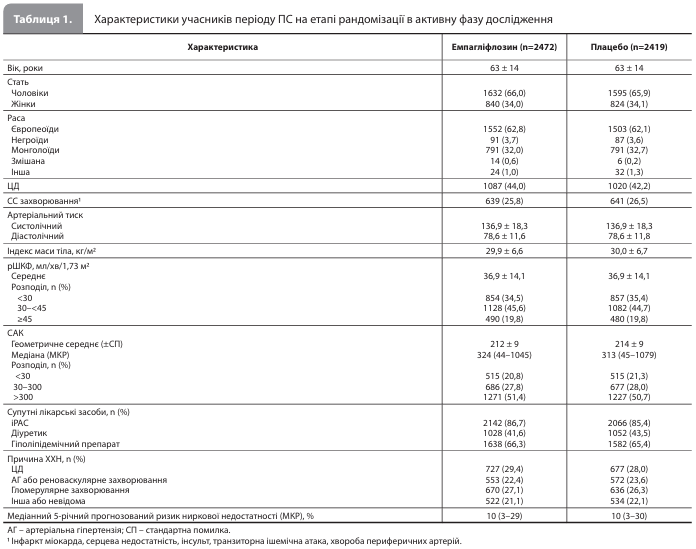
Результати дослідження Herrington et al. Із травня 2019 по квітень 2021 року загалом 6609 пацієнтів пройшли рандомізацію та розпочали участь в активній фазі дослідження, яка тривала в середньому 2,0 роки (міжквартильний розмах [МКР] 1,5–2,4). Із 6253 пацієнтів, які завершили участь в активній фазі, у період ПС перейшов 4891 пацієнт. Медіана ПС за цими пацієнтами становила 2,0 роки (МКР 2,0–2,1). До кінця ПС дані про виживаність були відсутні у 86 пацієнтів (1,8%), ще 7 (0,1%) відкликали згоду на участь під час ПС. У цілому, вибірка учасників ПС була репрезентативною для популяції хворих із ХХН і ризиком її прогресування, а отримані при рандомізації групи емпагліфлозину й плацебо були зіставними за вихідними характеристиками (табл. 1) [7]. Середній (± стандартне відхилення [СВ]) вік пацієнтів при рандомізації становив 63 ± 14 років, 1664 (34,0%) учасники були жінками, у 2784 (56,9%) не було ЦД, і у 3487 (71,3%) була недіабетична ХХН. Середня рШКФ становила 36,9 ± 14,1 мл/хв/1,73 м2, медіана САК – 317 мг/г (МКР 44–1063), при цьому у 2393 пацієнтів (48,9%) показник був ≤300 мг/г [7]. Учасники ПС рідше були монголоїдами, були трохи молодшими, мали трохи менші рШКФ і САК і дещо вищий ризик ниркової недостатності ніж пацієнти, які не брали участі в ПС. Частка пацієнтів, які приймали емпагліфлозин в активній фазі (досліджуваний препарат) / будь-який доступний іНЗКТГ2 в періоді ПС, становила 90%/43% серед пацієнтів із групи емпагліфлозину і 2%/40% – серед пацієнтів із групи плацебо відповідно [7]. Пацієнти, які не почали приймання доступного іНЗКТГ2 під час ПС, частіше були монголоїдами, рідше мали раніше діагностований ЦД, мали нижчу рШКФ, відрізнялися значно вищим ризиком ХХН і рідше приймали іРАС. У період ПС відзначалося зниження середнього рівня використання іРАС, проте цей показник залишався однаковим у групах емпагліфлозину й плацебо (68%) [7].
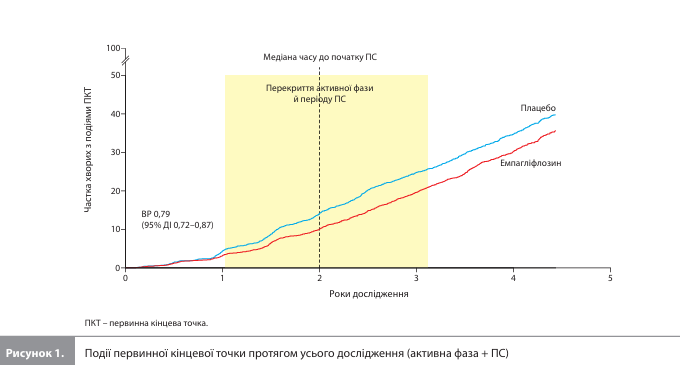
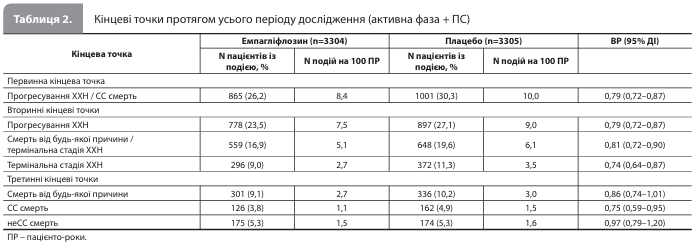
Протягом активної фази й ПС сукупно події первинної кінцевої точки (прогресування ХХН або СС смерть) були зареєстровані у 26,2% пацієнтів у групі емпагліфлозину й у 30,3% – у групі плацебо (ВР 0,79; 95% ДІ 0,72–0,87) (рис. 1, табл. 2) [7]. Значення ВР для активної фази й ПС становили 0,72 (95% ДІ 0,64–0,82; 990 подій) і 0,87 (95% ДІ 0,76–0,99; 876 подій) відповідно. У періоді ПС більша частина користі емпагліфлозину у вигляді зниження ризику первинної кінцевої точки припадала на початковий етап спостереження: ВР для перших 6 місяців ПС становило 0,60 (95% ДІ 0,38–0,93), для першого року – 0,76 (95% ДІ 0,60–0,96) і для другого року – 0,90 (95% ДІ 0,75–1,07) (рис. 2) [7]. Аналіз впливу терапії емпагліфлозином порівняно з плацебо на вторинні кінцеві точки протягом активної фази й ПС сукупно показав зниження ризику прогресування ХХН на 21% (частота події в групах емпагліфлозину й плацебо – 23,5 та 27,1% відповідно; ВР 0,79, 95% ДІ 0,72–0,87) (табл. 2), ризику розвитку термінальної стадії ХХН– на 26% (9,0 і 11,3% відповідно; ВР 0,74, 95% ДІ 0,64–0,87) і ризику комбінації «термінальна стадія ХХН /смерть від будь-якої причини» – на 19% (16,9 і 19,6% відповідно; ВР 0,81, 95% ДІ 0,72–0,90). У періоді ПС значення ВР для цих вторинних кінцевих точок становили 0,89 (95% ДІ 0,77–1,02), 0,80 (95% ДІ 0,66–0,98) і 0,82 (95% ДІ 0,70–0,96) відповідно [7].
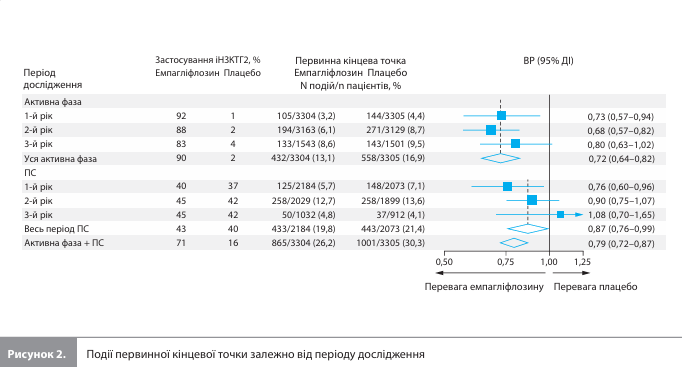
Розрахунок абсолютної міжгрупової різниці (± стандартна помилка) на 1000 пацієнтів із використанням кривих Каплана-Мейєра показав, що застосування емпагліфлозину було пов'язане зі зменшенням кількості хворих із подіями первинної кінцевої точки порівняно з плацебо на 57 ± 14 осіб у кінці активної фази й на 45 ± 14 осіб у кінці всього дослідження (активна фаза і ПС сукупно). Для термінальної стадії ХХН і комбінації «термінальна стадія ХХН / смерть від будь-якої причини» кількість пацієнтів із подіями при використанні емпагліфлозину порівняно з плацебо зменшилася на 26 ± 8 і 25 ± 11 осіб у кінці активної фази й на 25 ± 10 і 32 ± 12 осіб у кінці всього дослідження відповідно [7]. Аналіз підгруп показав, що вихідний статус ЦД, величина рШКФ, САК і причина ХХН не впливали на величину ефекту емпагліфлозину на первинну кінцеву точку порівняно з плацебо (рис. 3) [7].
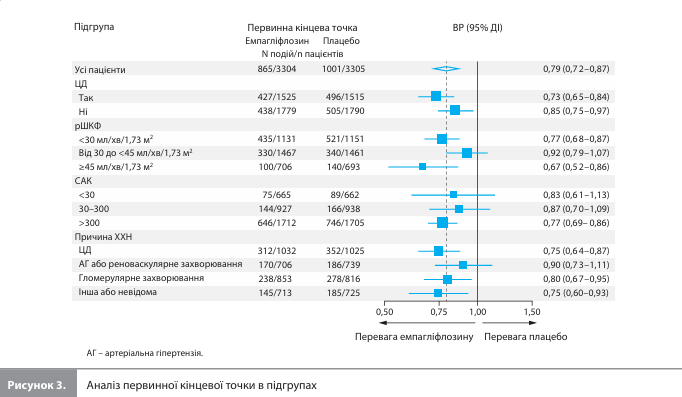
За весь період дослідження (активна фаза і ПС сукупно) СС смертність була істотно нижчою в групі емпагліфлозину (3,8 проти 4,9% в групі плацебо; ВР 0,75, 95% ДІ 0,59– 0,95), тоді як показники неСС (5,3% в обох групах; ВР 0,97; 95% ДІ 0,79–1,20) і загальної смертності (9,1 проти 10,2% відповідно; ВР 0,86; 95% ДІ 0,74–1,01) були зіставними в групах лікування (табл. 2) [7]. Середнє значення (± стандартна помилка) рШКФ при останньому вимірюванні в кінці періоду ПС у пацієнтів без термінальної стадії ХХН становило 31,4 ± 0,2 мл/хв/1,73 м2 у групі емпагліфлозину й 30,6 ± 0,2 мл/хв/1,73 м2 у групі плацебо (абсолютна різниця 0,8 мл/хв/1,73 м2; 95% ДІ 0,1–1,4). Результати оцінки абсолютної різниці значень рШКФ у ключових підгрупах не відрізнялися від показника в загальній досліджуваній вибірці пацієнтів [7].
Обговорення результатів дослідження Herrington et al. Раніше повідомлялося, що в ході активної фази дослідження EMPA-KIDNEY емпагліфлозин знижував ризик прогресування ХХН або СС смерті (первинна кінцева точка) протягом 2 років у вибірці хворих на ХХН, викликану широким спектром причин, із різним ступенем порушення функції нирок і різною тяжкістю альбумінурії, не викликаючи серйозних проблем із безпекою [3]. Herrington et al. у своєму звіті про результати 2-річного ПС, яке проводилося після закінчення активної фази дослідження EMPA-KIDNEY, показали збереження залишкових кардіоренальних переваг емпагліфлозину після його скасування як досліджуваного препарату. Частота призначення лікарями доступних іНЗКТГ2 в період ПС була зіставною в групах емпагліфлозину та плацебо. Корисні ефекти емпагліфлозину щодо ризику розвитку первинної кінцевої точки та її компонентів зберігалися до 12 місяців ПС і були найбільш виражені в перші 6 місяців після закінчення активної фази дослідження. Крім іншого, це підтверджує необхідність тривалого застосування іНЗКТГ2 при ХХН для отримання максимальної клінічної користі від лікування [7]. Механізми тривалого збереження корисних ефектів після скасування іНЗКТГ2 поки невідомі, але можуть бути пов'язані як зі збереженням кількості життєздатних нефронів на тлі приймання препарату (що зменшує гіперфільтрацію і ризик термінальної стадії ХХН), так і з деякими довготривалими СС ефектами іНЗКТГ2, що знижують ризик СС смерті [8]. Відомий феномен короткострокового зниження рШКФ на початковому етапі лікування з подальшим (протягом 4 тижнів після скасування іНЗКТГ2) її відновленням [9, 10] може частково пояснити уповільнення темпів зниження рШКФ на початку ПС, але не пояснює переваги емпагліфлозину при термінальній стадії ХХН [7]. Сучасні міжнародні настанови містять рекомендації різної сили щодо використання іНЗКТГ2 у хворих на ХХН, які відповідають критеріям дослідження EMPA-KIDNEY, залежно від рівня альбумінурії [11]. Більш тривале спостереження і майже двократне збільшення числа подій первинної кінцевої точки EMPA-KIDNEY (із 990 протягом активної фази до 1866 за весь період дослідження [до кінця періоду ПС]) можуть допомогти відповісти на запитання, що виникли на основі результатів аналізу даних з активної фази дослідження [3]. Так, Herrington et al. показали, що переваги емпагліфлозину у вигляді зниження ризику подій первинної кінцевої точки і прогресування ХХН, а також впливу на результати останнього вимірювання рШКФ в кінці ПС не залежали від рівня альбумінурії, наявності ЦД, ступеня порушення функції нирок і основної причини ХХН. Аналіз кута нахилу графіка зміни рШКФ в активній фазі дослідження також показав, що емпагліфлозин уповільнював прогресування ХХН у всіх підгрупах пацієнтів із різним ступенем тяжкості альбумінурії [9, 12]. Практичну користь і надійність цих результатів підтверджують дизайн (велика кількість учасників, широкі критерії включення) і якість (високий рівень комплаєнтності учасників, великий відсоток пацієнтів, які перейшли в період ПС і повністю пройшли всі процедури ПС) дослідження EMPA- KIDNEY. Серед обмежень, які потрібно враховувати при інтерпретації результатів, автори вказують на відсутність участі пацієнтів із Японії (із логістичних причин), вимірювання рівня креатиніну під час ПС у місцевих лабораторіях і відсутність додаткових даних про госпіталізацію (що не дозволило оцінити ефекти досліджуваного лікування на ризик госпіталізації протягом ПС) [7].
Висновок Отже, аналіз даних періоду подальшого спостереження, що дозволив удвічі збільшити загальну тривалість РКД EMPA-KIDNEY і зібрати більше інформації про події кінцевих точок, показав, що в широкого кола пацієнтів із ХХН і ризиком її прогресування, які отримували нетривалу 2-річну терапію емпагліфлозином, користь від лікування для СС системи і нирок зберігалася ще протягом року після скасування препарату в кінці активної фази дослідження.
Список літератури знаходиться в редакції
Автор огляду Микола Горін Medicine Review 2025; 6 (87): 21 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2026. Усі права захищені.
|
мапа сайту корисні посилання |