Ефективність метопрололу в профілактиці рецидиву фібриляції передсердь після кардіоверсії: результати багатоцентрового рандомізованого дослідженняФібриляція передсердь (ФП) є найпоширенішою хронічною аритмією, яка спричиняє значне підвищення захворюваності, погіршення якості життя і зниження працездатності порівняно із синусовим ритмом (СР) [1–3], що робить відновлення (кардіоверсію) та подальше підтримання СР основними завданнями терапії ФП. Із метою тривалого підтримання СР у пацієнтів з анамнезом ФП наразі застосовують цілу низку антиаритмічних препаратів (ААП), зокрема аміодарон, дронедарон, флекаїнід і пропафенон, які дають змогу підвищити якість життя, сповільнити прогресування ФП та її ускладнень і потенційно знизити рівень захворюваності, пов’язаної з ФП. Хоча ААП і не усувають ризик рецидивів ФП, але вони дають змогу зробити епізоди аритмії більш рідкісними, менш тривалими й менш нестерпними для пацієнтів, що вважається успіхом такого роду терапії. Крім перерахованих вище ААП, при ФП також використовують препарати з групи бета-адреноблокаторів (БАБ), і хоча при ФП їх частіше застосовують для контролю частоти серцевих скорочень (ЧСС), також було показано, що БАБ сприяють збереженню СР і знижують ризики рецидиву ФП після успішної кардіоверсії. Зокрема, такий ефект було виявлено в багатоцентровому рандомізованому подвійному сліпому плацебо-контрольованому дослідженні Kühlkamp et al. під час використання селективного блокатора β1-адренорецепторів метопрололу CR/XL (форма з контрольованим вивільненням, що забезпечує стабільну концентрацію метопрололу в крові впродовж 24 годин) у пацієнтів із ФП і відновленням СР після кардіоверсії [4]. Основна інформація про це дослідження стисло представлена в нашому огляді.
Методологія дослідження Kühlkamp et al. У цьому проспективному рандомізованому плацебо-контрольованому дослідженні взяли участь пацієнти з персистуючою формою ФП тривалістю від трьох днів і до одного року, у яких було заплановано проведення електричної (постійним струмом) або фармакологічної (ААП класу 1) кардіоверсії. Основними критеріями виключення були: протипоказання до застосування БАБ (наприклад, атріовентрикулярна [АВ] блокада II/III ступеня на момент огляду або в анамнезі, синдром слабкості синусового вузла, бронхіальна астма), хронічна пероральна терапія аміодароном у межах 6 місяців до включення в дослідження, супутнє лікування будьяким ААП 1 або 3 класу в межах 5 періодів напіввиведення препарату, операція на серці в попередні 2 місяці, клінічна необхідність супутнього лікування БАБ і нелікована дисфункція щитовидної залози. До участі в дослідженні також не допускали пацієнтів із пароксизмальною формою ФП на момент огляду або в анамнезі [4]. Усім учасникам настійно рекомендували адекватну антикоагулянтну терапію перед кардіоверсією і протягом щонайменше одного місяця після неї. Після кардіоверсії хворих рандомізували для отримання метопрололу CR/XL або плацебо. Початкова доза метопрололу CR/XL становила 100 мг 1 раз/добу. Дослідники отримали рекомендацію щодо збільшення дози метопрололу до 200 мг 1 раз/добу, утім за необхідності дозу препарату можна було залишити на рівні 100 мг 1 раз/добу або знизити до 50 мг 1 раз/добу. Супутня медикаментозна терапія не обмежувалася, проте застосування будь-якого ААП 1 або 3 класу, БАБ або блокатора кальцієвих каналів розглядалося як критерій виключення з дослідження [4]. Спостереження за пацієнтами проводили амбулаторно, воно передбачало проведення оглядів через тиждень, 1, 3 й 6 місяців після включення в дослідження, а також у разі розвитку рецидиву ФП або небажаних явищ. Під час кожного огляду проводили реєстрацію електрокардіограми (ЕКГ) у стані спокою, також ЕКГ реєстрували при появі симптомів, підозрілих на рецидив ФП. Після завершення дослідження всі ЕКГ вивчали в центральній лабораторії в сліпому режимі з оцінкою переважного ритму й розрахунком ЧСС. Крім того, на вихідному рівні проводили ехокардіографію з вимірюванням кінцево-систолічного й кінцево-діастолічного розмірів лівого шлуночка (ЛШ), товщини міжшлуночкової перегородки і задньої стінки ЛШ, а також фракційного вкорочення і діаметра лівого передсердя (ЛП) [4].
Первинною кінцевою точкою дослідження була кількість пацієнтів із рецидивом ФП або тріпотіння передсердь (ТП) упродовж 6 місяців після кардіоверсії, що призвела до відновлення СР. Вторинними кінцевими точками були частота скорочень шлуночків у пацієнтів із рецидивом ФП або ТП і параметри переносимості метопрололу CR/XL [4]. В основу дослідження лягло припущення про те, що в групі плацебо рецидив ФП протягом 6-місячного спостереження розвинеться у 70% пацієнтів, і що метопролол CR/XL знизить це значення до 55%. Для аналізу первинної кінцевої точки використовували логранговий критерій із номінальними двосторонніми значеннями p. Аналіз проводили з урахуванням лікування, призначеного під час рандомізації (підхід intention-to-treat). Дані про пацієнтів із СР були цензуровані на дату останнього візиту подальшого спостереження. Дані про ЧСС порівнювали з використанням t-критерію, для решти змінних було представлено описову статистику [4].
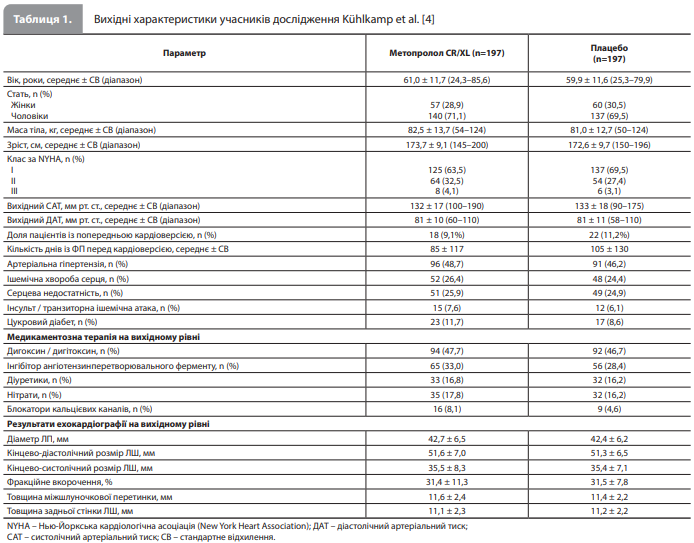
Результати дослідження Kühlkamp et al. У дослідження ввійшли 403 пацієнти, із них дані 9 осіб (5 із групи метопрололу CR/XL і 4 із групи плацебо) були виключені з остаточного аналізу, оскільки в них була відсутня інформація про подальше спостереження. Отже, в остаточний аналіз увійшли дані 394 пацієнтів, із яких 197 отримували метопролол і 197 – плацебо. Отримані групи були добре збалансовані за всіма вихідними характеристиками (табл. 1), у тому числі за тривалістю ФП до кардіоверсії та за часткою пацієнтів із попередньою електричною або фармакологічною кардіоверсією в анамнезі [4]. У більшості пацієнтів відновлення СР у рамках дослідження було досягнуто за допомогою кардіоверсії постійним струмом (n=325, 82,5%). Підгрупа пацієнтів, які пройшли фармакологічну кардіоверсію за допомогою ААП 1 класу (n=69, 17,5%), не відрізнялася за вихідними характеристиками від пацієнтів, які пройшли електричну кардіоверсію. Більшість учасників дослідження отримували 100 мг метопрололу CR/ XL (n=122, 62%) або відповідну дозу плацебо (n=131, 67%) 1 раз/добу. Дозу було знижено до 50 мг 1 раз/добу у 36 пацієнтів (18,3%) із групи метопрололу CR/XL і у 12 пацієнтів (6,1%) із групи плацебо. Відповідно в 33 (16,8%) і 50 (25,4%) пацієнтів у цих групах доза досліджуваного препарату була збільшена до 200 мг 1 раз/добу [4].
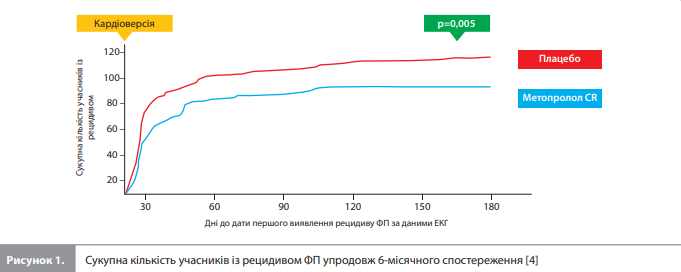
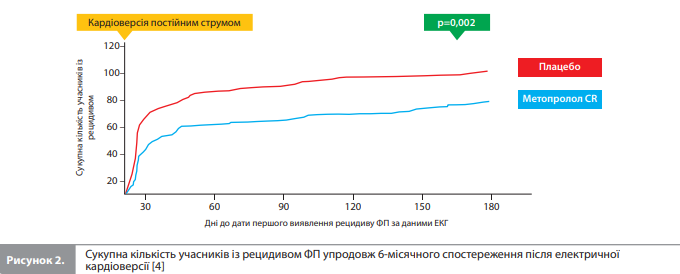
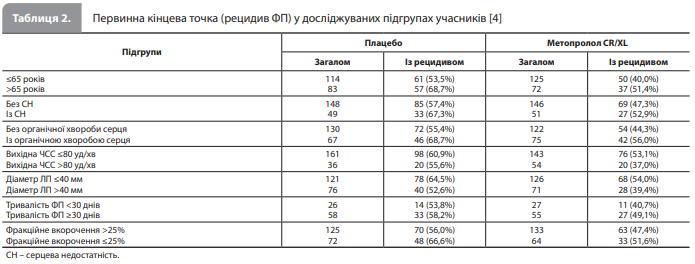
Аналіз первинної кінцевої точки показав, що рецидив ФП або ТП розвинувся в 118 пацієнтів (59,9%) із групи плацебо й у 96 пацієнтів (48,7%) із групи метопрололу CR/XL (p=0,005, рис. 1). У підгрупі учасників, які пройшли електричну кардіоверсію, частота рецидиву ФП/ТП становила 65,0 і 50,6% відповідно (p=0,002, рис. 2>) [4]. Медіана часу до рецидиву ФП становила 7,5 дня в групі плацебо і 13,0 днів у групі метопрололу CR/XL (p=0,001). Середній період спостереження в групі плацебо становив 73 ± 80 днів порівняно з 93 ± 81 день у групі метопрололу. Здатність метопрололу CR/XL знижувати ризик рецидиву ФП була продемонстрована в усіх проаналізованих підгрупах (табл. 2) [4].
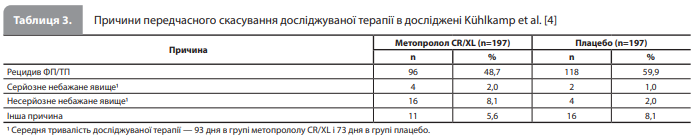
Аналіз ефекту досліджуваної терапії на ЧСС показав такі результати. Середня ЧСС у пацієнтів із рецидивом ФП або ТП становила 107 ± 27 уд/хв у групі плацебо порівняно з 98 ± 23 уд/хв у групі метопрололу (p=0,015) [4]. За відсутності рецидиву аритмії ЧСС на останньому візиті дослідження порівняно з вихідним значенням продемонструвало зниження (з 74 ± 14 уд/хв до 64 ± 11 уд/хв) у групі метопрололу CR/XL й деяке збільшення (з 70 ± 11 уд/хв до 72 ± 13 уд/хв) у групі плацебо. Міжгрупова різниця за ЧСС під час подальшого спостереження була високо статистично значущою (p=0,0001) [4]. Оцінка безпечності й переносимості лікування показала такі результати. Серйозні небажані явища й небажані явища, що призвели до скасування досліджуваного лікування, були зареєстровані у 20 пацієнтів із групи метопрололу й у 6 пацієнтів із групи плацебо (табл. 3), що, однак, слід інтерпретувати з урахуванням більшої тривалості спостереження за учасниками в групі метопрололу порівняно з групою плацебо. Основними причинами передчасного припинення приймання досліджуваного препарату в групі метопрололу CR/ XL були запаморочення, АВ-блокада II ступеня та задишка при фізичному навантаженні. Запаморочення, вертиго, нудота й брадикардія частіше реєструвалися в групі метопрололу CR/XL, ніж у групі плацебо. За час дослідження померли три пацієнти – усі з групи метопрололу. Один пацієнт раптово помер на тлі дилатаційної кардіоміопатії, другий помер унаслідок ішемічного інсульту, третій – від геморагічного інсульту через тиждень після рецидиву ФП на тлі пероральної антикоагуляції фенпрокумоном [4].
Обговорення результатів дослідження Kühlkamp et al. Представлене дослідження показало, що порівняно з плацебо терапія метопрололом CR/XL призвела до значного зменшення частки пацієнтів, у яких протягом 6 місяців після успішної кардіоверсії стався рецидив ФП. Цей ефект досягався на тлі хорошої безпечності й переносимості лікування, зокрема без розвитку проаритмічних ефектів і без значущого зростання частоти серйозних некардіальних ефектів, які потребують припинення терапії, порівняно з плацебо. Не менш важливо, що крім захисту від рецидиву ФП, БАБ, як відомо, покращують прогноз в осіб з артеріальною гіпертензією, пацієнтів після перенесеного інфаркту міокарда і у хворих на серцеву недостатність, яких досить багато в популяції пацієнтів із ФП [5–10]. Проте ефект метопрололу CR/XL на рецидив ФП не можна пояснити винятково кращим контролем фонових серцевих захворювань, оскільки його протирецидивна ефективність була зіставною в усіх проаналізованих підгрупах пацієнтів (табл. 2) [4].
Висновок Результати дослідження Kühlkamp et al. дають змогу зробити висновок, що метопролол CR/XL перевершує плацебо за здатністю знижувати ризик рецидиву ФП після успішної фармакологічної або електричної кардіоверсії, і що схема терапії метопрололом CR/XL, яка використовувалась у дослідженні, була безпечною і добре переносилася пацієнтами протягом 6-місячного періоду спостереження.
Список літератури знаходиться в редакції
Автор огляду Олена Грибова Medicine Review 2024; 6 (79): 16 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2025. Усі права захищені.
|
мапа сайту корисні посилання |