Кінцеві точки в дослідженнях методів лікування серцевої недостатності: минуле, сьогодення і майбутнєСерцева недостатність (СН) – це широко розповсюджений синдром (поширеність близько 2% у загальній популяції та 10% – серед людей літнього віку в західних країнах), пов’язаний зі значним зростанням захворюваності й смертності, а також медичних витрат, що робить її однією з найсерйозніших проблем суспільної охорони здоров’я [1–3]. Очікується, що старіння населення та вдосконалення методів лікування гострих серцево-судинних (СС) подій призведуть до подальшого зростання поширеності СН, незважаючи на ефективність багатьох сучасних методів терапії СН, які не просто полегшують симптоми й покращують гемодинамічні параметри, а й оптимізують віддалений прогноз через зниження захворюваності та ліпшу виживаність пацієнтів, про що свідчать результати оцінки специфічних для СН кінцевих точок (КТ) у численних клінічних дослідженнях [4]. Нижче представлено стислий огляд статті Hussain et al., що висвітлює еволюцію підходу до вибору СС КТ для використання в клінічних дослідженнях СН [4].

Еволюція КТ у дослідженнях методів лікування СН Як відомо, до 1970-х років варіанти терапії СН обмежувалися препаратами наперстянки й діуретиками, які давали змогу лише полегшити симптоми СН. Пізніше в арсеналі лікарів з’явилися вазодилататори, які, крім полегшення симптомів, позитивно впливали на показники гемодинаміки в людини, хворої на СН. Вазодилататори також оцінювали за їхнім впливом на смертність пацієнтів із СН, і перше велике кардіологічне рандомізоване плацебо-контрольоване клінічне дослідження V-HeFT I виявило тенденцію щодо зниження смертності за умови використання вазодилататорів [5]. Однак згодом, наприкінці 1980-х років, дослідження нової групи препаратів – інгібіторів ангіотензинперетворювального ферменту – продемонстрували їхню перевагу над вазодилататорами з погляду поліпшення виживаності та збереження ефективності на різних стадіях СН, що зсунуло цілі лікування з корекції порушень гемодинаміки на нейрогормональну блокаду [6–8]. Потім, наприкінці 1990-х років, послідувала ціла низка великомасштабних досліджень, які показали покращення виживаності серед пацієнтів із СН, які отримували бета-адреноблокатори, антагоністи мінералокортикоїдних рецепторів і, зовсім недавно, комбінацію блокатора рецепторів ангіотензину та інгібітора неприлізину, а також інгібітори натрійзалежного котранспортера глюкози 2 типу (іНЗКТГ2), в умовах СН зі зниженою фракцією викиду (СНзнФВ) [9–14]. Більшість із цих досліджень демонстрували узгоджені результати оцінок безпеки й ефективності, пов’язані зі зменшенням тяжкості симптомів, поліпшенням функціональних можливостей, підвищенням переносимості фізичних навантажень і зниженням частоти госпіталізацій. Ці результати докорінно відрізнялися від отриманих у дослідженнях інотропних препаратів, які в деяких випадках асоціювалися з підвищенням ризику смерті, що призвело до появи нормативних актів, які вимагали для реєстрації нових препаратів обов’язкового проведення клінічних досліджень з оцінкою ефектів на смертність (окремо або в поєднанні з іншими наслідками) [15]. Згодом, після того як госпіталізації з приводу СН (ГСН) визнали одними із найсильніших предикторів смертності та маркерів тяжкості захворювання і навантаження на систему охорони здоров’я, основний акцент у дослідженнях СН змістився зі зменшення ризику смерті на зниження ризику комбінації ГСН і загальної або серцево-судинної (СС) смертності [12–14, 16–18]. І дотепер КТ, що включають смертність і ГСН, розглядаються регуляторними органами як джерело надійної інформації для реєстрації нового методу лікування за умови достатності даних щодо його безпеки. Для будь-якого досліджуваного препарату критично важливо показати, що він не підвищує ризик смерті, водночас у разі зниження ризику комбінації ГСН і загальної / СС смертності вкрай важливо прояснити, з чим саме пов’язаний корисний ефект – зі зниженням ризику госпіталізацій, зниженням смертності або зменшенням ризику обох компонентів цієї комбінованої КТ. Від відповіді на це запитання залежить, зокрема, клас рекомендації щодо застосування препарату в настановах із ведення СН, у яких, наприклад, івабрадин і дигоксин, які в дослідженнях зменшували кількість ГСН, але не знижували смертність, отримали рекомендацію класу II, а не класу I [16, 19–21]. Нещодавні дослідження іНЗКТГ2 додатково посилили акцент на комбінованій КТ, що включає СС смерть і ГСН, у дослідженнях, присвячених СН [13, 14, 22–24]. Історично склалося так, що після того, як 2008 року Управління з нагляду за якістю харчових продуктів і лікарських засобів США (FDA) випустило настанову щодо розроблення нових препаратів для лікування цукрового діабету (ЦД) 2 типу, було проведено безліч великих рандомізованих контрольованих досліджень (РКД), основною метою яких була оцінка безпечності протидіабетичних препаратів (ПДП) за первинною КТ – серйозними несприятливими СС подіями (MACE), до яких належать СС смерть, нефатальний інфаркт міокарда (ІМ) і нефатальний інсульт, і серед яких немає СН [25]. Однак згодом кілька РКД, а саме дослідження іНЗКТГ2, показали сильний вплив цих ПДП на наслідки, пов’язані із СН, які не були спочатку заявлені як первинні КТ [26]. Після того, як усі РКД із застосуванням іНЗКТГ2 послідовно повідомили про зниження ризику ГСН серед хворих на ЦД, були організовані й проведені нові дослідження іНЗКТГ2 серед пацієнтів із СНзнФВ (із ЦД і без ЦД), які повторно продемонстрували безпечність й ефективність цих препаратів у зниженні первинної комбінованої КТ, яка включала СС смерть і ГСН, у пацієнтів із СНзнФВ незалежно від статусу ЦД [13, 14]. Цей результат підкреслює важливість КТ, пов’язаних із СН, для всіх СС досліджень, а також той факт, що дослідження СС захворювань не мають фокусуватися винятково на оцінці ризику подій MACE, які більшою мірою відображають вплив терапії на ішемічні наслідки, але не на наслідки, пов’язані із СН [4]. Слід зазначити, що у зв’язку з динамічними змінами в моделях надання медичної допомоги, наразі КТ, пов’язані з СН, включають, окрім власне ГСН, надання екстреної або невідкладної допомоги у зв’язку з СН, а також потребу в проведенні внутрішньовенної (в/в) терапії діуретиками. У майбутньому до цих КТ можуть також віднести терапію, що проводиться в домашніх умовах, і віддалені візити, пов’язані з СН [4]. Терапія СН, що покликана зменшити вираженість застійних явищ і поліпшити гемодинамічні параметри, може також мати несприятливі наслідки, зокрема ушкодження нирок або міокарда, які можуть звести нанівець переваги лікування, як, наприклад, спостерігалося в клінічних дослідженнях ультрафільтрації. Автори дослідження CARRESS-HF, виходячи з того, що гострий кардіоренальний синдром (КРС) часто спостерігається під час госпіталізації з приводу декомпенсації СН та є предиктором несприятливих наслідків [27], а венозна ультрафільтрація забезпечує контроль швидкості видалення й об’єму видаленої рідини та меншу активацію нейрогормональної осі, запропонували цей метод для зменшення застійних явищ і лікування дисфункції нирок у пацієнтів, госпіталізованих із гострою декомпенсованою СН і КРС, які не відповідають на медикаментозну терапію [28]. Однак отримані результати показали, що ультрафільтрація порівняно з терапією на основі діуретиків не забезпечила значних переваг із погляду зменшення маси тіла через 96 годин, впливу на рівень 60-денної смертності або частоту госпіталізацій, але при цьому значно збільшувала рівень креатиніну в сироватці [29], а також була пов’язана з вищою частотою небажаних явищ у вигляді ниркової недостатності, кровотеч і ускладнень, пов’язаних із внутрішньовенним катетером [30]. Як і у випадку з КТ «ГСН», КТ, пов’язані з пристроями та інтервенційними втручаннями, згодом змінилися, і тепер охоплюють не тільки наслідки, що відображають ефективність і безпечність пристроїв / втручань, а й клінічні наслідки та результати, про які повідомляють пацієнти. Однак у більш ранніх клінічних дослідженнях акцент на жорстких клінічних КТ призводив до того, що основна увага приділялася впливу терапії на ризик смерті та/або госпіталізації, а інтерес до таких критичних для пацієнтів і ухвалення рішень наслідків, як полегшення симптомів, поліпшення якості життя, функціональних можливостей і переносимості фізичних навантажень, був доволі обмеженим [4]. Тому вкрай важливою э нещодавно випущена FDA рекомендація, за якою основою для схвалення препарату, призначеного для лікування СН, може стати факт полегшення симптомів або покращення фізичної функції навіть за відсутності сприятливого впливу терапії на виживаність або ризик ГСН [31]. Очевидно, що в цьому випадку необхідні докази безпечності нового препарату у вигляді відсутності збільшення смертності або ризику госпіталізацій [15]. Звісно, випадки госпіталізації та декомпенсації СН, які потребують в/в терапії, також є КТ, важливими для пацієнтів, оскільки призводять до погіршення якості життя. При цьому, незважаючи на ефективність сучасних методів лікування, за останні 30 років частота перших і повторних ГСН знизилася незначно, як і пов’язані з ними витрати на охорону здоров’я [2]. Це створило потребу в розробці та використанні нових комбінованих КТ для оцінки ефективності та безпечності нових методів лікування. Як приклад можна навести дослідження імплантованих систем для довгострокового моніторингу тиску в легеневій артерії (CardioMEMS Heart Sensor), які дають змогу проводити орієнтоване на гемодинаміку амбулаторне лікування пацієнтів із хронічною СН, забезпечують значне зниження частоти ГСН і поліпшення якості життя пацієнтів [32–34]. У клінічних дослідженнях подібних систем комбінацію зміни показників гемодинаміки й частоти ГСН використовували як КТ ефективності, а ускладнення, пов’язані з пристроєм, – як КТ безпеки, і це є прикладом унікального поєднання гемодинамічних КТ і КТ безпеки, що відображають ефективність і безпечність пристрою, з одного боку, та клінічних КТ, значущих для пацієнтів і систем медичного обслуговування, зокрема якості життя і частоти повторних ГСН, – з іншого боку [34, 35].
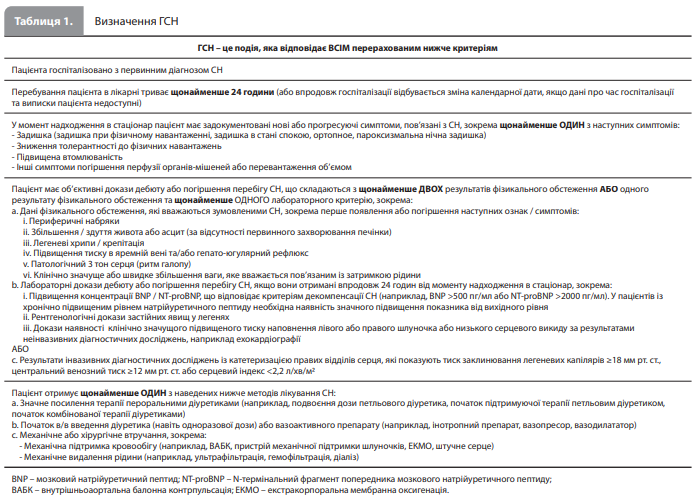
СС КТ, що використовуються в сучасних дослідженнях СН Основним обмеженням при порівнянні результатів досліджень як усередині однієї програми розробки препарату або пристрою, так і між різними програмами тривалий час була відсутність єдиних визначень СН і подій ключових КТ. Згодом було проведено стандартизацію цих визначень із використанням об’єктивних критеріїв та уніфікованих методів звітності, що забезпечило оптимальний облік подій, пов’язаних із СН [4]. Слід зазначити, що відповідно до сучасних уявлень ситуації, які не є власне ГСН, але входять до категорії подій, пов’язаних із СН, мають прогностичне значення, аналогічне значенню ГСН. До таких аналогічних ГСН подій належать, зокрема, екстрена допомога або візит до відділення невідкладної допомоги, які призводять до в/в терапії діуретиками та/або вазоактивними препаратами, оскільки ці події вказують на декомпенсацію СН, що збільшує витрати на охорону здоров’я та потенційно впливає на прогноз пацієнта. Ці події, разом із ГСН, часто включають у первинну КТ досліджень нових препаратів і пристроїв разом із загальною або СС смертністю (яка, як і раніше, важлива для реєстрації нових методів лікування). Проте різні події, пов’язані з СН, не є рівнозначними, що ускладнює процес порівняння різних методів лікування СН [4]. Подія, пов’язана з СН. В останній версії документу, що містить визначення СС і цереброваскулярних (пов’язаних з інсультом) КТ, розроблених спільно FDA і Програмою зі збору стандартизованих даних для СС досліджень, ГСН і події СН, не пов‘язані з ГСН, зазначено як важливі КТ для досліджень методів лікування СН і методів лікування, не пов’язаних із СН, але здатних вплинути на ризик СН [36]. Події, пов’язані з СН, включають ГСН та екстрені амбулаторні візити й визначаються за сукупністю ознак, симптомів, результатів діагностичних обстежень і методів лікування, спрямованих на СН (табл. 1 і 2) [4]. Підкреслюється, що слід відокремлювати ГСН від екстрених візитів, і що під час включення екстрених візитів до КТ, що описує події СН, кількість екстрених візитів необхідно оцінювати окремо від кількості ГСН [36]. ГСН. Згідно з визначенням, ГСН – це позапланова госпіталізація з основним діагнозом СН, яка триває більше ніж 24 години або більше одного календарного дня за умови наявності в пацієнта типових ознак, симптомів і результатів обстежень, що відповідають діагнозу СН (табл. 1) [4, 36]. Екстрений амбулаторний візит. Критерієм цієї події СН, не пов’язаної з ГСН, є екстрений позаплановий візит пацієнта до кабінету лікаря або до відділення невідкладної допомоги з приводу СН; при цьому в пацієнта мають бути ознаки, симптоми, а також лабораторні та інструментальні дані на підтримку СН, аналогічні описаним для ГСН [4], і він також має потребувати проведення терапії, аналогічної описаній вище для ГСН (табл. 1 і 2) [36]. Очевидно, що в це визначення не вписуються госпіталізації в клініку для планового лікування СН (наприклад, для в/в введення діуретиків, вазоактивних препаратів або механічного видалення рідини) [36].

Смерть від будь-яких причин. У клінічних дослідженнях смерть зазвичай використовують як КТ ефективності або безпеки. При оцінці цього результату величезне значення мають використання стандартизованих визначень і збір вихідної документації з інформацією про причину смерті, у тому числі свідоцтв про смерть (невисокий рівень достовірності інформації про причину смерті) і звіти про розтин (не завжди доступні) [37]. СС смерть. До цієї категорії належать випадки раптової серцевої смерті, випадки смерті внаслідок гострого ІМ, СН, інсульту, СС процедур, СС кровотечі та інших СС причин [36]. Серед пацієнтів із СНзнФВ і симптомами II і III функціонального класу за класифікацією New York Heart Association (NYHA), приблизно 90% смертей належать до категорії СС смерті, і тільки 10% – до смерті не від СС причин [38]. Смерть унаслідок СН. Ця категорія описує смерть, що настала внаслідок погіршення симптомів і/або ознак СН або як наслідок невиліковної СН. Така смерть зазвичай настає під час або після госпіталізації, і може статися в лікарні, вдома, в закладі тривалого догляду або в хоспісі. Гемодинамічні КТ. Дослідження пристроїв, особливо черезшкірних пристроїв для лікування гострої / декомпенсованої СН із розвитком кардіогенного шоку, також дають змогу по-новому поглянути на КТ для клінічних досліджень у пацієнтів із СН. Наприклад, при рефрактерному циркуляторному шоці застосовують пристрої механічної підтримки кровообігу або пристрої для екстракорпоральної мембранної оксигенації, які забезпечують виразні сприятливі гемодинамічні зміни з боку тиску в шлуночках / об’єму шлуночків, серцевого викиду й рівня артеріального тиску (АТ). На відміну від досліджень лікарських препаратів, у яких застосовують жорсткі клінічні КТ, більшість досліджень черезшкірних пристроїв підтримки функції лівого шлуночка прагнули продемонструвати поліпшення специфічних для пристрою гемодинамічних параметрів, таких як серцевий викид, АТ, тиск заклинювання легеневих капілярів, тиск у правому передсерді або системний судинний опір [39–42]. Оскільки ці дослідження проводили в пацієнтів із шоком і високим ризиком смерті, симптоми не брали до уваги, однак, з огляду на високу інвазивність методик, процедурні ускладнення також розглядали як КТ. У цих дослідженнях ефект лікування відображали сурогатні гемодинамічні КТ, і очікувалося, що вони корелюватимуть із клінічною користю. Тобто сурогатні кінцеві точки також можуть мати важливе значення, наприклад, у дослідженнях пристроїв або в невеликих дослідженнях із відносно коротким періодом спостереження, у яких буває складно оцінити клінічні КТ, що ґрунтуються на симптомах або виживаності пацієнтів [4]. Інші КТ. При розробці досліджень методів лікування СН або методів, здатних вплинути на перебіг СН, необхідно враховувати низку не завжди очевидних аспектів. Наприклад, у клінічних дослідженнях з аналізом часу до розвитку першої події комбінованої КТ, до якої входять смерть і ГСН, усі події, що розвинулися після першої, цензурують, прибираючи з підсумкової оцінки вплив багаторазових повторних госпіталізацій. З іншого боку, тривале перебування в стаціонарі під час першої госпіталізації зменшує тривалість періоду оцінки ризику повторної госпіталізації, а смерть пацієнта повністю виключає його з цієї оцінки. Для розв’язання цих суперечностей запропоновано використовувати такі КТ, як комбінація смерті й повторних госпіталізацій – для досліджуваних методів, що не впливають на тривалість індексної госпіталізації (ТІГ), та комбінація смерті, ТІГ і повторних госпіталізацій – для втручань, які можуть вплинути на ТІГ [4]. Не меншої уваги заслуговує використання КТ «госпіталізація з будь-якої причини» у програмах розробки препаратів для лікування СН. Особливо це стосується препаратів, які можуть впливати на перебіг супутніх захворювань, наприклад знижувати ризик ФП на додачу до зниження ризиків СН або (як деякі ПДП) зменшувати як кількість госпіталізацій із приводу ЦД, так і кількість ГСН. Крім того, КТ «госпіталізація з будь-якої причини» може бути корисною для досліджень у когортах пацієнтів із СН і збереженою ФВ ЛШ (СНзбФВ), для яких типова висока коморбідність і потреба в стаціонарному лікуванні [43], а також для досліджень апаратних методів лікування чи інвазивних втручань, які мають потенційні процедурні ризики чи ускладнення, які можуть вимагати госпіталізації через проведене лікування / втручання. Однак слід мати на увазі, що статистична потужність і чутливість аналізу значно підвищуються під час вивчення конкретних категорій госпіталізацій, на які, як очікується, впливає досліджуване лікування (наприклад, ГСН у дослідженнях терапії СН). Навпаки, і потужність, і чутливість аналізу знижуються в разі включення в КТ результатів, «нечутливих» до досліджуваної терапії (наприклад, госпіталізації з приводу раку або інсульту в дослідженнях терапії СН). Також статистична потужність значно знижується, якщо в аналізі враховується тільки перша госпіталізація з будь-якої причини (як в аналізі часу до розвитку першої події комбінованої КТ, описаному вище). Наприклад, за даними дослідження SOLVD, приблизно 38% ГСН в учасників дослідження сталися після попередньої госпіталізації з іншої причини [8]. Примітно, що, якби в цьому дослідженні замість ГСН використовувалася КТ «перша госпіталізація з будь-якої причини», це суттєво знизило б показники ефективності досліджуваного лікування [4]. Тобто необхідно враховувати, що оцінка всіх госпіталізацій призводить до зниження статистичної потужності результату через включення великої кількості нечутливих подій та (як у випадку з аналізом часу до розвитку першої події КТ) втрату суттєвої частини справді чутливих подій. Одним із підходів, запропонованих для оптимізації оцінки КТ, є комплексне ранжування (Global Ranking Approach), що дає змогу врахувати багато аспектів клінічного перебігу хвороби, включно з клінічними подіями та кількісними функціональними показниками (наприклад, оцінкою якості життя, результатами тесту з 6-хвилинною ходьбою, біомаркерами ушкодження міокарда тощо) за допомогою заздалегідь заданої ієрархічної системи пріоритетів [44]. Вважається, що цей підхід, наприклад, добре підходить для оцінки КТ у дослідженнях фази II і дає змогу уникнути непоодиноких розбіжностей у результатах між цією фазою та дослідженнями фази III. Йдеться про випадки, коли дослідження фази II, наприклад, показує поліпшення симптомів або зменшення вираженості застійних явищ під дією досліджуваної терапії, але ці зміни не трансформуються в позитивні результати після завершення дослідження фази III. Одна з можливих гіпотез, що пояснюють цю розбіжність, полягає в тому, що поліпшення симптомів або полегшення застійних явищ може компенсуватися розвитком непередбачених наслідків, таких як ушкодження нирок або міокарда [45]. Вважається, що використання підходу комплексного ранжування в дослідженнях фази II зможе забезпечити більшу узгодженість результатів між різними фазами програми розробки препаратів [4]. Комбіновані кінцеві точки (ККТ). ККТ (наприклад, популярна ККТ «смерть або ГСН») зазвичай однаковою мірою враховують усі складові ККТ, хоча лікарі та пацієнти можуть вважати дуже різною значущість кожного з цих компонентів. Водночас, оскільки несмертельні події, як правило, трапляються частіше, ніж випадки смерті, менш тяжкі наслідки (наприклад, госпіталізації) схильні до сильнішого впливу на частоту ККТ, ніж менш часті, але тяжчі наслідки (наприклад, смерть). Тому, хоча використання ККТ сприяє збільшенню частоти досліджуваних подій, у таких ситуаціях буває складно оцінити однорідність ефекту лікування на всі складові ККТ, зокрема зрозуміти, чи не зумовлений спостережуваний ефект лікування здебільшого впливом на більш поширений, але менш серйозний компонент ККТ (такий як ГСН у наведеному прикладі з ККТ «смерть або ГСН»). Додаткова проблема виникає при використанні ККТ у поєднанні з аналізом часу до розвитку першої події ККТ, який використовують у більшості довгострокових досліджень, що спостерігають за учасниками до першої події ККТ. У результаті менш серйозна подія, що сталася на більш ранньому етапі дослідження (наприклад, короткочасна ГСН), ураховується, а більш важка подія (наприклад, смерть), що сталася пізніше у цього ж учасника, буде цензурована в первинному аналізі результатів дослідження [44]. До того ж, у такому аналізі більш рання, але менш тяжка подія може розглядатися як гірший результат, ніж більш пізня, але більш серйозна подія, результатом чого стає ситуація, коли під час аналізу часу до ККТ «смерть або ГСН» результат лікування учасника, якого госпіталізували через 2 тижні після рандомізації з приводу СН, а потім він почував себе добре впродовж 5 років, буде розглядатися як гірший, ніж результат учасника, який помер через 2 місяці після рандомізації. І така оцінка очевидним чином суперечить оцінці клінічного перебігу захворювання з точки зору пацієнтів і лікарів. Щоб подолати цю проблему, наразі для реєстрації та аналізу ККТ часто вдаються до концепції «співвідношення перемог і поразок» (win ratio), яка дає змогу присвоїти різні рівні важливості різним компонентам ККТ [44]. Цей підхід передбачає складання відповідних пар пацієнтів і розрахунок бала на основі попарних порівнянь отриманих результатів [46]. Розглянемо цей підхід на прикладі ККТ «СС смерть і ГСН» (типова первинна КТ у дослідженнях СН). Для аналізу результатів такого дослідження з групи досліджуваного препарату й групи контрольного лікування складають відповідні пари учасників, у яких кожен учасник позначається як «переможець» або «переможений», залежно від того, хто з них першим помер від СС причини. Якщо обидва учасникі живі, поділ на «переможця» і «переможеного» відбувається з урахуванням того, хто перший був госпіталізований з приводу СН. Якщо обидва учасники вижили й не мали ГСН упродовж періоду спостереження, ситуація розцінюється як «нічия». Коефіцієнт виграшу (win ratio) розраховується як загальна кількість «переможців», поділена на загальну кількість «переможених» [4]. КТ, що враховують клінічний статус пацієнтів. Попри те, що смертність залишається традиційною КТ, результати оцінки якої край важливі для схвалення нових методів лікування органами охорони здоров’я, велике значення має також думка пацієнта, згідно з якою значущість кількості прожитих років може зменшуватись, якщо в пацієнта поганий клінічний статус, знижені функціональні можливості та низька якість життя [47]. Іноді пацієнт може надати перевагу нейтральному або навіть невеликому негативному впливу терапії на виживаність, якщо вона забезпечить йому більшу функціональність і більше якісне життя [48, 49]. З огляду на ці міркування в деяких дослідженнях СН використовували ККТ, що враховують клінічний статус пацієнтів. Водночас слід зазначити, що оцінка клінічного статусу є складним завданням у зв’язку з високою мінливістю і суб’єктивністю цих оцінок, а також їхньою залежністю від різноманітних супутніх захворювань. Проте існують так звані опитувальники для оцінювання якості життя, які містять оцінку різних варіантів фізичної активності, а також емоційних, функціональних і когнітивних порушень, наприклад спеціальні опитувальники для хворих на СН, зокрема KCCQ і Міннесотський опитувальник для оцінювання якості життя із СН, які можуть бути корисними й застосовуються в клінічних дослідженнях [4]. Сукупна клінічна оцінка. У випадку СН ця оцінка об’єднує жорсткі клінічні КТ, такі як смерть і госпіталізація, з функціональним класом за NYHA, результатами глобальної оцінки захворювання пацієнтом (яка проводиться особисто пацієнтом без участі лікаря), а також може містити оцінку ступеня полегшення симптомів і зміни рівнів біомаркерів. Сукупна клінічна оцінка зазвичай використовується для зменшення об’єму вибірки й всебічного вивчення результатів дослідження і дає змогу мінімізувати кількість рандомізованих учасників, виключених з дослідження у зв’язку з погіршенням стану або посиленням симптомів [4].
Перспективи використання КТ у майбутніх дослідженнях СН Відповідний вибір правильних КТ дає змогу розробити й впровадити методи лікування з результатами, значущими для пацієнтів і лікарів, а тому має вирішальне значення в клінічних дослідженнях СН. Нині для цієї мети використовують переважно КТ ефективності, що відображають загальну смертність і захворюваність та/або смертність від конкретних причин. Ці КТ вважаються надійними з наукової точки зору, оскільки дають змогу проводити об’єктивні, точні та відтворювані вимірювання, використовуючи стандартизовані визначення, з мінімальною похибкою або спотворенням. Однак ці КТ не повною мірою задовольняють вимогу значущості і для пацієнтів, і для медичних працівників, оскільки трапляються ситуації, коли хворі з важкою стадією СН, із вираженим обмеженням функціональних можливостей або госпіталізовані пацієнти можуть віддати перевагу якості життя перед її кількістю (тобто терапії, яка покращує симптоми захворювання, функціональні можливості та якість життя без значного ефекту на захворюваність і смертність). Утім, незважаючи на широке визнання важливості усунення симптомів, відновлення функцій і поліпшення якості життя як цілей лікування СН, наразі лише дуже невелика кількість препаратів схвалена для полегшення симптомів гострої або хронічної СН [4]. Оскільки КТ мають бути адаптовані до потреб досліджуваної популяції, результати, про які повідомляють пацієнти, самі по собі або в поєднанні з показниками функціонального статусу можуть бути вельми актуальними, особливо для пацієнтів із більш пізніми стадіями захворювання. Загалом, вкрай важливо зосередити увагу на розробці методів лікування, які допоможуть пацієнтам жити довше, поліпшити симптоми і якість життя, при цьому будуть спрямовані на досягнення цілей пацієнтів і лікарів, одночасно враховуючи вимоги регулюючих органів і очікування спонсорів досліджень [4]. Вище йшлося про нещодавній документ FDA, згідно з яким поліпшення пацієнторієнтованих результатів, що відображають сприйняття хворим свого здоров’я (симптоми, функціональний статус, фізичні функції, якість життя), навіть без демонстрації сприятливого впливу на виживаність і частоту госпіталізацій, може бути основою для схвалення нових методів лікування СН. Цей документ дуже важливий, оскільки очікується, що він сприятиме розробленню методів лікування СН, які впливають на всі значущі КТ і відповідають мінливим потребам пацієнтів. Слід підкреслити, що попри відсутність необхідності доводити, що спрямований на полегшення симптомів новий препарат покращує показники виживаності й захворюваності, вимога до дослідників і спонсорів виключити ризики несприятливого впливу досліджуваної терапії на смертність пацієнтів, щоб встановити межі безпеки, зберігається [4]. До важливих завдань, покликаних підвищити якість клінічних досліджень, прискорити процедуру схвалення необхідних препаратів і, в остаточному підсумку, поліпшити результати лікування пацієнтів із СН, також належать розробка надійних методів реєстрації інших наслідків СН, окрім ГСН або смерті, разом зі стратегіями, що дають змогу зменшити варіабельність і підвищити точність винесення рішень, а також розробка валідованих і стандартизованих інструментів оцінювання результатів, про які повідомляють пацієнти, особливо інструментів для самостійного застосування [4].
Висновки У представленому огляді коротко описано процес еволюції кінцевих точок, які використовуються в дослідженнях методів лікування СН. Як показує аналіз доступних даних, метою більшості сучасних великих досліджень у цій популяції пацієнтів досі залишається демонстрація позитивного впливу досліджуваної терапії на жорсткі клінічні кінцеві точки, зокрема на смертність і госпіталізацію з приводу СН. Крім того, дуже часто використовують метод оцінювання часу до першої події комбінованої кінцевої точки (що знижує цінність результатів аналізу, з якого виключено подальші та повторні події), а також комбіновані кінцеві точки, у яких, на відміну від реальної практики, усі компоненти мають однакову вагу. Проте в підходах до проведення досліджень при СН так само намітилася низка позитивних змін. По-перше, це розширення кінцевої точки «госпіталізація з приводу СН», до якої, з огляду на пов’язане зі зміною моделі надання медичної допомоги зменшення кількості госпіталізацій, тепер входять звернення по екстрену або невідкладну допомогу у зв’язку із СН і потреба у в/в терапії діуретиками. По-друге, це розробка методів зважування відносної важливості подій у складі комбінованих результатів, які, проте, потребують поліпшення, щоб виключити можливе «маскування» збільшення смертності зниженням захворюваності або частоти госпіталізацій у складі комбінованої кінцевої точки. По-третє, дедалі ширше визнають, що з огляду на пов’язаний із СН великий тягар симптомів і функціональних обмежень, критично важливо використовувати кінцеві точки у вигляді результатів, про які повідомляють пацієнти, показників якості життя і функціональних можливостей пацієнтів. Відповіддю на цю потребу стала нещодавня зміна підходу в нормативних настановах FDA з дозволом використовувати показники функціонального статусу або якості життя для схвалення методів лікування СН за результатами клінічних досліджень. Загалом, для збору доказів ефективності нових методів терапії, необхідних для реалізації потреб хворих на різних стадіях СН, і, зрештою, для поліпшення результатів лікування, потрібні спільні зусилля всіх зацікавлених сторін, включно з лікарями, вченими, спонсорами, виробниками, регулювальними органами, страховими компаніями й спільнотами пацієнтів.
Список літератури знаходиться в редакції
Автор огляду Галина Мілюхина Medicine Review 2024; 3 (76): 22 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2025. Усі права захищені.
|
мапа сайту корисні посилання |