Оцінка результатів переходу на монотерапію тикагрелором у пацієнтів після ЧКВ залежно від анамнезу АКШ: огляд дослідження TWILIGHT-CABGДля пацієнтів, які раніше перенесли аортокоронарне шунтування (АКШ), характерний ризик прогресування ішемічної хвороби серця (ІХС) і подальшої дисфункції коронарного шунта [1]. Літній вік, наявність множинних супутніх захворювань і анатомічно складної ІХС можуть ускладнювати проведення повторної коронарної реваскуляризації. Отже, останніми роками дедалі частіше проводять не повторну операцію АКШ, а (за сприятливої коронарної анатомії) черезшкірне коронарне втручання (ЧКВ) [2, 3]. Проте, ЧКВ, проведене після попереднього АКШ, пов’язане з гіршими довгостроковими результатами порівняно з пацієнтами без попереднього АКШ, особливо в разі ЧКВ на коронарному шунті [4–6], що, імовірно, пояснюється як патофізіологією шунта, так і загалом складністю стану пацієнта. У зв’язку із цим великого значення набуває вибір препаратів для подальшого лікування пацієнтів після процедури ЧКВ. Стандартом профілактики ішемічних подій після ЧКВ наразі є річна подвійна антитромбоцитарна терапія (ПАТ) комбінацією ацетилсаліцилової кислоти (АСК) та інгібітора P2Y12-рецепторів тромбоцитів (іP2Y12) [7]. Водночас про оптимальну антитромбоцитарну терапію після ЧКВ у пацієнтів, які раніше перенесли АКШ, відомо дуже мало, хоча й були отримані дані про те, що потужніші іP2Y12 тикагрелор і прасугрел можна розглядати як альтернативну антиагрегантну стратегію для зниження ризику тромбоутворення в пацієнтів після АКШ, а також про те, що монотерапія іP2Y12 є ефективною стратегією запобігання кровотечам серед пацієнтів із групи високого ризику. У зв'язку із цим інтерес становлять результати дослідження TWILIGHT (Ticagrelor With Aspirin or Alone in High-Risk Patients After Coronary Intervention), що включало пацієнтів після ЧКВ, як тих, хто раніше проходив, так і тих, хто не проходив АКШ, і показало, що перехід на монотерапію тикагрелором після 3 місяців ПАТ знижує ризик кровотеч, не підвищуючи ризик ішемічних подій, порівняно з подальшим продовженням ПАТ [8]. Нещодавно Sardella et al. опублікували результати апостеріорного аналізу даних із дослідження TWILIGHT, що порівнює результати досліджуваного лікування в підгрупах пацієнтів з АКШ і без АКШ в анамнезі (дослідження TWILIGHT-CABG) [9]. Основна інформація про цей аналіз стисло подана в цій статті.

Методологія дослідження TWILIGHT і аналізу TWILIGHT-CABG TWILIGHT було рандомізованим подвійним сліпим плацебо-контрольованим дослідженням, яке проводили в 187 дослідницьких центрах в 11 країнах із липня 2015 по липень 2019 року. У це дослідження зараховували пацієнтів, які успішно пройшли ЧКВ зі встановленням щонайменше одного стента з лікарським покриттям, мали щонайменше один клінічний і щонайменше один ангіографічний критерій високого ризику ішемії або кровотечі та під час виписки отримували ПАТ комбінацією тикагрелору й АСК. Клінічні критерії високого ризику включали вік 65 років і понад, жіночу стать, наявність тропонін-позитивного гострого коронарного синдрому (ГКС), підтверджене судинне захворювання, цукровий діабет (ЦД), що вимагає медикаментозної терапії, і хронічну хворобу нирок (ХХН) із розрахунковою швидкістю клубочкової фільтрації <60 мл/хв/1,73 м2. Ангіографічні критерії високого ризику охоплювали багатосудинну ІХС, загальну довжину стента понад 30 мм, тромбоз у ділянці цільового ураження, втручання на біфуркації коронарної артерії зі встановленням щонайменше двох стентів, обструктивне ураження лівої коронарної артерії або проксимальної лівої передньої низхідної коронарної артерії та використання атеректомії внаслідок кальцинозу цільового ураження. До участі в дослідженні не допускали пацієнтів з інфарктом міокарда (ІМ) із підйомом сегмента ST, кардіогенним шоком, інсультом в анамнезі, хворих із показаннями до застосування пероральних антикоагулянтів або протипоказаннями до призначення АСК чи тикагрелору. Упродовж перших трьох місяців після індексного ЧКВ учасники дослідження отримували тикагрелор (90 мг 2 рази на день) і АСК у кишковорозчинній оболонці (81–100 мг/ добу) у відкритому режимі. Потім пацієнти, які успішно застосовували ПАТ протягом 3 місяців без розвитку серйозних кровотеч або ішемічних подій, були рандомізовані в співвідношенні 1:1 для застосування АСК або плацебо на додаток до подальшого відкритого лікування тикагрелором протягом ще 12 місяців (група продовження ПАТ і група монотерапії тикагрелором відповідно). Первинною кінцевою точкою TWILIGHT була перша кровотеча 2, 3 або 5 типу за класифікацією Консорціуму з вивчення кровотеч (Bleeding Academic Research Consortium, BARC), що розвинулася протягом 12 місяців після рандомізації. Ключовою вторинною ішемічною кінцевою точкою була комбінація ІМ, інсульту й смерті від будь-якої причини. Вторинні геморагічні кінцеві точки включали кровотечу типу 3 або 5 за BARC, велику кровотечу за класифікацією Thrombolysis in Myocardial Infarction (TIMI), помірну, тяжку або загрозливу для життя кровотечу за класифікацією Global Utilization of Streptokinase and Tissue Plasminogen Activator for Occluded Coronary Arteries (GUSTO), а також велику кровотечу за визначенням Міжнародного товариства тромбозів і гемостазу (International Society of Thrombosis or Haemostasis, ISTH). Для свого аналізу Sardella et al. розділили учасників дослідження TWILIGHT за підгрупами з урахуванням статусу попереднього АКШ. Початкові й клінічні характеристики узагальнювали у вигляді середніх значень для безперервних змінних, а також у вигляді абсолютної та відносної (відсотки) кількості – для категоріальних змінних. Крім порівняння результатів монотерапії тикагрелором і лікування комбінацією АСК + тикагрелор залежно від статусу АКШ, серед пацієнтів, які раніше перенесли АКШ, було проведено пошуковий аналіз для оцінювання ефектів лікування залежно від типу цільової судини (тобто ЧКВ на нативній коронарній судині порівняно з ЧКВ на венозному або артеріальному шунті). Геморагічні й ішемічні наслідки оцінювали у вибірці рандомізованих пацієнтів і у вибірці, що виконала вимоги протоколу, відповідно. Для оцінки сукупної частоти первинної та вторинних кінцевих точок і обчислення різниці абсолютних ризиків (РАР) кровотеч і ішемічних подій із 95% довірчими інтервалами (ДІ) використовували метод Каплана-Мейєра. При оцінці зв'язку статусу попереднього АКШ із геморагічними й ішемічними наслідками використовували багатоваріантну модель пропорційного ризику Кокса із розрахунком відношень ризиків (ВР) і 95% ДІ. Результати коригували з урахуванням таких чинників, як вік, стать, ЦД, ХХН, артеріальна гіпертензія, гіперхолестеринемія, статус куріння і хвороба периферичних артерій. На статистичну значущість виявлених відмінностей вказували значення р<0,05.
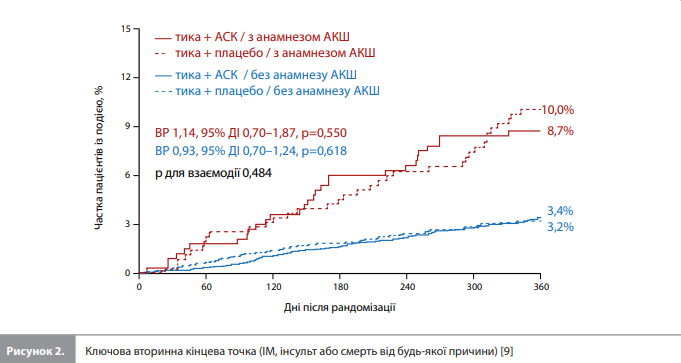
Результати аналізу TWILIGHT-CABG У дослідження було включено загалом 9006 пацієнтів, які перенесли ЧКВ, із них 7119 через три місяці після ЧКВ були рандомізовані в групи терапії комбінацією тикагрелор + плацебо (монотерапія тикагрелором) або тикагрелор + АСК (продовження ПАТ). До аналізу Sardella et al. увійшов 6531 пацієнт (587 учасників було виключено через нормативні причини, і 1 пацієнт – через відсутність даних про статус АКШ), із них 703 (10,8%) пацієнти раніше перенесли АКШ, а у 5828 (89,2%) не було анамнезу АКШ. Пацієнти, які перенесли АКШ, були старшими, частіше були європеоїдами й чоловіками, вирізнялися вищою поширеністю майже всіх вихідних супутніх захворювань, у тому числі ЦД і ХХН, перенесли в минулому більше ІМ і процедур ЧКВ, частіше мали діагноз стабільної ІХС і потребували складної процедури ЧКВ порівняно з пацієнтами без анамнезу АКШ (табл. 1). Усі пацієнти з анамнезом АКШ (100%) пройшли ЧКВ на нативних коронарних судинах, водночас у 132 із них (18,8%) додатково проводили ЧКВ на шунті з підшкірної вени й у 30 (4,3%) – ЧКВ на артеріальному шунті (табл. 1) [9]. Групи лікування були добре збалансовані за вихідними і процедурними характеристиками. Цікаво, що за даними за 12 місяців після рандомізації пацієнти, які раніше пройшли АКШ, вирізнялися меншою прихильністю до лікування тикагрелором (72,2 vs 83,1%, p<0,001) і приймання АСК / плацебо (79,9 vs 86,6%, p<0,001) порівняно з учасниками без анамнезу АКШ [9]. Геморагічні наслідки. Первинна кінцева точка – кровотеча 2, 3 або 5 типу за BARC – загалом частіше реєструвалася в підгрупі пацієнтів із попереднім АКШ порівняно з пацієнтами без АКШ в анамнезі (7,2 vs 5,2%, ВР 1,38, 95% ДІ 1,02–1,87, p=0,036), однак після багатофакторного коригування ці відмінності втрачали статистичну значущість (скориговане ВР 1,32, 95% ДІ 0,96–1,82, p=0,082). Кровотечі 3 або 5 типу за BARC також частіше розвивалися в пацієнтів, які перенесли АКШ. Кровотечі 2, 3 або 5 типу за BARC виникали значно рідше в групі монотерапії тикагрелором порівняно з групою продовження ПАТ як серед пацієнтів з АКШ в анамнезі (4,9 vs 9,6%, ВР 0,50, 95% ДІ 0,28–0,90, p=0,02; РАР -4,7%, 95% ДІ від -8,6% до -0,8%), так і серед пацієнтів без анамнезу АКШ (3,8 vs 6,6%, ВР 0,57, 95% ДІ 0,45–0,72, p<0,01) без ознак залежності терапевтичного ефекту від статусу АКШ (p для взаємодії 0,676) (рис. 1) [9]. Аналогічно великі кровотечі (3 або 5 типу за BARC) виникали значно рідше в групі монотерапії тикагрелором порівняно з групою продовження ПАТ як серед пацієнтів з АКШ в анамнезі (1,1 vs 4,5%, ВР 0,25, 95% ДІ 0,08–0,76, p=0,015; РАР -3,3%, 95% ДІ від -5,8 до -0,9%), так і серед пацієнтів без анамнезу АКШ (0,9 vs 1,7%, ВР 0,54, 95% ДІ 0,34–0,88, p=0,012). Монотерапія тикагрелором також була пов’язана зі значним зниженням ризику інших вторинних геморагічних кінцевих точок порівняно з продовженням ПАТ [9].
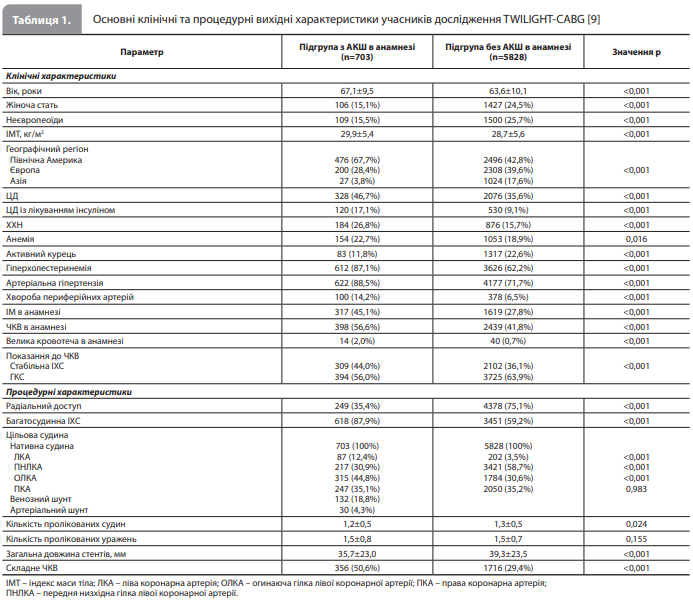
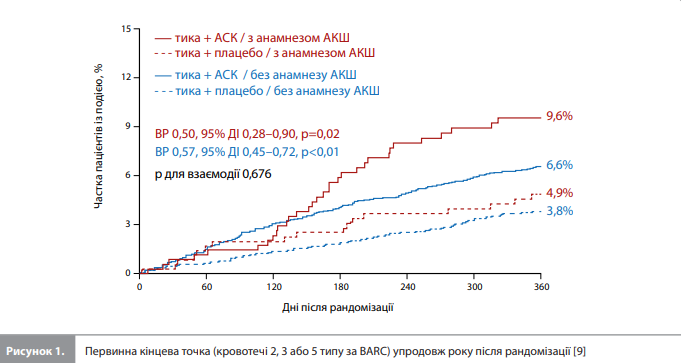
Ішемічні наслідки. Ключова вторинна ішемічна комбінована кінцева точка – комбінація ІМ, інсульту й смерті від будь-якої причини – загалом частіше реєструвалася в пацієнтів з АКШ в анамнезі порівняно з пацієнтами без анамнезу АКШ (9,4 vs 3,3%, скориговане ВР 2,20, 95% ДІ 1,63–2,98, p<0,001), як і комбінація ІМ, ішемічного інсульту й смерті від серцево-судинних (СС) причин. Водночас показники частоти реєстрації цієї кінцевої точки на тлі монотерапії тикагрелором і продовження ПАТ були зіставними як серед пацієнтів, які раніше перенесли АКШ (10,0 vs 8,7%, ВР 1,14, 95% ДІ 0,70–1,87, p=0,550, РАР 1,3%, 95% ДІ від -3,0 до 5,7%), так і серед пацієнтів без анамнезу АКШ (3,2 vs 3,4%, ВР 0,93, 95% ДІ 0,70–1,24, p=0,618) без ознак взаємодії між ефектом лікування і статусом АКШ (p для взаємодії 0,484) (рис. 2) [9]. Аналогічна картина спостерігалася при аналізі ефектів терапії залежно від статусу АКШ для комбінації ІМ, ішемічного інсульту й смерті від СС причин, її компонентів та інших ішемічних кінцевих точок [9]. Пошуковий аналіз з урахуванням типу цільової судини показав, що величина ефекту монотерапії тикагрелором на первинну кінцеву точку (кровотечі 2, 3 або 5 типу за BARC) порівняно з продовженням ПАТ була однаковою при втручаннях на шунтах і нативних коронарних артеріях (p для взаємодії 0,998), аналогічний результат було отримано для інших геморагічних кінцевих точок, а також для всіх ішемічних наслідків, включно з ключовою вторинною ішемічною кінцевою точкою (комбінація ІМ, інсульту й смерті від будь-якої причини) [9].
Обговорення і висновки Отже, можна окреслити такі основні результати апостеріорного аналізу дослідження TWILIGHT, проведеного Sardella et al. для порівняння ефектів монотерапії тикагрелором і продовження ПАТ у пацієнтів з АКШ в анамнезі та без анамнезу АКШ (табл. 2) [9]: 1. Раніше перенесене АКШ пов'язане з підвищеним ризиком великих кровотеч та ішемічних подій порівняно з пацієнтами без анамнезу АКШ. 2. Монотерапія тикагрелором зменшувала частоту розвитку кровотеч порівняно з продовженням ПАТ, не збільшуючи при цьому частоти ішемічних подій, незалежно від статусу АКШ. 3. Переваги скасування АСК після 3-місячної ПАТ порівняно з продовженням ПАТ зберігалися для всіх ішемічних і геморагічних кінцевих точок незалежно від судини, на якій виконували ЧКВ (нативна судина vs коронарний шунт). З огляду на характер дослідження TWILIGHT-CABG (апостеріорний аналіз даних дослідження TWILIGHT) отримані результати розповсюджуються лише на пацієнтів, які відповідають характеристикам учасників дослідження TWILIGHT, відносяться лише до антиагрегантної терапії на основі тикагрелору та, загалом, мають розглядатись як дані, що генерують гіпотези, й перевірятися в подальших добре організованих дослідженнях.

Висновки Незважаючи на підвищений ризик кровотеч та ішемічних подій після ЧКВ у пацієнтів, які раніше перенесли АКШ, перехід на монотерапію тикагрелором після 3-місячної ПАТ, за даними Sardella et al., дає змогу знизити ризик клінічно значущих кровотеч без збільшення ризику ішемічних подій порівняно з продовженням ПАТ до 15-го місяця після ЧКВ незалежно від статусу АКШ. Ці дані підтверджують, що монотерапія тикагрелором є безпечною стратегією профілактики кровотеч, яку можна розглядати після ЧКВ у пацієнтів із групи високого ішемічного ризику, котрі раніше перенесли АКШ.
Список літератури знаходиться в редакції
Автор огляду Наталія Генш Medicine Review 2024; 3 (76): 5 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2026. Усі права захищені.
|
мапа сайту корисні посилання |