Настанова Європейського товариства кардіологів щодо профілактики й ведення серцево-судинних захворювань у пацієнтів із цукровим діабетом (2023): стислий огляд основних положеньОднією з настанов, представлених Європейським товариством кардіологів (ESC) на щорічному конгресі кардіологів у серпні 2023 р., став документ, присвячений цукровому діабету (ЦД), переддіабету й серцево-судинним (СС) захворюванням (ССЗ), який підготували спільно експерти ESC та Європейської асоціації з вивчення ЦД (EASD). Це другий збірник рекомендацій на тему ЦД, переддіабету й ССЗ, перший був опублікований 2007 року. Суттєве зростання поширеності ЦД, відкриття нових зв’язків між ЦД і ССЗ, а також поява нових лікарських препаратів, які одночасно реалізують як протидіабетичні, так і СС ефекти, разом із накопиченням значного обсягу наукової та практичної інформації з експериментальних, клінічних досліджень і аналізів баз даних – усе це стало підставою для розроблення оновленої редакції настанови. Основні положення документа представлені нижче [1].
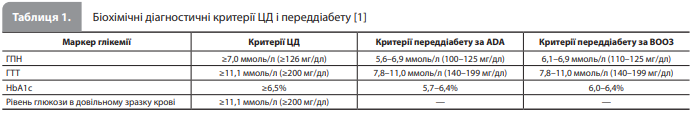
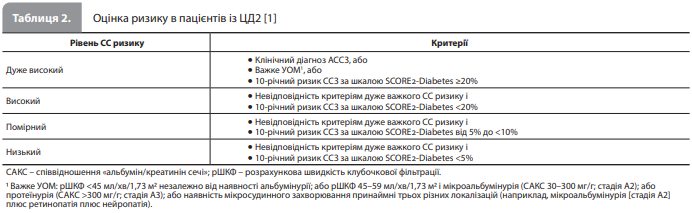
Порушення вуглеводного обміну й ССЗ Головною зміною в рекомендаціях із діагностики ЦД є визнання підвищеного рівня глікованого гемоглобіну A1c (HbA1c) валідним діагностичним критерієм ЦД. Це стало можливим завдяки проведенню високоякісних епідеміологічних досліджень, а також аналізу даних із 73 клінічних досліджень за участю 294 998 пацієнтів без встановленого діагнозу ЦД, який показав, що HbA1c не поступається рівню глюкози в плазмі натщесерце (ГПН), результату вимірювання рівня глюкози в довільно взятому зразку або результату глюкозотолерантного тесту (ГТТ), або навіть перевершує ці показники в прогнозуванні СС ризику [2]. Згідно з новими рекомендаціями ESC, рівень HbA1c ≥6,5% є діагностичною ознакою ЦД, а рівень 5,7 (6,0) – 6,4% – діагностичною ознакою переддіабету. Слід зазначити, що одноразове сумісне виявлення значень HbA1c і ГПН у діабетичному діапазоні вважається достатнім для постановки діагнозу ЦД навіть у пацієнтів без симптомів гіперглікемії. Однак, якщо ці два показники не узгоджуються, слід повторити той аналіз, який показав результат у діабетичному діапазоні, або краще провести ГТТ, який залишається золотим стандартом діагностики ЦД у спірних випадках. Критерії, які використовують для діагностики ЦД і переддіабету, узагальнено в таблиці 1 (для переддіабету представлено два набори критеріїв – від Американської асоціації з вивчення ЦД [ADA] і від Всесвітньої організації охорони здоров'я [ВООЗ]) [1]. У розділі, присвяченому класифікації ЦД, стисло представлено основні форми захворювання, включно з ЦД 1 типу, ЦД 2 типу (ЦД2), моногенним, вторинним і гестаційним ЦД, а також згадано, що більшість хворих на ЦД2 не мають симптомів гіперглікемії, що призводить до пізнього виявлення захворювання на стадії розвитку СС ускладнень і вказує на важливість скринінгу на ЦД для всіх пацієнтів із ССЗ. Також описується стан, відомий як стресова гіперглікемія, який часто спостерігається в госпіталізованих пацієнтів, зокрема у хворих із гострим коронарним синдромом (ГКС) або серцевою недостатністю (СН). Експерти нагадують, що наявність стресової гіперглікемії, навіть за відсутності ЦД, пов'язана з несприятливими внутрішньолікарняними наслідками й має підозрюватися в осіб із підвищеним рівнем ГПН за нормального рівня HbA1c. Таким пацієнтам для виключення ЦД або переддіабету показаний ГТТ, який потрібно провести за кілька тижнів після виписки зі стаціонару (результати деяких досліджень підтримують проведення ГТТ перед випискою, однак, на думку експертів ESC, на даний час даних для такої рекомендації недостатньо) [1]. Щодо скринінгового обстеження на ЦД слід зазначити, що ані універсальних критеріїв тестування, ані комплексної глобальної програми скринінгу наразі ще не розроблено. Загалом загальновизнано, що за відсутності ССЗ особам, які входять до груп високого ризику (тобто люди з надмірною вагою/ожирінням або ознаками резистентності до інсуліну), слід регулярно проходити скринінг на ЦД, особливо після 45 років. Крім того, ADA розробила відносно просту 7-бальну систему оцінювання, що враховує вік, стать, масу тіла, фізичну активність, наявність артеріальної гіпертензії (АГ), а також особистий анамнез гестаційного діабету та сімейний анамнез ЦД, із рекомендацією всім особам з оцінкою ≥5 балів пройти обстеження на ЦД. У популяції хворих на ССЗ поширеність ЦД істотно зростає, при цьому наявність ЦД призводить до гірших клінічних результатів порівняно з хворими на ССЗ і нормальним метаболізмом глюкози. Тому всі хворі з атеросклеротичними ССЗ (АССЗ), СН та/або фібриляцією передсердь (ФП), особливо госпіталізовані у зв'язку з гострою подією, мають бути обстежені на ЦД за допомогою аналізів на HbA1c та/або ГПН (пам'ятаючи про їхню роль як сильніших предикторів СС ускладнень порівняно з ГТТ), а також (у сумнівних ситуаціях) ГТТ [1]. Водночас, наявність ЦД, особливо ЦД2, значно (у 2–4 рази) підвищує ризик розвитку ССЗ, включно з ішемічною хворобою серця (ІХС), інсультом, СН, ФП і хворобою периферичних артерій, упродовж життя пацієнта, що робить украй важливим оцінювання СС ризику в осіб із ЦД. Результатом оцінки СС ризику в осіб із ЦД2 має бути віднесення пацієнта до однієї з чотирьох категорій ризику: дуже високий, високий, помірний або низький ризик (табл. 2) [1], при цьому беруть до уваги особистий і сімейний анамнез, симптоми, результати фізикального обстеження та лабораторних аналізів, наявність АССЗ або тяжкого ураження органів-мішеней (УОМ), а також оцінку за шкалою SCORE2-Diabetes (розробленою для оцінювання 10-річного ризику смертельних і несмертельних ССЗ у пацієнтів із ЦД віком від 40 років і понад без АССЗ і тяжкого УОМ) [1]. Порогові рівні оцінок ризику, що наведені в таблиці 2, призначені для використання в якості орієнтирів під час спільного з пацієнтом ухвалення рішень щодо необхідності збільшення інтенсивності лікування та застосування додаткових заходів із профілактики АССЗ (включно з призначенням ліпідознижувальної терапії, інгібіторів натрійзалежного котранспортера глюкози 2 типу [іНЗКТГ2] або агоністів рецепторів глюкагоноподібного пептиду 1 типу [АР ГПП–1]) [1].
Профілактика ССЗ у пацієнтів із ЦД Зміна способу життя. Серед вказівок щодо модифікації способу життя дотримання дієти зберігає свою значущість, однак оновлені рекомендації щодо харчування вирізняються набагато більшою гнучкістю: у них більше не йдеться про дотримання суворих вимог щодо кількості калорій, які надходять в організм з основними макронутрієнтами, натомість особлива увага приділяється відповідному споживанню енергії, адаптованому до потреб кожного пацієнта, та дієті, яка ґрунтується на фруктах, овочах, злаках, джерелах білка з низьким вмістом жирів та обмеженому споживанню насичених і транснасичених жирних кислот. На особливу увагу заслуговують результати дослідження PREDIMED, які показали, що середземноморська дієта, збагачена оливковою олією або горіхами, пов'язана з більш низькою частотою розвитку АССЗ (зниження ризику на 28–31%) у пацієнтів із групи високого СС ризику, серед яких 49% мали ЦД [3]. Решта рекомендацій щодо харчування, включно із вказівками щодо загальної кількості споживаних вуглеводів (загалом і за категоріями), обмеження споживання солі та збільшення споживання клітковини, загалом залишилися без змін, як і рекомендації щодо фізичних навантажень (регулярні прогулянки, вправи з обтяженням і вправи на витривалість з оптимальною тривалістю щонайменше 150 або 75 хвилин на тиждень для помірних чи інтенсивних навантажень відповідно) та куріння (відмова від куріння, зокрема й за допомогою фармакологічної підтримки) [1]. Контроль рівня глікемії. Підкресливши, що розвитку ССЗ у людей із ЦД найкраще запобігати за допомогою жорсткого контролю всіх чинників СС ризику, експерти ESC постаралися дати рекомендації за двома дуже важливими напрямами: цільові показники глікемії і вибір протидіабетичних препаратів (ПДП). 1. Цільові показники глікемії, досягнення яких дає змогу запобігти розвитку ССЗ та їхніх ускладнень. Відомо, що зниження рівня HbA1c знижує ризик мікросудинних ускладнень, особливо за досягнення значень, близьких до нормального значення показника (HbA1c <7%), проте зв'язок між рівнем HbA1c і макросудинними ускладненнями є більш складним. Зокрема, незважаючи на існування подібного зв'язку, результати досліджень, у яких оцінювали ефект жорсткого контролю глікемії на запобігання СС подій, показали суперечливі результати, а наглядові дослідження виявили U-подібний зв'язок між рівнем HbA1c і клінічними наслідками, показавши, що у випадку з рівнем HbA1c «нижчий – не завжди кращий». Отже, рекомендації, подані з урахуванням усіх доступних даних, вказують на необхідність прагнути рівня HbA1c <7% для зниження ризику мікросудинних ускладнень, уникати гіпоглікемічних епізодів, особливо в осіб зі встановленими ССЗ, персоналізувати цільове значення для HbA1c з урахуванням супутніх захворювань, тривалості ЦД та очікуваної тривалості життя (цільове HbA1c при короткій очікуваній тривалості життя – <8,5%) [1]. 2. Вибір ПДПдля зниження ризику АССЗ. У цьому розділі настанови всі ПДП, які застосовують у даний час, були розділені на три основні групи: ПДП із СС ефективністю, продемонстрованою в спеціальних дослідженнях з оцінкою СС наслідків – ДОССН (іНЗКТГ2, АР ГПП-1 і піоглітазон), ПДП, безпечні для СС системи, але без СС ефективності, продемонстрованої в спеціальних ДОССН (інгібітори дипептидилпептидази-4, ексенатид, ліксисенатид, інсулін, глімепірид), і старі ПДП, які не вивчалися в спеціальних ДОССН (метформін, препарати сульфонілсечовини). При цьому в настанові представлено нову рекомендацію, згідно з якою під час призначення ПДП перевагу слід надавати ПДП із доведеною СС ефективністю, на другому місці йдуть ПДП із доведеною СС безпекою і тільки потім – ПДП, для яких СС ефективність і безпеку не було доведено в спеціальних дослідженнях (ДОССН). Метааналіз шести спеціальних ДОССН, які вивчали ефекти іНЗКТГ2 у пацієнтів із ЦД, підтвердив зниження ризику великих несприятливих СС подій (МАСЕ), включно із СС смертю, інсультом та інфарктом міокарда (ІМ), на тлі застосування цих препаратів (відношення ризиків [ВР] 0,90, 95% довірчий інтервал [ДІ] 0, 85–0,95) і показав, що найбільш виражений і стабільний СС ефект іНЗКТГ2 пов'язаний зі зниженням ризику госпіталізації з приводу СН – ГСН (ВР 0,68, 95% ДІ 0,61–0,76), при цьому вплив іНЗКТГ2 на СС кінцеві точки не залежав від наявності діагностованого АССЗ (р для взаємодії між ефектом і діагностованим АССЗ 0,63 – для МАСЕ і 0,26 – для ГСН) [4]. Аналогічний метааналіз семи ДОССН, що проводили із застосуванням АР ГПП-1 у пацієнтів із ЦД2 та АССЗ/високим ризиком АССЗ, показав зниження ризику МАСЕ на 15% (ВР 0,85, 95% ДІ 0,80–0,90), а також значне зниження ризику СС смерті на 15%, ІМ – на 12%, інсульту – на 19% і ГСН – на 12% порівняно з плацебо [5]. СС ефект АР ГПП-1 був дещо більш вираженим у пацієнтів зі встановленим АССЗ (ВР 0,85), аніж в учасників без встановленого АССЗ (ВР 0,94), що з огляду на значення р для взаємодії (0,068) дає підстави припустити (хоча й не дає змоги остаточно стверджувати), що за наявності АССЗ зниження ризику під дією АР ГПП-1 може бути більш вираженим. На підставі цих сукупних даних, експерти ESC вважають, що застосування іНЗКТГ2 та/або АР ГПП-1 рекомендовано пацієнтам із ЦД2 і АССЗ незалежно від схеми гіпоглікемічної терапії та застосування метформіну (рекомендація класу I) і може розглядатися в пацієнтів із ЦД2 без АССЗ або тяжкого УОМ, але з розрахунковим 10-річним ризиком розвитку ССЗ за шкалою SCORE2-Diabetes ≥10% незалежно від схеми гіпоглікемічної терапії (IIb) [1]. Що стосується піоглітазону, то на підставі результатів проведеного дослідження та подальших метааналізів, а також з урахуванням здатності тіазолідиндіонів спричиняти затримку рідини й підвищувати ризик розвитку СН можливість його застосування може бути розглянута при потребі в посиленні контролю глікемії в пацієнтів із ЦД2 та АССЗ, але без СН (IIb). З огляду на непереконливі результати проведених досліджень і метааналізів щодо СС ефектів метформіну, його застосування не має бути обов'язковою умовою для призначення іНЗКТГ2 або АР ГПП-1 з метою зниження СС ризику. Однак більшість учасників ДОССН іНЗКТГ2 або АР ГПП-1 отримували метформін; тому пацієнтам із ЦД2 та АССЗ, які вже отримують метформін, слід призначати іНЗКТГ2 та/або АР ГПП-1 незалежно від потреби в додатковому контролі глікемії, а пацієнтам із ЦД2 та АССЗ, які не отримують метформін, слід першочергово призначати іНЗКТГ2 та/або АР ГПП-1, а метформін слід додавати до схеми лікування тих пацієнтів, які після цього потребуватимуть додаткового контролю рівня глюкози. У пацієнтів без АССЗ або тяжкого УОМ із низьким або помірним СС ризиком лікування метформіном має розглядатися (IIa), а в пацієнтів без АССЗ або тяжкого УОМ з високим або дуже високим СС ризиком лікування метформіном може розглядатися (IIb) [1]. Артеріальна гіпертензія. Розділ, присвячений цільовим значенням артеріального тиску (АТ) і контролю АГ у пацієнтів з ЦД і переддіабетом, не зазнав виражених змін. Експерти рекомендують застосовувати персоналізований підхід до корекції підвищеного АТ у цій групі пацієнтів. Зокрема, цільове значення систолічного АТ для молодших пацієнтів встановлено на рівні 130 мм рт. ст. (<130 мм рт.ст. за умови доброї переносимості, але не менше 120 мм рт. ст.), а для осіб віком >65 років – на рівні 130–139 мм рт. ст. (I). Цільове значення діастолічного АТ <80 мм рт. ст. рекомендовано для всіх пацієнтів, які отримують лікування АГ. Першою лінією антигіпертензивної терапії залишаються блокатори ренін-ангіотензинової системи (РАС) – інгібітори ангіотензинперетворювального ферменту (іАПФ) і блокатори рецепторів ангіотензину (БРА); за наявності показань до комбінованої терапії інгібітори РАС рекомендується комбінувати з блокаторами кальцієвих каналів або тіазидними/тіазидоподібними діуретиками (І) [1]. Дисліпідемія. Основні зміни в розділі «Дисліпідемія» присвячені застосуванню інгібіторів пропротеїнової конвертази субітилізин-кексинового типу 9 (PCSK9, еволокумаб і алірокумаб) – моноклональних антитіл, які виражено знижують рівень холестерину (ХС) ліпопротеїнів низької щільності (ЛПНЩ) у плазмі, впливаючи на білок, що бере участь у регуляції експресії рецептора ЛПНЩ на гепатоцитах. При використанні в поєднанні з високоінтенсивною терапією статинами (з езетимібом або без нього) інгібітори PCSK9 значно знижували частоту MACE в підгрупах пацієнтів із ЦД та АССЗ, включених до досліджень FOURIER (Further Cardiovascular Outcomes Research with PCSK9 Inhibition in Subjects with Elevated Risk) та ODYSSEY OUTCOMES (Evaluation of Cardiovascular Outcomes After an Acute Coronary Syndrome During Treatment With Alirocumab) відповідно [6, 7]. Зокрема, у дослідженні FOURIER еволокумаб продемонстрував 17% зниження ВР комбінованої первинної кінцевої точки, що включала смерть від СС причин, ІМ, інсульт, госпіталізацію з приводу нестабільної стенокардії або коронарну реваскуляризацію, у пацієнтів із ЦД (ВР 0,83, 95% ДІ 0,75–0,93, р=0,0008) [6]. А в дослідженнях BANTING (Evaluation of Evolocumab Efficacy in Diabetic Adults With Hypercholesterolemia/Mixed Dyslipidemia) і BERSON (Safety and Efficacy of Evolocumab in Combination With Statin Therapy in Adults With Diabetes and Hyperlipidemia or Mixed Dyslipidemia) еволокумаб також значно знижував рівень інших атерогенних ліпідів (тобто тригліцеридів [ТГ], ХС, що не входить до ліпопротеїнів високої щільності [ЛПВЩ], і частинок, що містять аполіпопротеїн В) у пацієнтів із ЦД і змішаною дисліпідемією порівняно з плацебо [8, 9]. Зі свого боку алірокумаб значно знижував частоту комбінації СС смерті, ІМ, інсульту або госпіталізації з приводу нестабільної стенокардії в підгрупі пацієнтів із ГКС і ЦД2 (n=5444) у дослідженні ODYSSEY OUTCOMES [10]. При цьому в умовах додавання до максимальної переносимої дози статину алірокумаб був ефективнішим за езетиміб або фенофібрат у зниженні рівня ХС не-ЛПВЩ та інших атерогенних ліпідів у пацієнтів із ЦД, включених у дослідження ODYSSEY DM-DYSLIPIDEMIA (Efficacy and Safety of Alirocumab Versus Usual Care on Top of Maximally Tolerated Statin Therapy in Patients With Type 2 Diabetes and Mixed Dyslipidemia) [11]. Метааналіз Khan et al. не виявив значущого зв’язку між застосуванням інгібіторів PCSK9 і de novo розвитком ЦД (ВР 1,00, 95% ДІ 0,93–1,07, р=0,96) і водночас підтвердив помірний ризик розвитку ЦД при монотерапії статинами (ВР 1,10, 95% ДІ 1,05–1,15, р<0,001) [12]. Як наслідок, у настанові з'явилася нова рекомендація щодо застосування інгібіторів PCSK9, згідно з якою їхнє призначення рекомендується пацієнтам із дуже високим СС ризиком і стабільно високими рівнями ХС ЛПНЩ, незважаючи на приймання максимальної переносимої дози статину в комбінації з езетимібом, або пацієнтам із непереносимістю статинів (рекомендація класу I) [1]. Щодо пацієнтів із гіпертригліцеридемією, у яких рівні ТГ залишаються підвищеними навіть на тлі статинотерапії, експерти ESC вважають, що стабільний ефір ейкозапентаєнової кислоти ікозапент етил може мати перевагу перед іншими омега-3 жирними кислотами, оскільки в дослідженні REDUCE-IT (Reduction of Cardiovascular Events with Icosapent Ethyl-Intervention Trial) під час застосування в дозі 2 г 2 рази на добу ікозапент етил чинив сприятливий вплив на СС наслідки, незалежно від наявності ЦД (р для взаємодії 0,29) [13]. Як наслідок зазначено, що застосування вказаної дози ікозапент етилу в комбінації зі статином можна розглядати в пацієнтів із гіпертригліцеридемією (IIb) [1]. Антитромбоцитарна терапія. Розділ, присвячений питанням застосування антитромбоцитарної терапії (АТТ) у пацієнтів із ЦД, розділений на три основні частини. У першій частині розглядається популяція пацієнтів із ЦД, але без анамнезу симптоматичного АССЗ або реваскуляризації. Аналіз доступних даних, включно з результатами крупного рандомізованого клінічного дослідження (РКД) ASCEND (A Study of Cardiovascular Events iN Diabetes) і великомасштабного метааналізу даних 95 тис. учасників шести РКД, дали змогу дійти висновку, що в цій підгрупі хворих на ЦД застосування ацетилсаліцилової кислоти (АСК) у дозі 75–100 мг/добу з метою профілактики розвитку першої тяжкої судинної події можна розглядати за відсутності явних протипоказань (IIb). Друга частина розділу присвячена застосуванню АТТ у пацієнтів з АССЗ та/або реваскуляризацією, які не мають показань до довгострокової антикоагулянтної терапії. Рекомендації щодо АТТ у цій популяції залежать від типу коронарного синдрому (гострий [ГКС] vs хронічний [ХКС]) і типу реваскуляризації (черезшкірне коронарне втручання [ЧКВ] vs аортокоронарне шунтування [АКШ]) та стисло представлені на рисунку 1 [1]. Третя частина розділу стосується пацієнтів із ЦД, ГКС/ ХКС, які пройшли реваскуляризацію і потребують довгострокової антикоагулянтної терапії. У цьому випадку рекомендується щонайменше тижнева потрійна терапія комбінацією низької дози АСК, клопідогрелю та перорального антикоагулянту (ОАК) із подальшим переходом на подвійну терапію комбінацією ОАК та одного з антиагрегантів (I). У разі, якщо в окремих пацієнтів тромботичний ризик переважує ризик кровотеч, тривалість потрійної терапії можна збільшити до 1 місяця (IIa), а в деяких пацієнтів можна розглянути 3-місячну потрійну антитромботичну терапію (IIb) [1]. Слід зазначити окрему рекомендацію класу III, згідно з якою при використанні клопідогрелю гастропротекція за допомогою призначення омепразолу й езомепразолу не рекомендується [1].
СН і ЦД СН є одним із найчастіших початкових проявів ССЗ у пацієнтів із ЦД2 і може проявлятися у вигляді СН зі збереженою (СНзбФВ), помірно зниженою (СНпзнФВ) і зниженою (СНзнФВ) фракцією викиду (ФВ) лівого шлуночка (ЛШ). З огляду на те що одночасна наявність ЦД і СН значно погіршує прогноз пацієнта, вкрай важливо обстежувати всіх пацієнтів із ЦД на наявність проявів СН із метою раннього призначення терапії, що зберігає життя. Для прогнозування ризику СН серед амбулаторних пацієнтів із ЦД2 запропоновано використовувати шкалу ризику WATCH-DM, у рамках якої кожне збільшення оцінки на 1 одиницю пов'язане з підвищенням 5-річного ризику СН на 24% [1]. Крім того, хороші результати прогнозування 5- і 10-річного ризику СН серед пацієнтів із ЦД показав підхід із застосуванням біомаркерів, включно з високочутливим серцевим тропоніном Т (пороговий рівень ≥6 нг/л), N-термінальним фрагментом мозкового натрійуретичного пептиду (NT-proBNP; ≥125 пг/мл), високочутливим С-реактивним білком (≥3 мг/л), а також ознаками гіпертрофії ЛШ за даними ЕКГ. За відповідність кожному із цих критеріїв пацієнт отримує 1 бал, найвищий 5-річний ризик СН відзначають серед осіб з оцінкою ≥3 балів. Алгоритм регулярного обстеження, покликаного зафіксувати перехід пацієнта із ЦД із групи підвищеного ризику розвитку СН до наявності розвиненої СН, наведено на рисунку 2 [1].


Принципи лікування СН у пацієнтів із ЦД у настанові подано з урахуванням фенотипу СН. У частині, присвяченій лікуванню СНзнФВ, особливий акцент зроблено на застосуванні іНЗКТГ2 (дапагліфлозин, емпагліфлозин і сотагліфлозин), іАПФ або комбінації сакубітрил/валсартан (ARNI), а також бета-блокаторів (БАБ) і антагоністів мінералокортикоїдних рецепторів (АМР); ці препарати рекомендовані всім пацієнтам із СНзнФВ і симптомами СН II–IV класу за класифікацією Нью-Йоркської асоціації кардіологів (NYHA), оскільки вони доведено знижують ризик госпіталізації з приводу СН (ГСН) і ризик смерті (СС смерті – для іНЗКТГ2) (усі рекомендації класу І з рівнем доказовості [РД] А) [1]. Ба більше, у настанові представлено рекомендацію класу I, РД В, у якій описується застосування інтенсивної терапевтичної стратегії з раннім призначенням науково-обґрунтованої медикаментозної терапії (НОМТ: іНЗКТГ2, ARNI/іАПФ, БАБ і АМР), швидким титруванням доз цих препаратів до визначених у дослідженнях цільових значень і частими контрольними візитами впродовж перших 6 тижнів після ГСН для зниження ризику повторних госпіталізацій і смерті пацієнтів [1]. До застосування апаратної терапії з використанням імплантованого кардіовертера-дефібрилятора й пристроїв для серцевої ресинхронізуючої терапії у хворих із ЦД рекомендується підходити так само, як і в загальній популяції хворих на СН. При непереносимості ARNI/іАПФ дозволяється замінити ці препарати на блокатори рецепторів ангіотензину II (БРА). Для полегшення симптомів, підвищення фізичної витривалості та зниження ризику ГСН у пацієнтів з ознаками та/або симптомами затримки рідини рекомендується використовувати діуретики. Також зазначено, що в пацієнтів із синусовим ритмом і частотою серцевих скорочень у спокої ≥70 уд/хв, у яких симптоми СН зберігаються на тлі приймання БАБ (у максимальній переносимій дозі), іАПФ/БРА і АМР, рекомендується розглянути застосування івабрадину для зниження ризику ГСН і СС смерті (IIa). Схожа рекомендація щодо застосування дигоксину (за збереження симптомів СН незважаючи на НОМТ) спрямована на зниження ризику ГСН і є рекомендацією класу IIb [1]. У розділах, присвячених лікуванню СНпзнФВ і СНзбФВ, основна увага приділяється іНЗКТГ2, оскільки їх застосування було пов'язане зі сприятливими результатами при ФВ ЛШ >40%. Зокрема, у дослідженні EMPEROR-Preserved (Empagliflozin Outcome Trial in Patients with Chronic Heart Failure With Preserved Ejection Fraction) за участю пацієнтів із симптомами II–IV класу за NYHA, ФВ ЛШ >40% і підвищеним рівнем NT-proBNP емпагліфлозин порівняно з плацебо знижував ризик первинної кінцевої точки, що включала СС смерть або ГСН, на 21%, що в основному було пов’язано з 29% зниженням ризику ГСН [14], при цьому отриманий ефект не залежав від статусу ЦД і значення HbA1c на вихідному рівні [15]. У дослідженні DELIVER (Dapagliflozin Evaluation to Improve the Lives of Patients with Preserved Ejection Fraction Heart Failure), яке проводили в схожій вибірці пацієнтів, дапагліфлозин знижував ризик комбінованої кінцевої точки, що включала погіршення перебігу СН і смерть від СС причин, на 18% порівняно з плацебо, що також було зумовлено переважно зниженням частоти ГСН, і, як і в EMPEROR-Preserved, отриманий ефект не залежав від статусу ЦД [16]. Подальший метааналіз даних 12 251 учасника досліджень DELIVER і EMPEROR-Preserved підтвердив, що в досліджуваній популяції іНЗКТГ2 значно знижують як ризик комбінації СС смерті та першої ГСН (ВР 0,80, 95% ДІ 0,73-0,87), так і ризики окремих її компонентів (СС смерть: ВР 0,88, 95% ДІ 0,77–1,00; перша ГСН: ВР 0,74, 95% ДІ 0,67–0,83) [17]. Загалом, досягнуті ефекти іНЗКТГ2 не відрізнялися в підгрупах пацієнтів із різними значеннями ФВ ЛШ, а також між пацієнтами із ЦД і без ЦД. Як наслідок, застосування іНЗКТГ2 емпагліфлозину або дапагліфлозину в пацієнтів із ЦД2 і ФВ ЛШ >40% рекомендується для зниження ризику ГСН і СС смерті й розглядається в настанові ESC як рекомендація класу I [1]. Отже, іНЗКТГ2 у цій настанові розглядаються як ПДП вибору для пацієнтів із ЦД2 та будь-яким типом СН (СНзбФВ, СНпзнФВ і СНзнФВ), які слід призначати незалежно від рівня HbA1c і супутньої протидіабетичної терапії (I). За необхідності посилити протидіабетичну терапію слід розглядати можливість призначення інших ПДП із нейтральним ефектом на СН за даними ДОССН, а саме АР ГПП-1, ситагліптину/лінагліптину, метформіну або інсуліну (інсулін гларгін або інсулін деглудек) (клас IIa). З огляду на здатність до підвищення ризику ГСН, продемонстровану в ДОССН, застосування піоглітазону й саксагліптину в такій ситуації не рекомендується (клас III) [1].
ЦД і ФП У розділі, присвяченому ФП, основний акцент зроблено на важливості систематичного скринінгу, стратифікації ризиків емболії та кровотеч, а також на застосуванні пероральних антикоагулянтів (ОАК). Важливість скринінгу на ФП зумовлена високою поширеністю цієї серцевої аритмії та вищим ризиком розвитку інсульту серед хворих на ЦД. Пропонований алгоритм скринінгу представлений на рисунку 3 [1].
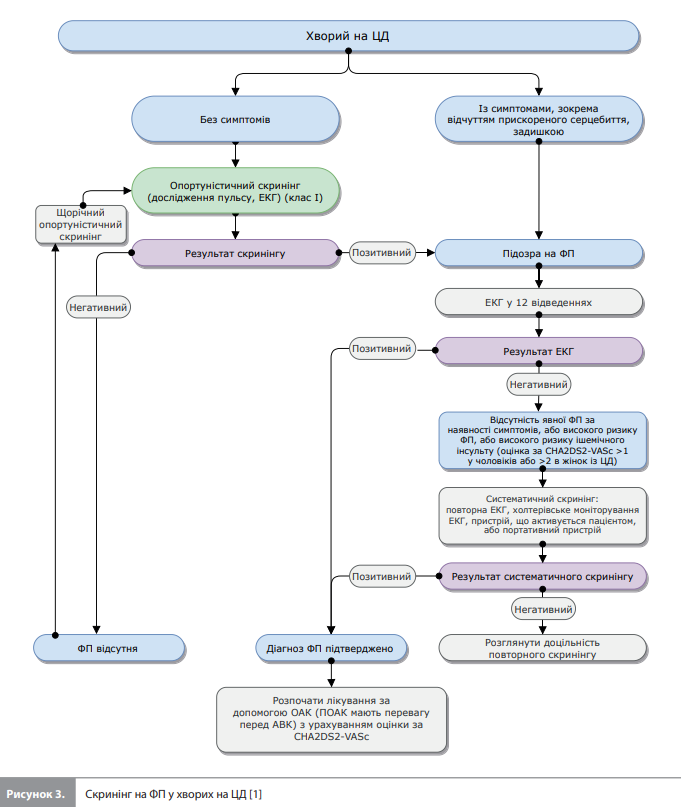
Для стратифікації ризиків інсульту й кровотечі в пацієнтів на ЦД рекомендується використовувати шкали CHA2DS2-VASc і HAS-BLED відповідно. Профілактику інсульту за допомогою ОАК рекомендується розпочинати за наявності в пацієнта з ЦД і ФП щонайменше одного додаткового фактора ризику інсульту (тобто за оцінкою за CHA2DS2-VASc >1 у чоловіків або >2 у жінок) (І) і слід розглядати в осіб із ЦД і ФП без додаткових факторів ризику інсульту, включно з пацієнтами із ЦД 1 або 2 типу віком до 65 років (IIa). При виборі ОАК антагоністи вітаміну К (АВК) поступаються прямим ОАК (ПОАК), чия дія не пов’язана з антагонізмом по відношенню до вітаміну К (за винятком пацієнтів з механічними серцевими клапанами або помірним/тяжким мітральним стенозом) (I). Важливою метою оцінки за шкалою HAS-BLED є виявлення оборотних факторів ризику кровотеч для їх подальшої корекції, а також ідентифікація пацієнтів, які потребують ретельного подальшого спостереження [1].
ЦД і хронічна хвороба нирок У розділі, присвяченому веденню пацієнтів із комбінацією ЦД і хронічної хвороби нирок (ХХН), основна увага приділяється таким аспектам: зниження СС ризику й ризику розвитку ниркової недостатності (НН), організація антигіпертензивної, антитромботичної та гіполіпідемічної терапії. Статинотерапія знижує ризик серйозних атеросклеротичних подій (тобто ризик смерті від коронарних подій, ризики нефатального ІМ, ішемічного інсульту й коронарної реваскуляризації) у пацієнтів із ХХН, але не сповільнює значущо прогресування ХХН. Більше того, дослідження та метааналізи досліджень статинів виявили тенденцію до менш вираженого відносного зниження СС ризику на кожен 1 ммоль/л зменшення рівня ХС ЛПНЩ у міру зниження розрахункової швидкості клубочкової фільтрації (рШКФ) та невизначеність щодо користі статинотерапії для пацієнтів, які перебувають на діалізі [18]. На основі цих даних було зроблено висновок про необхідність застосування більш інтенсивних схем, спрямованих на зниження рівня ХС ЛПНЩ, для досягнення максимального ефекту в осіб із ХХН. Отже, метою гіполіпідемічної терапії в пацієнтів із ХХН та ЦД має бути максимально можливе, але безпечне зниження абсолютного рівня ХС ЛПНЩ. Чотири великі дослідження за участю різних підгруп пацієнтів із ХХН підтвердили безпечність інтенсивного зниження рівня ХС ЛПНЩ за допомогою монотерапії статинами (аторвастатин, розувастатин, флувастатин) або комбінації помірної дози симвастатину з езетимібом [19–23]. Крім того, попри відсутності спеціального великомасштабного дослідження інгібіторів PCSK9 у пацієнтів із ХХН, аналіз у підгрупах, виділених за стадіями ХХН, проведений у дослідженні FOURIER, у якому оцінювали інгібітор PCSK9 еволокумаб, виявив, що ефект досліджуваного лікування у вигляді зниження рівня ХС ЛПНЩ зберігається в пацієнтів із 3 стадією ХХН, і, до того ж, СС ефекти лікування не залежать від вихідного значення рШКФ [24]. Виходячи з наведених даних, у чинній версії настанови застосування в пацієнтів із ЦД і ХХН інтенсивної терапії статином або комбінацією статин + езетиміб для зниження рівня ХС ЛПНЩ є рекомендацією класу I [1]. Із великих досліджень за участю пацієнтів із ЦД2 і ХХН відомо, що кілька груп препаратів, розроблених для зниження СС ризику або корекції гіперглікемії, а саме інгібітори РАС, іНЗКТГ2 і фінеренон, паралельно знижують ризик прогресування ХХН. Існуючі дані підтримують якомога більш раннє призначення цих препаратів із метою запобігти ушкодженню органів-мішеней у таких пацієнтів, тому інгібітори РАС рекомендується призначати пацієнтам із ЦД одразу після встановлення клінічного діагнозу ХХН і прагнути при цьому до досягнення максимальних переносимих доз цих препаратів (I). Слід зазначити, однак, що поєднане застосування іАПФ і БРА, як і раніше, не рекомендується (III). Навпаки, комбіноване застосування іНЗКТГ2 та іАПФ або БРА заохочується, оскільки явно знижує ризик розвитку НН і ГСН у пацієнтів із ХХН і ЦД2 [25, 26]; при цьому окремі плацебо-контрольовані дослідження іНЗКТГ2 (CREDENCE, DAPA-CKD і EMPA-KIDNEY) і метааналіз усіх великих досліджень іНЗКТГ2 показали, що зниження ризику прогресування ХХН і вплив терапії на ризик ГСН або СС смерті не залежали від вихідного рівня рШКФ [27]. Як наслідок, застосування іНЗКТГ2 канагліфлозину, емпагліфлозину або дапагліфлозину рекомендується пацієнтам із ЦД2 та ХХН (із призначенням після появи перших клінічних ознак ХХН) і рШКФ ≥20 мл/хв/1,73 м2 для зниження ризику ССЗ і НН (I). Через відсутність великих досліджень із достатньо тривалим подальшим спостереженням серед пацієнтів із ЦД1 і ХХН на цей момент незрозуміло, чи переважують абсолютні переваги іНЗКТГ2, пов'язані з впливом на ризик НН і СС наслідків, підвищений абсолютний ризик кетоацидозу під час застосування іНЗКТГ2 в умовах ЦД1. Рекомендація класу I щодо застосування фінеренону на додаток до іАПФ або БРА в пацієнтів із ЦД2 та рШКФ >60 мл/хв/1,73 м2 і співвідношенням альбумін/креатинін у сечі (САКС) ≥30 мг/ммоль або з рШКФ 25–60 мл/хв/1,73 м2 і САКС ≥3 мг/ммоль засновані на результатах досліджень FIDELIO-DKD (Efficacy and Safety of Finerenone in Subjects With Type 2 Diabetes Mellitus and Diabetic Kidney Disease) і FIGARO-DKD (Efficacy and Safety of Finerenone in Subjects With Type 2 Diabetes Mellitus and the Clinical Diagnosis of Diabetic Kidney Disease), які показали, що лікування фінереноном призводить до зниження ризику розвитку НН та комбінованого СС наслідку, що включав смерть від СС причин, нефатальний ІМ, нефатальний інсульт або ГСН, у пацієнтів з ХХН та ЦД2, які вже отримували максимальну дозу іАПФ або БРА [28–30]. Інформація про безпечність та ефективність комбінування фінеренону з іНЗКТГ2 при ХХН обмежена: таку комбінацію отримували лише ~4% учасників FIDELIO-DKD, ~8% учасників FigaroDKD і ~5% учасників DAPA-CKD. Однак результати аналізів у підгрупах дають змогу вважати, що ця комбінація не впливає на результати оцінювання безпечності фінеренону та іНЗКТГ2 у ключових дослідженнях цих препаратів [1]. У частині, присвяченій контролю рівня АТ і глікемії за наявності ЦД і ХХН, встановлюються такі цільові значення показників: АТ ≤130/80 мм рт. ст. (рекомендується як цільове значення, досягнення якого дає змогу знизити ризик ССЗ та альбумінурію) і HbA1c 6,5–8% (за можливості – <7%, оскільки такий рівень глікемії знижує ризик розвитку мікросудинних ускладнень) (клас І для обох рекомендацій). Серед препаратів, що дають змогу контролювати рівень глюкози в крові, зазначено метформін (за умови, що рШКФ перевищує 30 мл/хв/1,73 м2), а також значна увага приділяється АР ГПП-1 [1]. Екстраполяція даних із досліджень, проведених за участю пацієнтів із ЦД2, дає змогу припустити, що АР ГПП-1 безпечно покращують контроль глікемії та можуть знижувати масу тіла й СС ризик у пацієнтів із ХХН [5]. Метааналіз досліджень АР ГПП-1 (ліксисенатиду, ліраглутиду, семаглутиду, ексенатиду, альбіглутиду, дулаглутиду, еффегленатиду) показав сприятливе зниження рівня альбумінурії у хворих на ЦД2, зниження ризику MACE в осіб із попереднім ССЗ або з високим СС ризиком на тлі приймання деяких АР ГПП-1, при цьому зниження ризику MACE було однаковим в учасників зі зниженою та нормальною вихідною рШКФ [5]. Як наслідок, призначення АР ГПП-1 у пацієнтів із рШКФ >15 мл/ хв/1,73 м2 розглядають як стратегію, що дає змогу домогтися адекватних рівнів глікемії з низьким ризиком гіпоглікемії та сприятливим ефектом на масу тіла, СС ризик і альбумінурію, а тому є рекомендацією класу I [1]. Що стосується застосування АСК у хворих на ЦД і ХХН, то низькі дози (75–100 мг один раз на день), як і раніше, показані тільки за наявності діагностованого АССЗ (вторинна СС профілактика, рекомендація класу I), оскільки в рамках первинної профілактики АССЗ користь і ризик низьких доз АСК можуть нівелювати одне одного [1].
З повним текстом настанови англійською мовою можна ознайомитися на офіційному сайті ESC за адресою www.escardio.org.
Список літератури знаходиться в редакції
Автор огляду Віктор Мицьо Medicine Review 2024; 1 (74): 19 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2026. Усі права захищені.
|
мапа сайту корисні посилання |