Порівняльна ефективність і безпечність прасугрелю й тикагрелору в пацієнтів із ГКС залежно від анамнезу інфаркту міокарда: результати апостеріорного аналізу дослідження ISAR-REACT 5У наші дні приблизно 20% пацієнтів, які проходять лікування гострого коронарного синдрому (ГКС), мають в анамнезі перенесений інфаркт міокарда (ІМ) [1], що означає більший ризик повторних ішемічних подій і гірші віддалені результати порівняно з пацієнтами без попереднього ІМ [2–4]. Цей анамнез і пов’язані з ним ризики треба обов’язково враховувати під час призначення антитромботичної терапії, зокрема подвійної антиагрегантної терапії (ПАТ) комбінацією ацетилсаліцилової кислоти (АСК) та інгібітора P2Y12-рецепторів тромбоцитів (іP2Y12), після ГКС [5, 6]. Для початкової (перші 6–12 місяців) ПАТ було встановлено, що потужніші іP2Y12 тикагрелор і прасугрель у складі ПАТ з АСК перевершують менш потужний іP2Y12 клопідогрель у запобіганні повторним тромботичним подіям після ГКС [7, 8]. Для тикагрелору ці переваги були доведені, зокрема, і серед пацієнтів з ІМ в анамнезі, включно з хворими, які пройшли інвазивне лікування [7], у той час як для прасугрелю подібні порівняльні дані відсутні. Однак розширити знання про прасугрель у цьому напрямі дали змогу результати рандомізованого клінічного дослідження (РКД) ISARREACT (Intracoronary Stenting and Antithrombotic Regimen: Rapid Early Action for Coronary Treatment) 5, яке показало, що прасугрель перевершує тикагрелор у зниженні 12-місячної кумулятивної частоти ішемічних подій, не підвищуючи при цьому ризик кровотеч, у пацієнтів із ГКС, які пройшли інвазивне лікування [8], а також дані подальшого апостеріорного аналізу ISAR-REACT 5, проведеного Lahu et al. із метою з'ясувати, чи впливає раніше (до індексного ГКС) перенесений ІМ на порівняльну ефективність і безпечність тикагрелору й прасугрелю в пацієнтів, які пройшли інвазивне лікування ГКС [9]. Результати цього аналізу коротко представлені нижче.
Дизайн дослідження ISAR-REACT 5 і методологія аналізу Lahu et al. Учасниками РКД ISAR-REACT 5 були пацієнти з ГКС (нестабільна стенокардія, ІМ із підйомом [ІМпST] або без підйому [ІМбпST] сегмента ST на електрокардіограмі [ЕКГ]), направлені на отримання інвазивного лікування та рандомізовані в групи терапії тикагрелором або прасугрелем у співвідношенні 1:1. Пацієнти, рандомізовані в групу тикагрелору, отримували навантажувальну дозу препарату (180 мг) якомога швидше після рандомізації, а потім приймали підтримуючу дозу 90 мг 2 рази на день. Схема лікування в групі прасугрелю залежала від типу ГКС, віку й маси тіла пацієнта. Учасники з ІМпST отримували навантажувальну дозу 60 мг якомога швидше після рандомізації, а потім приймали підтримуючу дозу 10 мг один раз на день, а пацієнти з ГКС без підйому сегмента ST (ГКСбпST) отримували навантажувальну дозу 60 мг після оцінки анатомії коронарних артерій (але до виконання черезшкірного коронарного втручання [ЧКВ]), після чого також приймали підтримуючу дозу 10 мг один раз на день. Учасникам віком ≥75 років і людям із масою тіла <60 кг була рекомендована підтримуюча доза прасугрелю 5 мг. Усі пацієнти в обох групах також отримували АСК: спочатку навантажувальну дозу (внутрішньовенно або перорально) 150–300 мг, а потім – пероральну підтримуючу дозу 75–100 мг на добу. Тривалість ПАТ комбінацією тикагрелор + АСК або прасугрель + АСК становила як мінімум 12 місяців [9]. До учасників з ІМ в анамнезі відносили пацієнтів, які відповідали принаймні одному з таких критеріїв: наявність документального підтвердження раніше перенесеного ІМ, наявність патологічних зубців Q на вихідній ЕКГ за відсутності інших неішемічних причин та/або наявність ознак регіональної втрати життєздатності міокарда за даними методів променевої діагностики. Відповідно до цих критеріїв усі учасники дослідження були розділені на дві групи: з раніше перенесеним ІМ і без раніше перенесеного ІМ [9]. Первинною комбінованою кінцевою точкою ефективності РКД і апостеріорного аналізу була комбінація ІМ, інсульту й смерті від усіх причин. Вторинною кінцевою точкою безпеки була комбінація кровотеч 3–5 типів згідно з визначенням Академічного консорціуму з вивчення кровотеч (BARC). Додаткові кінцеві точки включали окремі компоненти первинної комбінованої кінцевої точки, а також доведений і ймовірний тромбоз стента. Оцінка всіх кінцевих точок проводилася через 12 місяців після рандомізації. За час спостереження стан учасників оцінювали тричі – через 30 ± 10 днів, 6 ± 1 місяць і 12 ± 1 місяць після рандомізації на основі інформації, зібраної за допомогою телефонного опитування, листів або відомостей з амбулаторної та стаціонарної документації пацієнтів [9]. Аналіз, проведений Lahu et al., не був заздалегідь запланованим і проводився як апостеріорний (post hoc) вторинний аналіз. Під час опрацювання даних із РКД ISAR-REACT 5 безперервні змінні було подано як середнє значення ± стандартне відхилення або медіана з міжквартильним розмахом, і їх порівнювали з використанням t-критерію Стьюдента або непараметричного критерію суми рангів Вілкоксона. Категоріальні дані були подані у вигляді показників абсолютної та відносної (відсотки) кількості й порівнювалися з використанням критерію хі-квадрат або точного критерію Фішера. Для аналізу первинної комбінованої кінцевої точки й смертності від усіх причин використовували метод Каплана-Мейєра. Усі інші кінцеві точки аналізували після врахування конкуруючого ризику смерті. В аналізі, проведеному Lahu et al., ризики всіх небажаних подій оцінювали двічі – спочатку залежно від наявності/відсутності в анамнезі раніше перенесеного ІМ, а потім залежно від групи досліджуваного лікування (тикагрелор vs прасугрель). На обох етапах використовували модель пропорційних ризиків Кокса з оцінкою потенційного статистичного взаємозв'язку між досліджуваним лікуванням і статусом раніше перенесеного ІМ (був vs не було). При оцінці ризиків розраховували відношення ризиків (ВР) і відповідні 95% довірчі інтервали (ДІ). Первинну комбіновану кінцеву точку аналізували у вибірці рандомізованих пацієнтів (тобто з урахуванням призначеного, а не фактично отриманого лікування), вторинну кінцеву точку безпеки – у модифікованій вибірці рандомізованих пацієнтів, що включала всіх пацієнтів, які отримали хоча б одну дозу досліджуваного препарату, при цьому в оцінку включали всі кровотечі, зареєстровані впродовж усього періоду лікування плюс 1 тиждень після припинення приймання досліджуваного препарату. Крім того, для виявлення можливої залежності ризику первинної комбінованої кінцевої точки від часу проводили етапний аналіз даних, зібраних протягом перших 30 днів лікування. І, нарешті, був проведений аналіз чутливості, що включав тільки дані пацієнтів, які пройшли ЧКВ, для оцінки впливу коронарної реваскуляризації на ризик первинної та вторинної кінцевих точок на тлі досліджуваного лікування. При всіх порівняннях двостороннє значення р<0,05 вказувало на статистичну значущість отриманих результатів [9].

Результати аналізу Lahu et al. До цього аналізу увійшли дані 4015 учасників РКД ISARREACT 5 із відомим статусом раніше перенесеного ІМ, з яких 631 (15,7%) пацієнт мав ІМ в анамнезі, а 3384 (84,3%) пацієнти – не мали анамнезу ІМ [9]. Вихідні дані й результати ангіографії відповідно до статусу раніше перенесеного ІМ. Вихідні й ангіографічні дані відповідно до статусу раніше перенесеного ІМ наведено в таблиці 1 [1]. Як видно з таблиці 1, пацієнти з ІМ в анамнезі були старшими, частіше мали цукровий діабет (ЦД), гіперхолестеринемію, раніше перенесену коронарну реваскуляризацію, вищий індекс маси тіла, але рідше були курцями порівняно з пацієнтами без раніше перенесеного ІМ. У пацієнтів з ІМ в анамнезі індексний ГКС частіше був нестабільною стенокардією і рідше – ІМпST, порівняно з пацієнтами без раніше перенесеного ІМ. Загалом 4001 пацієнт (99,7%) пройшов коронарографію, і за цим показником підгрупи пацієнтів з анамнезом і без анамнезу ІМ були зіставними (99,4 vs 99,7%; р=0,26). У пацієнтів із раніше перенесеним ІМ частіше реєстрували багатосудинне ураження коронарного русла, знижену фракцію викиду лівого шлуночка й використання стегнового доступу порівняно з пацієнтами без раніше перенесеного ІМ. Крім того, пацієнти з ІМ в анамнезі при надходженні в стаціонар у зв’язку з індексним ГКС частіше приймали АСК і/або клопідогрель порівняно з пацієнтами без раніше перенесеного ІМ [1].
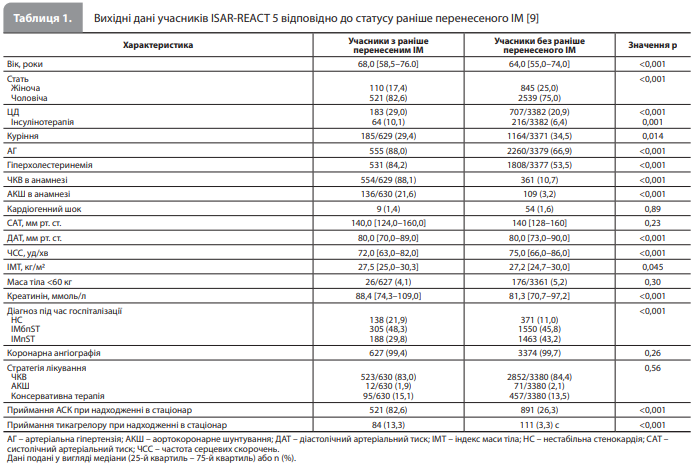
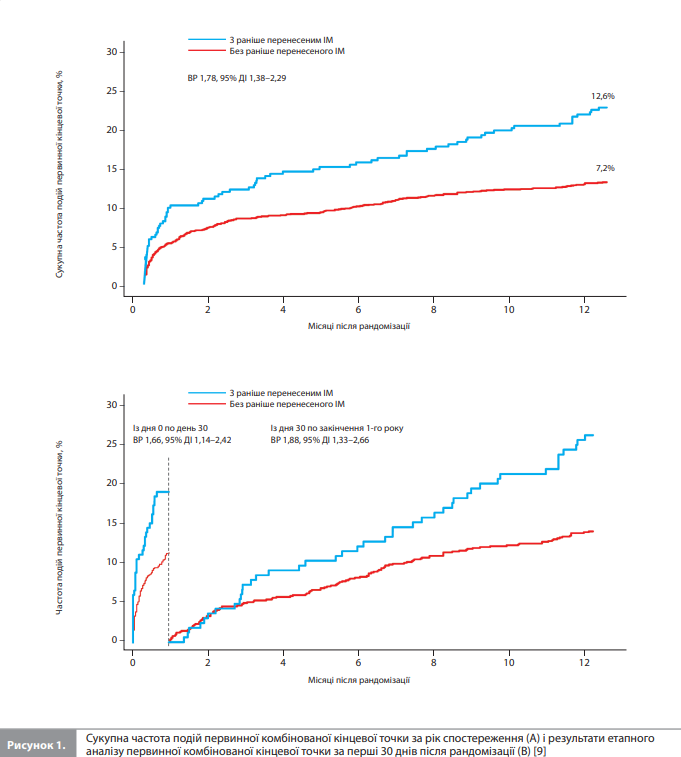
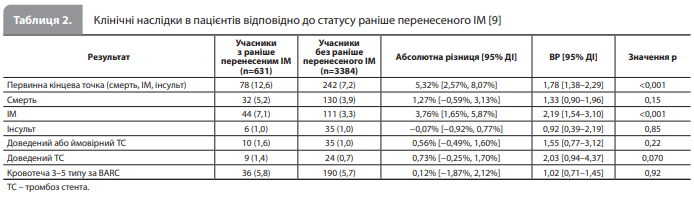
Клінічні наслідки залежно від статусу раніше перенесеного ІМ. Результати, зареєстровані в досліджуваній вибірці з урахуванням статусу раніше перенесеного ІМ, представлені в таблиці 2 [9]. Події первинної комбінованої кінцевої точки сталися в 78 пацієнтів із раніше перенесеним ІМ і в 242 пацієнтів без ІМ в анамнезі (кумулятивна захворюваність 12,6 vs 7,2%, ВР 1,78, 95% ДІ 1,38–2,29; рис. 1А) [9]. Статистично значуща різниця між групами була в основному зумовлена вищою частотою повторного ІМ у пацієнтів із раніше перенесеним ІМ порівняно з пацієнтами без ІМ в анамнезі (7,1 vs 3,3%, ВР 2,19, 95% ДІ 1,54–3,10). Ризик подій первинної комбінованої кінцевої точки відповідно до анамнезу ІМ не залежав від часу (рис. 1B): пацієнти з раніше перенесеним ІМ мали стабільно вищий ризик подій первинної комбінованої кінцевої точки як упродовж перших 30 днів після рандомізації (ВР 1,66, 95% ДІ 1,14–2,42), так і в інтервалі з 30-го дня до закінчення 12 місяців після рандомізації (ВР 1,88, 95% ДІ 1,33–2,66) порівняно з пацієнтами без ІМ в анамнезі. Кровотечі 3–5 типів за BARC розвинулися в 36 пацієнтів з ІМ в анамнезі й в 190 пацієнтів без раніше перенесеного ІМ (5,8 vs 5,7%, ВР 1,02, 95% ДІ 0,71–1,45, р=0,92). Доведений або ймовірний тромбоз стента й інсульт реєструвалися нечасто, без статистично значущої різниці між групами пацієнтів із різним статусом раніше перенесеного ІМ (табл. 2) [9].
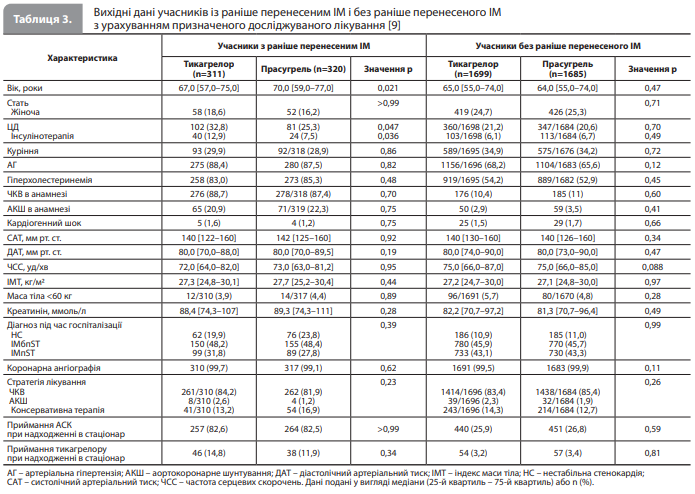
Вихідні дані відповідно до статусу раніше перенесеного ІМ і досліджуваного препарату. У групі учасників із раніше перенесеним ІМ 311 пацієнтам було призначено тикагрелор, а 320 пацієнтам – прасугрель. У групі учасників без ІМ в анамнезі ці показники становили 1699 і 1685 відповідно. Розподіл вихідних даних відповідно до призначеного лікування і статусу раніше перенесеного ІМ представлено в таблиці 3 [1]. Серед пацієнтів з ІМ в анамнезі, які отримували тикагрелор або прасугрель, не було статистично значущих відмінностей за демографічними, клінічними, ангіографічними, процедурними даними й медикаментозною терапією, яку вони отримували під час надходження в стаціонар із приводу індексного ГКС, за винятком меншого середнього віку та більшої ймовірності ЦД серед пацієнтів, які отримували тикагрелор. Порівняння вихідних, ангіографічних і процедурних даних серед пацієнтів без ІМ в анамнезі, які отримували тикагрелор або прасугрель, показало незначні відмінності між групами лікування (табл. 3).
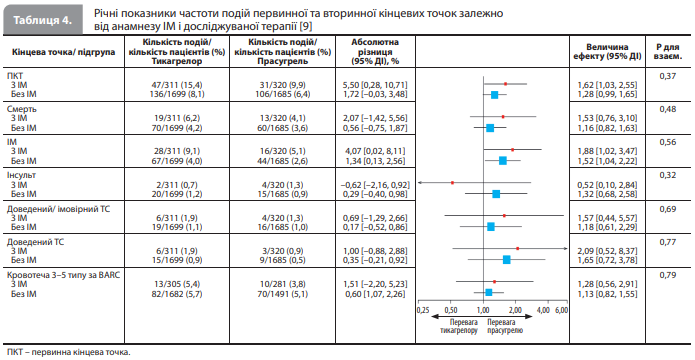
Клінічні результати залежно від статусу раніше перенесеного ІМ і досліджуваного препарату представлені в таблиці 4 [9]. Серед пацієнтів із раніше перенесеним ІМ кількість подій первинної комбінованої кінцевої точки становила 47 у групі тикагрелору й 31 у групі прасугрелю (кумулятивна захворюваність 15,4 vs 9,9%, ВР 1,62, 95% ДІ 1,03–2,55), при цьому ІМ частіше реєстрували в пацієнтів, які отримували тикагрелор, аніж у групі прасугрелю (кумулятивна захворюваність після врахування конкуруючого ризику смерті: 9,1 vs 5,1%, ВР 1,88, 95% ДІ 1,02–3,47). Кровотечі 3–5 типу за BARC були зареєстровані в 13 й 10 пацієнтів, які приймали тикагрелор і прасугрель відповідно (кумулятивна частота після врахування конкурентного ризику смерті: 5,4 vs 3,8%, ВР 1,28, 95% ДІ, 0,56–2,91). Серед пацієнтів без раніше перенесеного ІМ кількість подій первинної комбінованої кінцевої точки становила 136 у групі тикагрелору й 106 у групі прасугрелю (кумулятивна захворюваність 8,1 vs 6,4%, ВР 1,28, 95% ДІ 0,99–1,65), при цьому ІМ також частіше реєстрували в пацієнтів, що одержували тикагрелор, аніж в учасників, які приймали прасугрель (кумулятивна частота після врахування конкуруючого ризику смерті: 4,0 vs 2,6%, ВР 1,52, 95% ДІ 1,04–2,22). Кровотечі 3–5 типу за BARC були зареєстровані у 82 і 70 пацієнтів, які приймали тикагрелор і прасугрель відповідно (кумулятивна частота після врахування конкуруючого ризику смерті: 5,7 vs 5,1%, ВР 1,13, 95% ДІ 0,82–1,55). Аналіз взаємодії групи лікування й статусу раніше перенесеного ІМ показав відсутність статистично значущої взаємодії як для первинної (р для взаємодії 0,37), так і для вторинної (р для взаємодії 0,79) кінцевих точок. Ризик розвитку доведеного або ймовірного тромбозу стента або інсульту, вочевидь, мало різнився між групами тикагрелору й прасугрелю, незалежно від статусу раніше перенесеного ІМ. Результати аналізу чутливості, що включав тільки дані пацієнтів, які пройшли ЧКВ, були зіставні з результатами аналізу первинної і вторинної кінцевих точок у всій досліджуваній вибірці. З урахуванням деякого дисбалансу вихідних даних (за віком і статусом ЦД), виявленого серед пацієнтів із раніше перенесеним ІМ, зв'язок досліджуваного препарату з первинною та вторинною кінцевими точками дослідження було скориговано на вік і статус ЦД як на потенційні чинники, що можуть спотворювати результати. Після коригування ризик первинної комбінованої кінцевої точки ефективності (ішемічні події) на тлі приймання тикагрелору збільшувався (скориговане ВР 1,65, 95% ДІ 1,05–2,61, р=0,031), а ризик вторинної кінцевої точки безпеки (геморагічні події) залишався без зміни (скориговане ВР 1,46, 95% ДІ 0,64–3,35, р=0,37) [9].
Обговорення результатів аналізу Lahu et al. Результати, отримані Lahu et al. під час вторинного аналізу даних РКД ISAR-REACT 5 в ході порівняння ефективності й безпечності тикагрелору та прасугрелю в пацієнтів із ГКС залежно від статусу раніше перенесеного ІМ, можна підсумувати так [9]: 1. Порівняно з пацієнтами без раніше перенесеного ІМ, пацієнти з ІМ в анамнезі характеризуються підвищеним ризиком повторних ішемічних подій без збільшення ризику кровотеч при спостереженні впродовж 12 місяців. 2. У пацієнтів із ГКС прасугрель, вочевидь, перевершує тикагрелор у зниженні ризику ішемічних подій (первинна комбінована кінцева точка) і зниженні ризику повторного ІМ за будь-якого статусу раніше перенесеного ІМ (порівняно з прасугрелем, річний ризик повторного ІМ при застосуванні тикагрелору був підвищений на 52 і 88% у пацієнтів без анамнезу ІМ і з анамнезом ІМ відповідно). 3. Відносний ризик кровотечі при застосуванні тикагрелору й прасугрелю не залежав від статусу раніше перенесеного ІМ. Попередні дослідження показали, що пацієнти з рецидивуючими атеротромботичними подіями, наприклад хворі на ГКС із раніше перенесеним ІМ, вирізняються підвищеною інтенсивністю системного судинного запалення й більш високим тромботичним навантаженням, а також, що пацієнти з ІМ в анамнезі можуть отримати користь від посиленої антиагрегантної терапії, хоча й за рахунок збільшення ризику кровотечі [10–14]. З цієї причини чинні настанови з ведення пацієнтів із ГКС рекомендують застосовувати потужніші схеми антиагрегантної терапії у хворих із підвищеним ризиком ішемії (у тому числі після раніше перенесеного ІМ) за відсутності супутнього високого ризику кровотеч [6]. Представлені результати аналізу Lahu et al. дають змогу припустити, що в подібній ситуації, тобто в пацієнтів із ГКС і попереднім ІМ, ПАТ на основі прасугрелю може забезпечити кращий протиішемічний захист через потужніше й більш необоротне інгібування тромбоцитів порівняно з ПАТ на основі тикагрелору [15] без створення надлишкового ризику кровотеч завдяки коригуванню схеми лікування з урахуванням віку й маси тіла пацієнта, а також стратегії відмови від приймання дози прасугрелю перед коронарною ангіографією в пацієнтів із ГКСбпST [16, 17]. Автори вважають, що представлений аналіз розширює знання про можливість застосування пероральних іP2Y12 нового покоління серед хворих на ГКС із раніше перенесеним ІМ, які належать до групи високого ризику, але визнають, що дизайн дослідження (апостеріорний аналіз) обмежує його статистичну потужність, не даючи змоги зробити остаточні висновки щодо порівняльної ефективності та безпечності прасугрелю й тикагрелору в цих клінічних умовах. У зв'язку з цим отримані результати пропонується розглядати як гіпотезу, що потребує перевірки в добре організованих РКД [9].
Висновки Отже, апостеріорний аналіз результатів РКД ISAR-REACT 5 показав, що серед пацієнтів, які проходять інвазивне лікування ГКС, раніше перенесений ІМ пов'язаний зі значно підвищеним ризиком повторних ішемічних подій, але не збільшує ризик кровотеч порівняно з пацієнтами без попереднього ІМ. При цьому в зазначеній групі пацієнтів прасугрель, вочевидь, перевершує тикагрелор у зниженні ішемічного ризику без супутнього збільшення ризику кровотеч, незалежно від статусу раніше перенесеного ІМ. Ці дані можуть мати велике клінічне значення, а тому потребують підтвердження результатами рандомізованих досліджень, спеціально орієнтованих на пацієнтів із ГКС і раніше перенесеним ІМ.
Список літератури знаходиться в редакції
Автор огляду Віктор Мицьо Medicine Review 2023; 5 (72): 25 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2026. Усі права захищені.
|
мапа сайту корисні посилання |