Нові дані щодо застосування стратегії раннього переходу на монотерапію тикагрелором після ЧКВ у хворих на цукровий діабет: результати метааналізу п’яти рандомізованих дослідженьЦукровий діабет (ЦД) і атеросклеротична ішемічна хвороба серця (ІХС) тісно пов'язані між собою через численні патофізіологічні механізми та фактори ризику, що призводить до 2–4-кратного зростання ризику ІХС в осіб із ЦД [1] і наявності ЦД приблизно в половини хворих з ІХС [2]. Як наслідок, пацієнти з ЦД становлять значну частку в популяції хворих з ІХС і показаннями до черезшкірного коронарного втручання (ЧКВ) через наявність оклюзії коронарних артерій. Після ЧКВ з імплантацією коронарних стентів усім хворим для запобігання ішемічним подіям, пов'язаним і не пов'язаним зі стентом, рекомендовано приймати подвійну антитромбоцитарну терапію (ПАТ) комбінацією ацетилсаліцилової кислоти (АСК) та інгібітора P2Y12-рецепторів тромбоцитів (клопідогрель у разі стабільної ІХС та один із потужніших антиагрегантів – прасугрель або тикагрелор – при гострому коронарному синдромі [ГКС]) упродовж 6–12 місяців (за відсутності високого ризику кровотеч) із подальшим переходом на монотерапію АСК [3]. Однак зараз панує думка, що в складних випадках (наприклад, після реваскуляризації за допомогою складного ЧКВ) у зв’язку з іще вищими ризиками небажаних подій застосування стандартної схеми може не забезпечувати достатнього рівня захисту, що призвело до пошуку варіантів покращення результативності застосованої після ЧКВ антиагрегантної терапії. Варіант із подовженням ПАТ понад 6–12 місяців вважається досить спірним, оскільки потенційно пов'язаний зі збільшенням частоти кровотеч і вищими рівнями захворюваності та смертності в цільовій когорті пацієнтів [4]. Інший варіант – короткострокова (1–3 місяці) ПАТ комбінацією АСК і потужного інгібітора P2Y12-рецепторів (іP2Y12) із подальшим скасуванням АСК і тривалою монотерапією потужним іP2Y12 – розглядають як перспективніший, оскільки дослідження показали, що застосування подібної схеми з іP2Y12 тикагрелором пов'язане зі зниженням частоти кровотеч без збільшення ризику серцево-судинних (СС) подій порівняно зі стандартною ПАТ [5]. Крім того, другий із зазначених варіантів також може бути застосований після ЧКВ у хворих на ЦД, оскільки в них стандартна схема може бути недостатньо ефективною у зв'язку з доведеною гіперактивністю тромбоцитів [6,7], що створює потребу в потужнішому антитромбоцитарному режимі, який забезпечить необхідний рівень антиіщемічного захисту, не спричиняючи зростання частоти кровотеч. Для обґрунтування застосування схеми на основі тикагрелору (короткострокова ПАТ комбінацією АСК + тикагрелор із подальшим переходом на довгострокову монотерапію тикагрелором) Wang et al. провели метааналіз результатів опублікованих досліджень, спрямований на оцінку результатів такої терапії в пацієнтів із ЦД 2 типу (ЦД2) після ЧКВ [8]. Основні відомості з цього метааналізу коротко подано нижче.
Методологія аналізу Wang et al. Для пошуку відповідних публікацій використовували такі електронні бази даних: MEDLINE, EMBASE, Web of Science, Google Scholar, Cochrane і база даних порталу ClinicalTrials. gov. Для аналізу підходили дослідження, присвячені порівнянню монотерапії тикагрелором після короткострокової ПАТ із подовженою ПАТ, у яких брали участь особи з ЦД2 після ЧКВ. У процесі пошуку використовували такі терміни/фрази: «тикагрелор і черезшкірне коронарне втручання», «монотерапія тикагрелором і черезшкірне коронарне втручання», «монотерапія тикагрелором і цукровий діабет і черезшкірне коронарне втручання», «інгібітори P2Y12 і черезшкірне коронарне втручання»; у цих пошукових фразах термін «черезшкірне коронарне втручання» також замінювали на «коронарна реваскуляризація», «коронарне стентування», «коронарна ангіопластика» й «ЧКВ» [8]. Загалом, для включення в аналіз підходили рандомізовані або спостережні дослідження, що проводилися за участю осіб із ЦД2, реєстрували несприятливі СС наслідки й кровотечі як клінічні кінцеві точки та були опубліковані англійською мовою. Дослідження з дизайном типу «випадок-контроль», метааналізи, систематичні огляди й огляди літератури, а також дослідження, у яких не брали участі пацієнти з ЦД2, дослідження, що проводилися без контрольної групи, і дослідження, опубліковані не англійською мовою, в аналізі не використовували [8]. Релевантними для аналізу вважали наслідки, про які повідомляли принаймні у двох різних включених дослідженнях. Отже, в аналізі Wang et al. оцінювали такі кінцеві точки: серйозні несприятливі серцеві події (MACE: смерть від будь-якої причини/смерть від серцевої причини, інфаркт міокарда [ІМ] і реваскуляризація), загальна смертність, смертність від серцевої причини, ІМ, повторна реваскуляризація (включно з реваскуляризацією цільової судини та реваскуляризацією цільового ураження), інсульт, тромбоз стента, великі й незначні кровотечі за класифікацією Thrombolysis in myocardial infarction (TIMI), кровотеча 2, 3 або 5 типу за визначенням Академічного консорціуму дослідників кровотеч (BARC), будь-які незначні кровотечі. Тривалість подальшого спостереження коливалася в діапазоні від 1 до 24 місяців. Як експериментальну терапію в більшості досліджень використовували 3-місячну ПАТ із подальшою 1–2-річною монотерапією тикагрелором [8]. Результати порівняння досліджуваних стратегій лікування представляли у вигляді відношень ризиків (ВР) із 95% довірчими інтервалами (ДІ). Для оцінки неоднорідності сукупностей даних використовували Q-критерій і I2-критерій. За I2 менше 50% в аналізі застосовували статистичну модель із фіксованим ефектом, в іншому випадку – статистичну модель із випадковим ефектом. Також проводили аналіз чутливості (з послідовним виключенням даних кожного включеного дослідження), щоб оцінити вплив даних окремих досліджень на загальні результати аналізу [8].

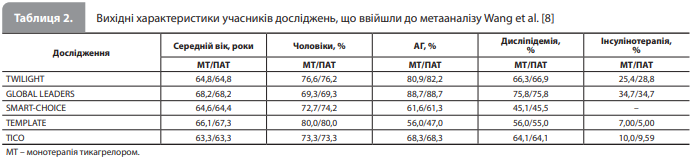
Результати метааналізу Wang et al. У результаті пошуку та застосування критеріїв включення й включення в метааналіз увійшли п'ять досліджень, що відповідали всім переліченим вимогам (табл. 1) [8]. Загалом, в аналіз включено дані 8621 пацієнта з ЦД2, із яких 4357 отримували монотерапію тикагрелором, а 4264 – ПАТ. Більшість учасників були чоловіками (69,3–80,0%), середній вік варіювався в діапазоні 63,3–68,2 року, середні показники за основними вихідними характеристиками учасників наведено в таблиці 2 [8].
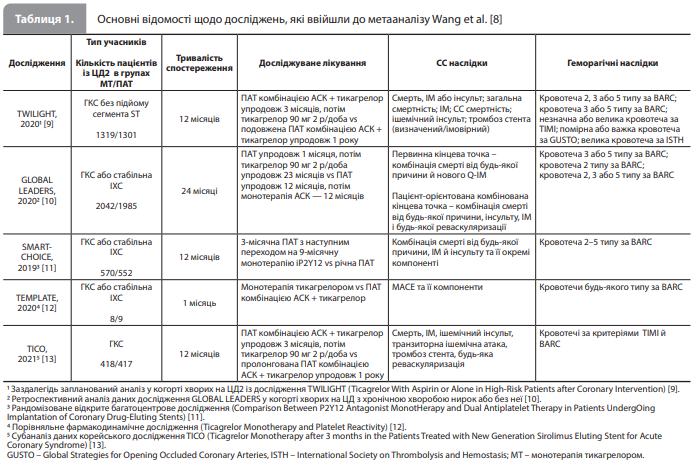
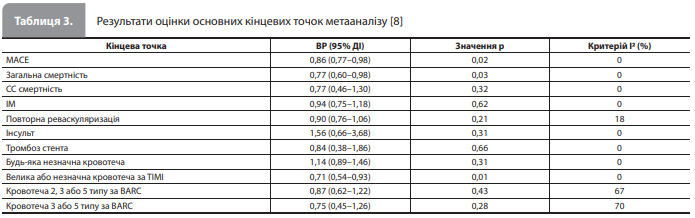
Проведений аналіз показав, що порівняно з тривалою ПАТ монотерапія тикагрелором після короткого курсу ПАТ пов'язана зі значно нижчими ризиком MACE (ВР 0,86, 95% ДІ 0,77–0,98; р=0,02) і рівнем загальної смертності (ВР 0,77, 95% ДІ 0,60–0,98; р=0,03; рис. 1) без істотних відмінностей між досліджуваними стратегіями за рівнями смертності від СС причин (ВР 0,77, 95% ДІ 0,46–1,30; р=0,32) і ризиками ІМ (ВР 0,94, 95% ДІ 0,75–1,18; р=0,62), інсульту (ВР 0,84, 95% ДІ 0,66–3,68; р=0,31), тромбозу стента (ВР 0,84, 95% ДІ 0,38– 1,86; р=0,66) або повторної реваскуляризації (ВР 0,90, 95% ДІ 0,76–1,06; р=0,21; рис. 1) [8] Водночас перехід на монотерапію тикагрелором після короткострокової ПАТ був пов'язаний зі значно нижчим ризиком великих або незначних кровотеч за критеріями TIMI (ВР 0,71, 95% ДІ 0,5–0,93; р=0,01) порівняно з тривалою ПАТ (рис. 2), тоді як показники частоти решти геморагічних кінцевих точок були зіставними в групах лікування (будь-яка незначна кровотеча – ВР 1,14, 95% ДІ 0,89–1,46, р=0,31; кровотеча 2, 3 або 5 типу за BARC – ВР 0,87, 95% ДІ 0,62–1,22, р=0,43; кровотеча 3 або 5 типу за BARC – ВР 0,75, 95% ДІ 0,45–1,26, р=0,28) (табл. 3) [8]. Аналіз чутливості показав, що основний внесок у результат оцінки ризику великих або незначних кровотеч за критеріями TIMI забезпечило дослідження TWILIGHT [9]; результати оцінки решти наслідків були послідовними та узгоджувалися з результатами загального аналізу [8]


Обговорення результатів метааналізу Wang et al. Результати метааналізу Wang et al. показали, що нова стратегія антиагрегантної терапії у вигляді довготривалої монотерапії тикагрелором після короткого курсу ПАТ, яка є доведено ефективною в загальній популяції пацієнтів із ІХС після ЧКВ, забезпечує сприятливі наслідки й у підмножині цієї популяції, яка складається з хворих на ЦД2. Зокрема, порівняно з подовженою ПАТ довготривала монотерапія тикагрелором асоціюється зі значно нижчими ризиками MACE, смерті від усіх причин і комбінації великих і незначних кровотеч за критеріями TIMI. Ці результати узгоджуються з висновками низки попередніх досліджень, субдосліджень і метааналізів, згідно з якими довготривала монотерапія тикагрелором після короткострокової ПАТ асоціюється зі значно нижчим ризиком великих кровотеч без зростання ризику ішемічних подій [14–16], у тому числі серед пацієнтів із ЦД2 [17]. Разом із результатами метааналізу 8 рандомізованих досліджень, який показав, що в когорті пацієнтів із ЦД2, які перенесли ЧКВ, застосування ПАТ на основі тикагрелору ефективніше знижує ризик МАСЕ, не збільшуючи загальний ризик кровотеч, порівняно з ПАТ на основі прасугрелю або клопідогрелю [18], результати Wang et al. підтримують внесення відповідних змін до діючих практичних рекомендацій з антитромбоцитарної терапії в пацієнтів із групи високого ризику (зокрема й із ЦД), які перенесли ЧКВ. Результати представленого метааналізу слід розглядати з урахуванням низки обмежень, таких як порівняно невелика кількість включених досліджень й учасників, різна тривалість періодів подальшого спостереження, різна тривалість ПАТ (1–3 місяці) в експериментальних групах досліджень і сукупна оцінка великих і незначних кровотеч за критеріями TIMI (без окремих аналізів для оцінки ризику кожного з цих типів кровотеч), оскільки ці обмеження в теорії могли вплинути на результати метааналізу.
Висновки Отже, за даними метааналізу результатів п'яти рандомізованих порівняльних досліджень, у пацієнтів із ЦД 2 типу, які пройшли ЧКВ, тривала монотерапія тикагрелором після короткого курсу ПАТ показала кращі результати, ніж подовжена ПАТ. Незважаючи на потребу в подальшому вивченні цієї стратегії у великих добре організованих клінічних дослідженнях, схему з раннім (після 3-місячної ПАТ) переходом на монотерапію тикагрелором після ЧКВ уже зараз можна охарактеризувати як значний крок на шляху до оптимальної антиагрегантної терапії для хворих із поєднанням ЦД та ІХС.
Список літератури знаходиться в редакції
Автор огляду Наталія Генш |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2026. Усі права захищені.
|
мапа сайту корисні посилання |