У пошуках оптимальної антиагрегантної стратегії після складного ЧКВ — рання відміна ацетилсаліцилової кислоти vs стандартна ПАТ: результати великомасштабного метааналізуПацієнти, які проходять складне черезшкірне коронарне втручання (ЧКВ), відрізняються підвищеним ризиком ішемічних подій і, як наслідок, часто отримують тривалу подвійну антитромбоцитарну терапію (ПАТ) з метою довгострокового захисту від атеротромбозу [1–3]. Така стратегія здебільшого ґрунтується на результатах ретроспективного аналізу даних 9577 учасників шести рандомізованих клінічних досліджень (РКД), у якому довгострокова ПАТ (≥1 року), що призначалася замість 3- або 6-місячної ПАТ з подальшою монотерапією ацетилсаліциловою кислотою (АСК), асоціювалась із більшим зниженням ішемічного ризику серед пацієнтів після складного ЧКВ [4]. Однак за даними пізнішого аналізу даних 14 963 учасників восьми РКД, розділених на страти з урахуванням складності ЧКВ (складне vs нескладне), переваги довготривалої ПАТ, пов’язані із захистом проти ішемічних подій, проявлялися тільки за відсутності ознак високого ризику кровотечі як після складного, так і після нескладного ЧКВ [5]. Більше того, у субаналізі даних РКД, у якому брали участь особи з високим ризиком кровотечі, місячна ПАТ із подальшою антитромбоцитарною монотерапією (переважно інгібітором P2Y12-рецепторів тромбоцитів [іP2Y12]) і стандартна ПАТ продемонстрували зіставні показники частоти розвитку основних несприятливих серцевих або церебральних подій серед пацієнтів, які пройшли складне або нескладне ЧКВ [6, 7]. Загалом, скасування АСК після ПАТ тривалістю 1–3 місяці з подальшим прийманням іP2Y12 у вигляді монотерапії сприятливо впливає на баланс між ризиками кровотечі та ішемії серед невідібраних хворих після коронарної реваскуляризації [8, 9], що підтверджено низкою досліджень. Зокрема, у метааналізі індивідуальних даних (ІД) 23 308 учасників шести РКД (дослідження Sidney–2 [8]) порівняння цієї стратегії зі стандартною ПАТ продемонструвало зіставні показники частоти смертельних та ішемічних подій і більш низький ризик великих кровотеч у разі раннього скасування АСК. Як наслідок, у міжнародних настановах застосування укороченої ПАТ із подальшим переходом на монотерапію іP2Y12 рекомендовано використовувати як альтернативний підхід [1–3]. Проте ретроспективні аналізи окремих досліджень [10–14] так і не дозволили остаточно оцінити баланс між безпекою та ефективністю раннього переходу з ПАТ на монотерапію іP2Y12 у пацієнтів, які перенесли складне ЧКВ, через що зберігаються побоювання стосовно потенційних шкідливих наслідків раннього скасування АСК у групах високого ризику. Для роботи з цими побоюваннями та оцінки співвідношення «користь/ризик» описаної стратегії у хворих після ЧКВ різного ступеня складності Gragnano et al. провели аналіз у підгрупах складного й нескладного ЧКВ, використовуючи ІД учасників дослідження Sidney–2 та інформацію про наслідки, централізовано підтверджені комісією експертів [8, 15].
Методологія дослідження Gragnano et al. Проєкт Sidney–2 був метааналізом ІД учасників РКД, що проводили для порівняння ефектів монотерапії іP2Y12 і ПАТ за даними централізованого оцінювання результатів лікування в пацієнтів після коронарної реваскуляризації [8]. Водночас, Gragnano et al. у своєму аналізі порівнювали ефективність і безпечність двох досліджуваних антитромбоцитарних стратегій – стандартної ПАТ і монотерапії іP2Y12 після початкової 1–3-місячної ПАТ – у пацієнтів, які перенесли складне й нескладне ЧКВ, виключивши для цього з бази даних проєкту Sidney–2 хворих, які не проходили ЧКВ. На проведення складного ЧКВ вказувала наявність щонайменше однієї з таких ангіографічних ознак: втручання на трьох судинах, імплантація ≥3 стентів, втручання на ≥3 патологічних вогнищах, загальна довжина стента >60 мм, біфуркаційне ураження з імплантацією ≥2 коронарних стентів або хронічна повна оклюзія як цільове ураження. Крім основного аналізу було виконано аналіз чутливості, для чого використовували альтернативне розширене визначення складного ЧКВ, яке додатково охоплює використання пристроїв для атеректомії, втручання на лівій коронарній артерії або втручання на коронарному шунті. Первинною кінцевою точкою ефективності в аналізі Gragnano et al. була комбінація смертності від усіх причин, інфаркту міокарда (ІМ) та інсульту впродовж усього періоду рандомізованого порівняння двох варіантів антитромбоцитарної терапії (монотерапія іP2Y12 vs продовження ПАТ). Основною кінцевою точкою безпечності була кровотеча 3 або 5 типу за класифікацією Консорціуму з вивчення кровотеч (Bleeding Academic Research Consortium, BARC). Вторинні кінцеві точки включали окремі компоненти первинної кінцевої точки, смертність від серцево-судинних (СС) та несерцево-судинних (неСС) причин, ішемічний і геморагічний інсульти, доведений та/або ймовірний тромбоз стента, кровотечу за класифікаціями BARC і Thrombolysis In Myocardial Infarction (TIMI), а також сукупну кількість несприятливих клінічних подій (net adverse clinical events, NACE: сукупність подій, що входять до первинної кінцевої точки ефективності й основної кінцевої точки безпечності). Усі події оцінювали централізовано. Визначення кінцевих точок у різних РКД, що увійшли до аналізу, здебільшого збігалися.

У дослідженні було передбачено одночасний аналіз даних усіх включених РКД за допомогою регресійної моделі Кокса зі змішаним ефектом, стратифікованої за РКД. Первинний аналіз проводили у вибірці рандомізованих пацієнтів (експериментальна група – група раннього переходу з ПАТ на монотерапію іP2Y12, контрольна група – група стандартної ПАТ) на підставі даних про клінічні події, які відбулися після передбаченого протоколом РКД моменту переходу з ПАТ на монотерапію іP2Y12 в експериментальній групі. Усі події, що відбулися до моменту такого переходу в обох групах, цензурували. Ефект лікування оцінювали за допомогою обчислення відношень ризиків (ВР) і 95% довірчих інтервалів (ДІ). Використовували дані, зібрані за періоди до завершення максимальної обумовленої протоколом відповідного РКД тривалості монотерапії іP2Y12 і стандартної ПАТ в експериментальній і контрольній групах відповідно. Вищезазначений аналіз чутливості проводили з використанням моделі випадкових ефектів ДерСимоніана-Лерда. Для оцінки узгодженості виявлених відмінностей між монотерапією іP2Y12 і стандартною ПАТ у підгрупах складного й нескладного ЧКВ використовували формальну перевірку взаємодії. Додаткові аналізи проводили шляхом стратифікації пацієнтів відповідно до окремих компонентів визначення складного ЧКВ і кількості таких компонентів. Усі критерії були двосторонніми, на статистичну значущість результату порівняння вказувало значення р<0,05.
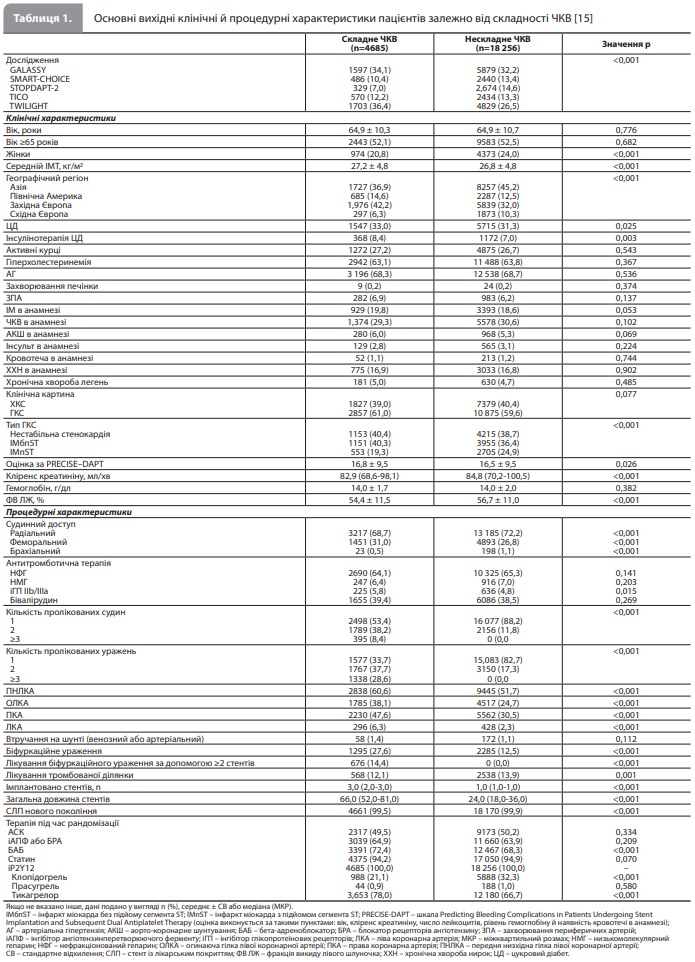
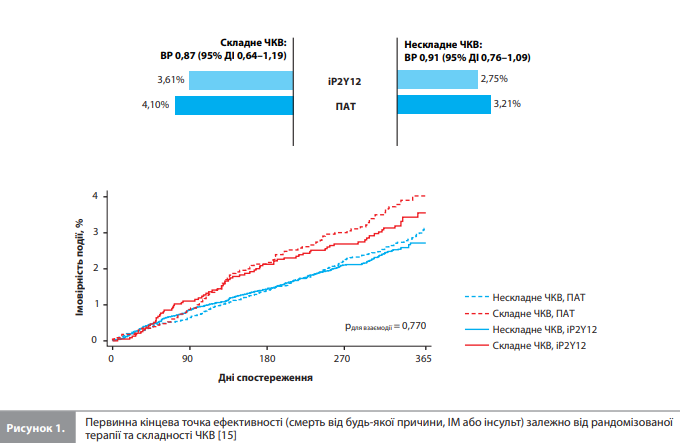
Результати дослідження Gragnano et al. Спочатку в базі даних Sidney-2 містилися ІД 23 308 пацієнтів із шести РКД. Після виключення даних усіх 334 учасників (1,4% від загальної вибірки) одного дослідження (оскільки вони перенесли хірургічну реваскуляризацію [16]) і 33 учасників (0,14%) іншого дослідження (оскільки вони не пройшли ЧКВ після рандомізації [17]) когорта дослідження Gragnano et al. включала 22 941 пацієнта з п’яти РКД, з яких 4685 (20,4%) перенесли складне і 18 256 (79,6%) нескладне ЧКВ. Поширеність ознак складності в підгрупі складного ЧКВ була такою: втручання на трьох судинах – 8,4%, імплантація ≥3 стентів – 40,4%, втручання на ≥3 патологічних вогнищах – 28,6%, загальна довжина стента >60 мм – 63,9%, біфуркаційне ураження з ≥2 імплантованими стентами – 14,4%, хронічна повна оклюзія як цільове ураження – 11,1% [15]. Початкові клінічні й процедурні характеристики пацієнтів зі складним і нескладним ЧКВ представлені в таблиці 1 [15]. Середній вік учасників становив 64,9 року в обох групах лікування. Пацієнти, які перенесли складне ЧКВ, частіше були чоловіками, у них частіше був цукровий діабет, частіше діагностували гострий ІМ без підйому сегмента ST і рідше – ІМ із підйомом сегмента ST порівняно з пацієнтами з нескладним ЧКВ. На відміну від вихідних клінічних характеристик, добре збалансованих у групах, виділених з урахуванням рандомізованого лікування й складності ЧКВ, за процедурними характеристиками групи складного та нескладного ЧКВ були значною мірою незбалансовані, що пояснюється очевидними причинами (різною складністю процедури в цих групах). Медіана тривалості спостереження становила 334 дні (діапазон 275–365 днів) [15]. В аналізі кінцевих точок ефективності залежно від складності ЧКВ отримали такі результати. Первинна кінцева точка ефективності (смерть від будь-якої причини, ІМ або інсульт) частіше реєструвалася в групі складного ЧКВ порівняно з групою нескладного ЧКВ (3,86 vs 2,98%, ВР 1,28, 95% ДІ 1,04–1,59, р=0,02). Ризик основної кінцевої точки безпчності (кровотечі 3 або 5 типу за BARC) був чисельно, але статистично незначуще вищим серед пацієнтів, які перенесли складне ЧКВ (1,66 vs 1,31%, ВР 1,18, 95% ДІ 0,87–1,59, р=0,292). Показники інших вторинних кінцевих точок були загалом чисельно, але статистично незначуще вищими за умов проведення складного ЧКВ [15]. Аналіз кінцевих точок ефективності залежно від рандомізованого лікування й складності ЧКВ показав такі результати (табл. 2) [15]. Події первинної кінцевої точки ефективності відбулися в 3,61 і 2,75% пацієнтів, які отримували монотерапію іP2Y12, і у 4,1 і 3,21% пацієнтів, які отримували стандартну ПАТ, у групі складного (ВР 0,87, 95% ДІ 0,64–1,19, р=0,379) і нескладного (ВР 0,91, 95% ДІ 0,76–1,09, р=0,299) ЧКВ відповідно без ознак значущої взаємодії між ефектом лікування та складністю ЧКВ (рдля взаємодії = 0,770) (рис. 1) [15]. Серед пацієнтів, які перенесли складне та нескладне ЧКВ, ризики смерті від будь-якої причини, СС смерті, ІМ, інсульту й доведеного або ймовірного тромбозу стента на тлі двох досліджуваних видів антитромбоцитарної терапії були зіставними; ознаки взаємодії між ефектом лікування й складністю ЧКВ для цих ішемічних кінцевих точок також не виявлені (табл. 2) [15]. Ефект монотерапії іP2Y12, розпочатої після 1- або 3-місячної ПАТ, на ризик подій первинної кінцевої точки ефективності порівняно зі стандартною ПАТ був стабільним за наявності будь-яких критеріїв із визначення складного ЧКВ і будь-якої кількості цих критеріїв [15].
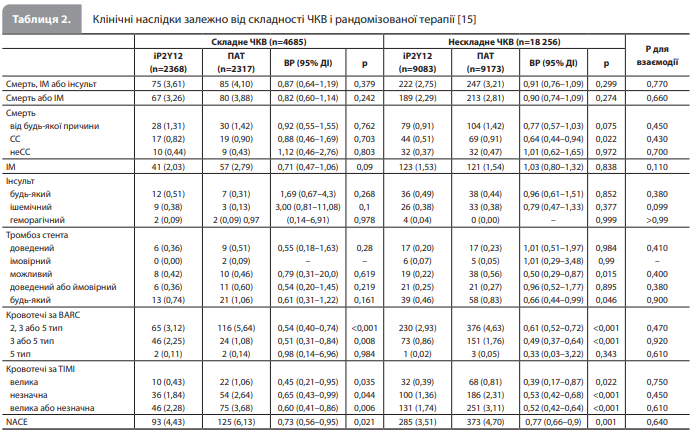
При аналізі результатів терапії в підгрупах усередині групи складного ЧКВ ефект лікування загалом був стабільним; аналогічний аналіз у групі нескладного ЧКВ показав наявність взаємодії між лікуванням і статтю (рдля взаємодії = 0,010), що свідчить про те, що монотерапія іP2Y12 знижує ризик первинної кінцевої точки ефективності порівняно зі стандартною ПАТ в жінок (ВР 0,59, 95% ДІ 0,40–0,87), але не в чоловіків (ВР 1,03, 95% ДІ 0,84–1,27). Відповідне значення number-needed-to-treat to benefit (NNTB, кількість хворих, яких потрібно пролікувати для досягнення корисного ефекту) серед пацієнток дорівнювало 66 (95% ДІ 40–200). Проте під час стратифікації пацієнтів за статтю з подальшою оцінкою компонентів первинної кінцевої точки серед чоловіків і жінок не була виявлена значна взаємодія між статтю пацієнтів і ризиком окремих наслідків [15]. Аналіз кінцевих точок ефективності залежно від тривалості ПАТ (1 vs 3 місяці після ЧКВ) перед переходом на антиагрегантну монотерапію, проведений в експериментальній групі, не виявив ознак впливу термінів скасування ПАТ на ефект послідуючої монотерапії іP2Y12. Крім того, ефекти монотерапії іP2Y12 на первинну кінцеву точку та її компоненти були однаковими при використанні клопідогрелю й нових іP2Y12 (тикагрелор, прасугрель), незалежно від складності ЧКВ. Цікаво, що подальші вторинні аналізи в підгрупах, проведені окремо для досліджень, що застосовували клопідогрель, і досліджень, що застосовували тільки нові іP2Y12, показав, що в першому випадку ефект монотерапії іP2Y12 був стабільним у всіх досліджуваних підгрупах, а в другому стать пацієнта взаємодіяла з ефектом лікування після нескладного ЧКВ (рдля взаємодії = 0,027) [15]. Аналіз кінцевих точок безпечності залежно від рандомізованого лікування й складності ЧКВ показав, що монотерапія іP2Y12 значно знижувала ризик основної кінцевої точки безпечності – кровотечі 3 або 5 типу за BARC – порівняно зі стандартною ПАТ серед пацієнтів після складного (1,08 vs 2,25%, ВР 0,51, 95% ДІ 0,31–0,84, р<0,008; NNTB 83, 95% ДІ 50–250) і нескладного (0,86 vs 1,76%, ВР 0,49, 95% ДІ 0,37–0,64, р<0,001; NNTB 111, 95% ДІ 76–200) ЧКВ без ознак залежності ефекту лікування від складності ЧКВ (рдля взаємодії = 0,920) (рис. 2) [15]. Аналогічним чином, переваги монотерапії іP2Y12 перед стандартною ПАТ були значними й при оцінці інших геморагічних кінцевих точок, а також при аналізі ефекту терапії на NACE і теж без ознак залежності ефекту лікування від складності ЧКВ (табл. 2, рис. 3) [15].


Аналізи чутливості й вторинні аналізи загалом підтвердили результати первинних аналізів досліджуваних кінцевих точок ефективності та безпечності. Зокрема, аналіз подій первинної кінцевої точки ефективності, що сталися протягом перших 9 місяців монотерапії іP2Y12 в експериментальній групі (проводили для вирівнювання тривалості спостереження в різних дослідженнях), показав стабільність ефектів лікування незалежно від складності ЧКВ (ВР після складного ЧКВ – 0,89, 95% ДІ 0,63–1,25, р=0,487; ВР після нескладного ЧКВ – 0,92, 95% ДІ 0,76–1,12, р=0,428; рдля взаємодії = 0,830). Крім того, ефект лікування не залежав від клінічної форми коронарної патології та був однаковим у пацієнтів із гострим і хронічним коронарними синдромами [15].
Обговорення результатів дослідження Gragnano et al. Отже, Gragnano et al. провели метааналіз ІД 22 941 учасника п’яти РКД, що пройшли ЧКВ із використанням коронарних стентів із лікарським покриттям (СЛП), для порівняння ефектів монотерапії іP2Y12, розпочатої після ПАТ тривалістю 1–3 місяці, з ефектами стандартної ПАТ за даними централізованого оцінювання зареєстрованих подій і з урахуванням складності ЧКВ. У результаті дійшли таких висновків [15]: 1. Пацієнти після складного ЧКВ відрізнялися значно вищим ризиком ішемічних подій і чисельно вищою частотою кровотеч порівняно з хворими після нескладного ЧКВ. 2. Ризики смерті й ішемічних подій були зіставними при застосуванні монотерапії іP2Y12 і стандартної ПАТ незалежно від складності ЧКВ; утім вплив монотерапії іP2Y12 на ризики смерті та ішемічних подій не залежав від наявних критеріїв складності ЧКВ, застосованого іP2Y12 і показань до ЧКВ. 3. Монотерапія іP2Y12 значно знижувала ризик великої кровотечі й частоту подій NACE порівняно зі стандартною ПАТ; величина цього ефекту була зіставною серед пацієнтів після складного та нескладного ЧКВ. 4. Результати первинних аналізів дістали підтвердження в аналізах у підгрупах і аналізах чутливості, що підтвердили стійкі переваги монотерапії іP2Y12 з погляду зниження ризику кровотечі порівняно зі стандартною ПАТ без шкоди для антиішемічного захисту. З урахуванням отриманих результатів, автори дослідження рекомендують при виборі антитромбоцитарної стратегії для застосування після складного ЧКВ брати до уваги такі фактори. Насамперед, варто враховувати, що, хоча чинні міжнародні рекомендації (клас I) щодо застосування 6–12-місячної ПАТ у пацієнтів після ЧКВ незалежно від клінічної картини [1–3] ґрунтуються на доказах потенційного зниження ризику пов’язаних зі стентами й спонтанних ішемічних подій (який вважається підвищеним у пацієнтів із розповсюдженим ураженням коронарного русла та складним стентуванням) при збільшенні тривалості ПАТ, отриманих у великих РКД і реєстрах [1–4, 18, 19], впровадження СЛП нового покоління значно знизило частоту ускладнень, пов’язаних зі стентами, які тепер відповідальні за меншість рецидивів ішемії після коронарної реваскуляризації [20, 21]. Відтак, наразі користь від антитромбоцитарної терапії в основному зумовлена запобіганням тромботичним подіям у нестентованих сегментах коронарного русла й некоронарних судинах [21], у зв’язку з чим надлишково інтенсивна та/або тривала ПАТ може порушувати баланс між зниженням ішемічного ризику та збільшенням ризику кровотечі [1–7, 22] і таким чином чинити потенційний несприятливий вплив на подальшу смертність. Крім того, пацієнти, які відповідають критеріям складного ЧКВ, зазвичай мають супутні захворювання, що додатково підвищують ризик кровотечі й можуть діяти як фактори, що обмежують тривалість ПАТ [5, 7]. Отже, останні дані свідчать про те, що складність ЧКВ сама по собі не виправдовує більш тривалу ПАТ, і що основою для вибору оптимальної стратегії антитромбоцитарної терапії після складного ЧКВ має бути загальна оцінка співвідношення «користь/ризик» у конкретного пацієнта [5, 7, 15]. Представлене дослідження є найбільшим аналізом ефектів відміни АСК після 1 або 3 місяців ПАТ із продовженням монотерапії іP2Y12 порівняно зі стандартною ПАТ з урахуванням складності ЧКВ. Отримані результати показують, що незалежно від складності ЧКВ, типу іP2Y12 і часу відміни АСК після ЧКВ (через 1 або 3 місяці), перехід на монотерапію пероральним іP2Y12 не пов’язаний із небажаними наслідками, оскільки не підвищує ризиків смерті та ішемічних подій, зокрема ІМ і тромбозу стента, порівняно зі стандартною ПАТ [15]. Автори вважають, що на окрему увагу заслуговують результати, що спостерігалися в жінок, які загалом узгоджуються з незалежним від складності ЧКВ зниженням загальної й СС смертності серед пацієнток, які отримували монотерапію іP2Y12, у попередньому дослідженні, проведеному цим же колективом учених [8]. В описаному метааналізі зниження зазначених ризиків серед жінок, які перенесли складне й нескладне ЧКВ, становило 63 і 53% – для загальної смертності та 73 і 66% – для СС смертності відповідно, і у всіх випадках зниження ризику було статистично значущим. Проте аналіз взаємодії між статтю пацієнтів і ефектом монотерапії іP2Y12 порівняно зі стандартним ПАТ підтвердив значущу взаємодію тільки в когорті нескладного ЧКВ, що може пояснюватися помилкою 2 роду, що стала наслідком необхідності проведення аналізу «підгруп у складі підгруп» (підгруп за ознакою статі у складі підгруп за ознакою складності ЧКВ). Цей висновок підтверджується тим, що за даними точкових оцінок, зниження загальної та СС смертності серед жінок було більш вираженим після складного, ніж після нескладного ЧКВ, і вказує на необхідність подальшого вивчення цього феномена [15]. Оцінка ризику геморагічних подій показала значне й стійке зниження частоти великих кровотеч при монотерапії іP2Y12 порівняно зі стандартною ПАТ; відносне зниження ризику становило близько 50% і було зіставним у підгрупах пацієнтів зі складним та нескладним ЧКВ. Аналізи в підгрупах показали, що спостережуваний ефект монотерапії іP2Y12 на ризик кровотечі був стійким і відтворюваним у різних підгрупах та потенційно більш значущим у пацієнтів із гострими коронарними синдромами, що узгоджується з попередніми спостереженнями [23]. Загалом, результати метааналізу Gragnano et al. ставлять під сумнів незаперечність значущості продовження ПАТ по завершенні 1–3-місячного періоду після ЧКВ і підтримують перехід до раннього початку монотерапії іP2Y12, незалежно від складності процедури. Слід також зазначити, що, хоча ефект лікування в метааналізі залишався стабільним незалежно від типу іP2Y12, у досліджуваній вибірці тикагрелор отримувала більша кількість пацієнтів, ніж прасугрель, а результати монотерапії клопідогрелем оцінювали тільки в азійських когортах і тільки порівняно з ПАТ на основі клопідогрелю. Тому необхідно продовжити оцінку впливу типу іP2Y12 на співвідношення «користь/ризик» під час порівняння монотерапії іP2Y12 і стандартної ПАТ після складного й нескладного ЧКВ [15]. Слід зазначити, що представлений об’єднаний аналіз даних п’яти РКД розширює й доповнює результати більш ранніх ретроспективних метааналізів та аналізів окремих досліджень [10–14] завдяки більшій кількості учасників (що дозволило досягти більш точної оцінки ішемічного й геморагічного ризиків у підгрупі складного ЧКВ), централізованій оцінці результатів (що знижує ризик неправильної класифікації подій), використанню двох чітко визначених наборів критеріїв складності ЧКВ, а також виключенню з оцінки подій, зареєстрованих під час загального для експериментальної та контрольної груп періоду початкової ПАТ (в результаті, у когорті складного ЧКВ було цензуровано 35% усіх подій первинної кінцевої точки, 48% випадків СС смерті, 63% випадків доведеного або ймовірного тромбозу стентів і 41% кровотеч 3 або 5 типу за BARC, що відбулися протягом періоду початкової ПАТ і, отже, не мали братися до уваги при оцінці ризиків і переваг раннього скасування АСК та переходу на монотерапію іP2Y12) [15]. Результати представленого дослідження потрібно інтерпретувати з урахуванням можливих обмежень, таких як відкритий дизайн чотирьох із п’яти включених РКД, власний дизайн дослідження Gragnano et al. (субаналіз на основі метааналізу ІД), недостатня статистична потужність порівнянь у когорті складного ЧКВ для формулювання остаточних висновків щодо ефектів монотерапії іP2Y12 порівняно зі стандартною ПАТ, а також невелика кількість пацієнтів у деяких підгрупах (наприклад, у підгрупі пацієнтів, що пройшли атеректомію). Унаслідок цих обмежень результати дослідження Gragnano et al. слід розглядати як гіпотези та підтверджувати в подальших рандомізованих дослідженнях [15].
Висновки Загалом, згідно з результатами аналізу індивідуальних даних учасників п’яти РКД, які перенесли ЧКВ, безперервна стандартна ПАТ і рання (після 1–3 місяців ПАТ) відміна АСК із продовженням монотерапії пероральним іP2Y12 асоціюються із зіставними ризиками комбінації ІМ, інсульту й смерті від будь-якої причини, незалежно від складності ЧКВ. Утім порівняно з продовженням ПАТ перехід на монотерапію іP2Y12 був пов’язаний зі значним зниженням ризику великих кровотеч і NACE, зіставним у когортах пацієнтів після складного й нескладного ЧКВ.
Список літератури знаходиться в редакції
Автор огляду Віктор Мицьо Medicine Review 2023; 3 (70): 8 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2025. Усі права захищені.
|
мапа сайту корисні посилання |