Оцінка впливу параметрів фонової терапії на ефективність і безпечність емпагліфлозину при серцевій недостатності: результати ретроспективного аналізу даних дослідження EMPEROR-ReducedЯк відомо, у клінічних дослідженнях нових методів лікування, зокрема фармакотерапії серцевої недостатності (СН), досліджувані препарати додають до оптимальної стандартної терапії, що дає змогу оцінити «додаткову» користь нових препаратів. Однак в умовах лікування хворих із СН і зниженою фракцією викиду (ФВ) лівого шлуночка (СНзнФВ) доволі поширеною є ситуація, коли пацієнту з тієї чи іншої причини не вдається досягти цільової дози одного або кількох препаратів стандартної терапії [1, 2]. У результаті виникає питання про користь призначення нових препаратів особам, які не отримують цільові дози стандартних препаратів для лікування СН [3]. Одним з останніх великих досліджень новітніх препаратів у контексті СНзнФВ стало дослідження EMPEROR-Reduced (Empagliflozin Outcome Trial in Patients with Chronic Heart Failure and Reduced Ejection Fraction), спрямоване на оцінку ефектів інгібітора натрійзалежного котранспортера глюкози 2 типу (іНЗКГТ2) емпагліфлозину порівняно з плацебо. Як показали результати, емпагліфлозин забезпечив зниження ризику комбінованої кінцевої точки, що включала смерть від серцево-судинних (СС) причин і госпіталізацію з приводу СН, серед учасників дослідження порівняно з плацебо [4]. Крім того, емпагліфлозин знизив загальну частоту госпіталізацій із приводу СН і ризик серйозних несприятливих ниркових наслідків, а також сприяв зниженню функціонального класу СН за класифікацією Нью-Йоркської кардіологічної асоціації (NYHA) та поліпшенню стану здоров'я, при цьому ефект препарату не залежав від наявності у хворих цукрового діабету, для лікування якого спочатку розробляли емпагліфлозин [4–7]. Критерії відбору пацієнтів у EMPEROR-Reduced вимагали, щоб учасники отримували терапію СН, але без зазначення конкретних доз або конкретних препаратів. Тому дані з цього дослідження дають змогу визначити, чи залежить корисний ефект емпагліфлозину від вибору конкретних препаратів для фонової терапії СН (зокрема інгібітора ангіотензинперетворюючого ферменту [АПФ], блокатора рецепторів ангіотензину II [БРА], інгібітора неприлізину/рецепторів ангіотензину [ARNI], β-блокатора [БАБ] і антагоніста мінералокортикоїдних рецепторів [АМР]) та від величини доз (цільова або нижча за цільову) цих препаратів. Задля пошуку відповіді на це запитання колектив учених Verma et al. провів ретроспективний аналіз результатів EMPEROR-Reduced, під час якого вивчали ефективність і безпечність емпагліфлозину в пацієнтів, які приймали перераховані вище фонові препарати в різних комбінаціях у дозах, які становили більшу або меншу за половину (50%) від цільових доз [8].
Методологія ретроспективного аналізу Verma et al. У дослідженні EMPEROR-Reduced брали участь пацієнти із СН, ФВ лівого шлуночка (ФВ ЛШ) ≤40% і симптомами II–IV функціонального класу за NYHA, яких рандомізували в співвідношенні 1:1 для лікування емпагліфлозином у дозі 10 мг/добу або плацебо на додаток до фонової терапії СН [4]. У дослідженні взяли участь 520 дослідницьких центрів із 20 країн Азії, Австралії, Європи, Північної й Південної Америки. Учасники EMPEROR-Reduced належали до категорії високого ризику, про що свідчило виражене підвищення рівня N-термінального фрагмента попередника мозкового натрійуретичного пептиду (NT-proBNP), який перевищував порогове значення, що залежало від величини ФВ ЛШ (≥600 пг/мл – для пацієнтів з ФВ ЛШ ≤30%, а також для пацієнтів із ФВ ЛШ ≤40% і перенесеною за останні 12 місяців госпіталізацією з приводу СН; ≥1000 пг/мл – для пацієнтів із ФВ ЛШ 31–35% і ≥2500 пг/мл – для пацієнтів із ФВ ЛШ 36–40%) і наявності/відсутності фібриляції передсердь (для хворих із фібриляцією передсердь порогові рівні NT-proBNP подвоювалися). Під час дослідження дозволялося додавання, скасування або зміна дози фонових препаратів для лікування СН на розсуд лікарів. Основними критеріями виключення були симптоматична гіпотензія або систолічний артеріальний тиск (САТ) <100 мм рт. ст., а також розрахункова швидкість клубочкової фільтрації (рШКФ) <20 мл/хв/1,73 м2 [4]. Первинною кінцевою точкою дослідження EMPEROR-Reduced був час до першої госпіталізації з приводу СН або СС смерті; основною вторинною кінцевою точкою була кількість загальних (перших і повторних) госпіталізацій з приводу СН. У межах свого аналізу для реєстрації внутрішньолікарняних і позалікарняних подій, пов'язаних із погіршенням перебігу СН, Verma et al. використовували розширену комбіновану кінцеву точку, яка включала СС смерть, госпіталізацію з приводу СН, термінові візити до лікаря з приводу погіршення перебігу СН, яке вимагало терапії з внутрішньовенним введенням препаратів, а також амбулаторну інтенсифікацію терапії пероральними діуретиками у зв'язку з погіршенням перебігу СН в інтервалі між плановими візитами до лікаря. Ефекти емпагліфлозину порівнювали з плацебо в пацієнтів, які отримували ІАПФ, БРА, БАБ та АМР у дозах, більших і менших за 50% від цільових (під час дослідження не проводили послідовної реєстрації доз ARNI). Крім того, ефект лікування емпагліфлозином порівнювали в пацієнтів, які отримували й не отримували на вихідному рівні дослідження такі терапевтичні комбінації: 1) ІАПФ/БРА/ARNI + БАБ – обидва препарати в будь-якій дозі; 2) ІАПФ/БРА + БАБ – обидва препарати в дозі, що становить ≥50% від цільової; 3) ІАПФ/БРА/ARNI + БАБ + АМР – усі препарати в будьякій дозі; 4) ІАПФ/БРА + БАБ + АМР – усі препарати в дозі, що становить ≥50% від цільової, і 5) ARNI + БАБ + АМР – усі препарати в будь-якій дозі [8].

Для узагальнення вихідних характеристик учасників дослідження використовували середні значення, стандартні відхилення (СВ), медіану й міжквартильний розмах (МКР), а також показники абсолютної (n) і відносної (%) кількості. Результати аналізу первинної комбінованої та розширеної комбінованої кінцевих точок було представлено у вигляді відношень ризиків (ВР) і відповідних 95% довірчих інтервалів (ДІ), розрахованих за допомогою моделі пропорційних ризиків Кокса з поправкою на попередньо визначені коваріати: вік, рШКФ, регіон, статус цукрового діабету, стать і ФВ ЛШ. В аналізі загальної кількості (перша і повторні) госпіталізацій із приводу СН міжгрупові відмінності оцінювали за допомогою об’єднаної моделі, що враховує індивідуальну вразливість пацієнтів (joint frailty model), використовуючи СС смерть як конкуруючий ризик [8].
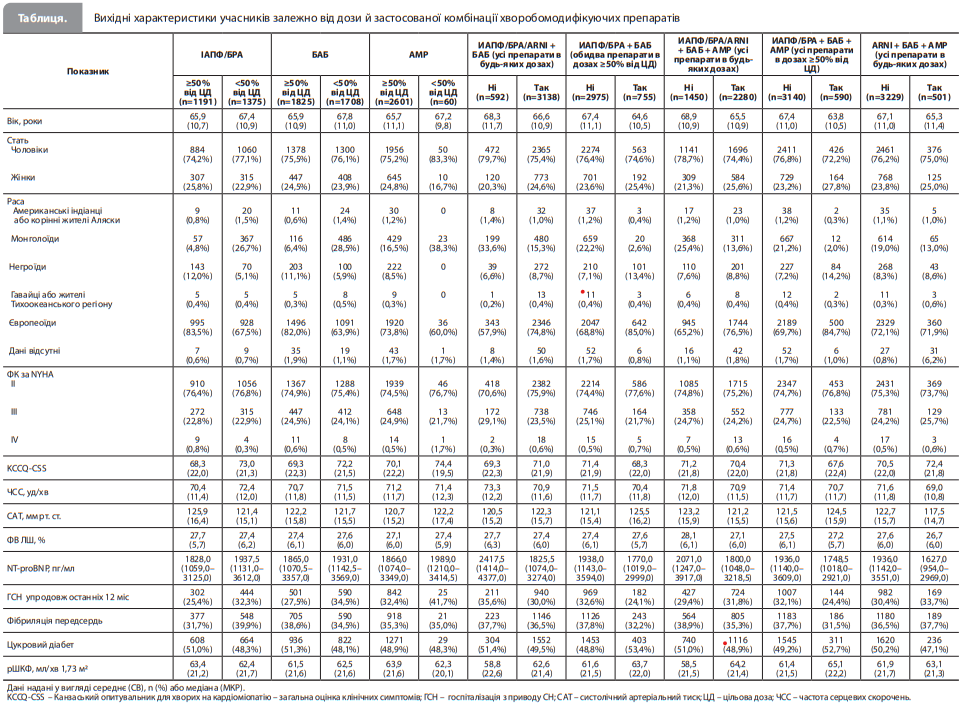
Результати ретроспективного аналізу Verma et al. За період із 6 березня 2017 року до 28 травня 2020 року з 3730 пацієнтів (середній вік [СВ] 66,8 року [11,0], 893 [23,9%] жінки) зі СНзнФВ, зарахованих до дослідження EMPEROR-Reduced, 1863 (49,9%) було рандомізовано в групу емпагліфлозину й 1867 (50,1%) – у групу плацебо (табл.) [8]. Аналіз схем фонової терапії показав, що більшість пацієнтів (88,3%) приймали ІАПФ, БРА або ARNI (з них 46,4% отримували дозу, яка становила ≥50% від цільової); відповідні показники для БАБ та АМР становили 94,7% (51,7%) і 71,3% (97,7%). Також було показано, що більшість учасників (84,1%) отримували комбінацію ІАПФ/БРА/ARNI + БАБ, водночас тільки 20,2% від загальної досліджуваної вибірки отримували комбінацію ІАПФ/ БРА + БАБ із застосуванням доз обох препаратів, що становили ≥50% від цільової. Потрійну терапію комбінацією ІАПФ/БРА/ARNI + БАБ + АМР призначили 61,1% пацієнтів, при цьому 13,4% пацієнтів отримували комбінацію ARNI + БАБ + АМР (табл.) [8].
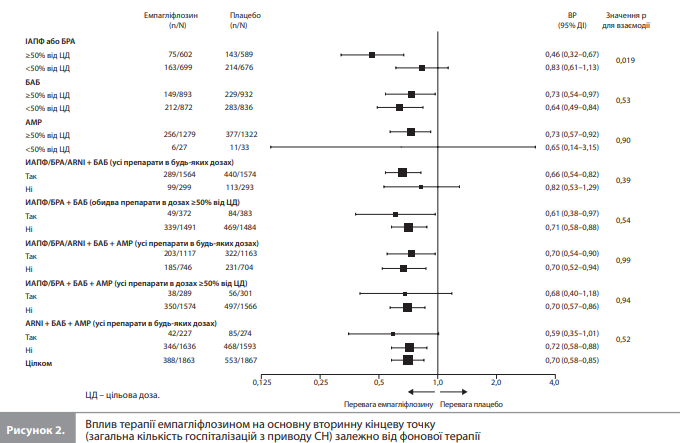
Емпагліфлозин послідовно знижував ризик первинної комбінованої кінцевої точки, що включала госпіталізацію з приводу СН і СС смерть, за всіх оцінюваних діапазонів вихідних доз фонових препаратів (рис. 1) [8]. Зокрема, у пацієнтів, які приймали ІАПФ або БРА, ВР первинної кінцевої точки для доз <50% від цільової становило 0,85 (95% ДІ 0,69–1,06), а для доз ≥50% від цільової – 0,67 (95% ДІ 0,52–0,88; p для взаємодії = 0,18). Аналогічно, у пацієнтів, які отримували БАБ, ВР первинної кінцевої точки для доз <50% від цільової становило 0,66 (95% ДІ 0,54–0,80), а для доз ≥50% від цільової – 0,81 (95% ДІ 0,66–1,00; p для взаємодії = 0,15). Під час аналізу впливу фонової терапії на ефекти емпагліфлозину на основну вторинну кінцеву точку (загальну кількість госпіталізацій із приводу СН) було виявлено номінально значущу взаємодію між дозою фонових препаратів і ефектами емпагліфлозину в пацієнтів, які отримували ІАПФ/БРА (ВР для дози, що становила <50% від цільової: 0,83, 95% ДІ 0,61–1,13; ВР для дози, що становила ≥50% від цільової: 0,46, 95% ДІ 0,32–0,67; p для взаємодії = 0,019; рис. 2) [8]. Ефект емпагліфлозину на цю кінцеву точку був послідовним при використанні різних доз БАБ (ВР для дози, що становила <50% від цільової: 0,64, 95% ДІ 0,49–0,84; ВР для дози, що становила ≥50% від цільової: 0,73, 95% ДІ 0,54–0,97; p для взаємодії = 0,53; рис. 2) [8]. Вплив емпагліфлозину на розширену комбіновану кінцеву точку так само не залежав від доз ІАПФ, БРА або БАБ (рис. 3) [8]. Аналіз впливу вибору конкретних комбінацій фонових препаратів показав, що ефект емпагліфлозину на первинну кінцеву точку був послідовним серед пацієнтів, які приймали клінічно значущі подвійні та потрійні комбінації хворобомодифікуючих препаратів (рис. 1) [8]. Слід зазначити, що серед пацієнтів, які отримували комбінацію ІАПФ/БРА/ ARNI + БАБ, ВР первинної кінцевої точки становило 0,73 (95% ДІ 0,62–0,85) на користь емпагліфлозину, в той час як серед пацієнтів, які не отримували цієї комбінації препаратів, ВР становило 0,84 (95% ДІ 0,62–1,13), хоча статистичних ознак взаємодії між цією комбінацією фонових препаратів і ефектом емпагліфлозину не виявлено (p для взаємодії = 0,42). Водночас, аналіз ефектів досліджуваного лікування залежно від вихідного застосування потрійної фонової терапії комбінацією ІАПФ/БРА/ARNI + БАБ + АМР показав, що перевага емпагліфлозину була стабільною незалежно від приймання такої терапії (на тлі застосування вказаної комбінації ВР первинної кінцевої точки становило 0,73 [95% ДІ 0,61–0,88], а за відсутності такої терапії – 0,76 [95% ДІ 0,62–0,94]; p для взаємодії = 0,77). Примітно, що ефект емпагліфлозину також не залежав від приймання потрійної комбінації ІАПФ/БРА + БАБ + АМР у дозах, що становили ≥50% від цільової (ВР за умови застосування вказаної комбінації та без неї становило 0,80 [95% ДІ 0,55–1,17] і 0,74 [95% ДІ 0,64–0,86] відповідно; p для взаємодії = 0,71), і потрійної комбінації ARNI + БАБ + АМР (ВР становило 0,55 [95% ДІ 0,35–0,86] і 0,77 [95% ДІ 0,67–0,89] відповідно; p для взаємодії = 0,15). Аналізи взаємодії між ефектами емпагліфлозину на первинну кінцеву точку й прийманням інших комбінацій фонових препаратів показали аналогічні результати (стабільний і послідовний ефект емпагліфлозину). Вплив досліджуваного препарату на основну вторинну кінцеву точку (загальна кількість госпіталізацій з приводу СН) також не залежав від фонової терапії (рис. 2) [8]. Зокрема, значення ВР для пацієнтів, які отримували й не отримували комбінацію ІАПФ/БРА/ ARNI + БАБ, становили 0,66 (95% ДІ 0,54–0,82) і 0,82 (95% ДІ 0,53–1,29) відповідно (p для взаємодії = 0, 39), а для пацієнтів, які отримували й не отримували комбінацію ІАПФ/БРА/ARNI + БАБ + АМР, – 0,70 (95% ДІ 0,54–0,90) і 0,70 (95% ДІ 0,52–0,94) відповідно (p для взаємодії = 0,99). Застосування або незастосування цих комбінацій фонових препаратів також не впливало на динаміку зниження ризику розширеної комбінованої кінцевої точки під дією емпагліфлозину (рис. 3) [8].

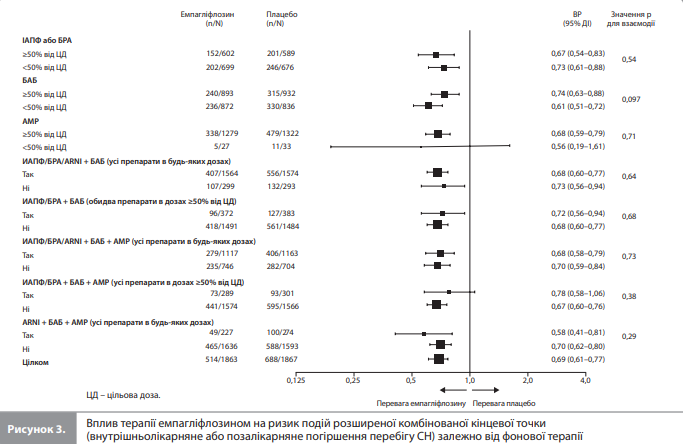
Аналіз впливу фонової терапії на безпеку досліджуваного лікування засвідчив, що тенденції, які спостерігалися в загальній досліджуваній вибірці (більша частота неускладнених інфекцій статевих шляхів у групі емпагліфлозину порівняно з групою плацебо й відсутність значущих міжгрупових відмінностей щодо частоти переломів кісток, гіпоглікемії, ампутації нижніх кінцівок, гіпотензії, симптоматичної гіпотензії та гіперкаліємії), загалом зберігалися в усіх досліджуваних підгрупах, виділених з урахуванням фонової терапії [8].
Обговорення результатів аналізу Verma et al. Отже, аналіз, проведений з метою з'ясувати, чи впливає вибір класу й рівень дози препаратів фонової хворобомодифікуючої терапії СН на динаміку ризику наслідків СН під дією емпагліфлозину в пацієнтів із СНзнФВ, продемонстрував стабільну перевагу емпагліфлозину над плацебо в зниженні ризику подій первинної комбінованої кінцевої точки (СС смерть або госпіталізація з приводу СН) під час застосування різних клінічно значущих подвійних і потрійних комбінацій фонових препаратів у дозах на рівні менш чи більш ніж 50% від цільової. Аналогічно, ефективність емпагліфлозину в зниженні ризиків основної вторинної (загальна кількість госпіталізацій) і розширеної комбінованої (внутрішньо- і позалікарняні епізоди погіршення перебігу СН) кінцевих точок була зіставною в усіх аналізованих підгрупах. Також схема фонової терапії (вибір препаратів і доз) не впливала на безпечність і переносимість емпагліфлозину. Загалом, ці дані свідчать про те, що при застосуванні на додаток до раніше призначеної хворобомодифікуючої терапії СНзнФВ емпагліфлозин забезпечує клінічно значущі переваги незалежно від класу й дози препаратів фонової терапії [8]. Результати аналізу Verma et al. доповнюють спостереження, зроблені в дослідженні DAPA-HF [9, 10], даними щодо ефективності й безпечності застосування іНЗКТГ2 у поєднанні з потрійними комбінаціями фонових препаратів: ІАПФ/БРА + БАБ + АМР (усі препарати у дозах, що становлять ≥50% від цільових) і ARNI + БАБ + АМР (найефективніша фармакотерапевтична комбінація при СНзнФВ; частка пацієнтів, які отримували цю комбінацію, становила 6–9% у DAPA-HF і 15% у EMPERORReduced). Аналіз результатів застосування емпагліфлозину з урахуванням приймання зазначених комбінацій на вихідному рівні показав незалежність ефектів іНЗКТГ2 на досліджувані кінцеві точки від фонової терапії, а також добру переносимість остаточної схеми лікування, яка складалася з чотирьох препаратів (трикомпонентна фонова терапія + іНЗКТГ2) [8]. Результати представленого аналізу мають вагоме клінічне значення. По-перше, вони демонструють, що фонова терапія СНзнФВ не впливає на ефективність емпагліфлозину; по-друге, свідчать про те, що 4-компонентна терапія СН є корисною для пацієнтів навіть у разі недосягнення цільових доз фонових препаратів унаслідок гіпотонії або інших проблем; і, по-третє, показують, що, можливо, в емпагліфлозину є додатковий механізм дії при СНзнФВ, який не залежить від глікемічного статусу й зберігається навіть за низьких значень рШКФ (зниження до 20 мл/хв/1,73 м2 в EMPEROR-Reduced). Імовірно, цей механізм пов'язаний зі зворотним ремоделюванням серця й реалізується через посилене передавання сигналів про нестачу поживних речовин, що, своєю чергою, може поліпшити функцію та виживаність кардіоміоцитів [8, 10–12]. Сукупно, отримані дані дають змогу припустити, що емпагліфлозин можна включати до схеми лікування СНзнФВ незалежно від інших видів терапії, оскільки його переваги не залежать ні від доз, ні від обраної комбінації хворобомодифікуючих фонових препаратів [8]. Результати представленого аналізу слід інтерпретувати з урахуванням низки обмежень, зокрема ретроспективного типу аналізу (що робить отримані результати пошуковими й генеруючими гіпотези), множинності порівнянь (що може збільшити частку хибнопозитивних результатів), відсутності доступних даних щодо застосованих доз ARNI (що не дало змоги провести аналіз за цим параметром), недоступності даних щодо комплаєнтності пацієнтів і змін схеми лікування СН під час дослідження, порівняно невеликої кількості пацієнтів у деяких проаналізованих підгрупах, а також нерандомізованого призначення фонової терапії з урахуванням особливостей конкретного пацієнта й місцевих рекомендацій (що могло призвести до важливих відмінностей між досліджуваними підгрупами) [8].
Висновки Отже, результати ретроспективного аналізу даних рандомізованого дослідження EMPEROR-Reduced показали, що ефективність емпагліфлозину при СНзнФВ зберігалася незалежно від використовуваних доз і комбінацій препаратів хворобомодифікуючої терапії СН. Тому застосування емпагліфлозину слід розглядати у всіх пацієнтів із СНзнФВ незалежно від одержуваної фонової терапії.
Список літератури знаходиться в редакції
Автор огляду Наталія Генш Medicine Review 2023; 2 (69): 16 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2026. Усі права захищені.
|
мапа сайту корисні посилання |