Роль гіперсимпатикотонії в розвиненні артеріальної гіпертензії та методи її корекціїЕфективна терапія артеріальної гіпертензії (АГ), як однієї з основних причин передчасної смерті в усьому світі, входить до групи першочергових завдань громадської охорони здоров’я. Водночас своєчасна та адекватна антигіпертензивна терапія (АГТ) має не тільки продовжити життя людей з АГ, а й знизити ризик інвалідизації, пов’язаної з серцево-судинними (інсульт, стенокардія, інфаркт міокарда, серцева недостатність, захворювання периферичних артерій та аневризма черевного відділу аорти) і нирковими (ниркова недостатність) ускладненнями АГ [1, 2]. До того ж, АГТ має бути персоналізованою, тобто має враховувати інші фактори серцево-судинного (СС) ризику, які часто співіснують з АГ, у тому числі цукровий діабет (ЦД), дисліпідемію/гіперхолестеринемію, ожиріння й хронічну хворобу нирок [1, 3, 4], а також переважні патофізіологічні механізми, що лежать в основі розвитку АГ у конкретного пацієнта. Зокрема, важливою характеристикою значної частини гіпертензивних хворих є гіперактивність симпатичної нервової системи (СНС), що обґрунтовує використання терапії, спрямованої на модулювання активності СНС, у схемі лікування таких пацієнтів. У цьому огляді представлені основні відомості про патофізіологію АГ з урахуванням ролі СНС, а також про роль препаратів, що впливають на СНС, у досягненні контролю АГ [5].
Патофізіологія АГ з акцентом на ролі СНС Згідно з сучасним визначенням, про наявність АГ свідчить рівень систолічного артеріального тиску (САТ) ≥140 мм рт.ст. і/або рівень діастолічного артеріального тиску (ДАТ) ≥90 мм рт.ст. при вимірі АТ на прийомі у лікаря [2]. Фактори ризику АГ добре відомі, це надмірна вага, надлишок кухонної солі в раціоні, сидячий спосіб життя й зловживання алкоголем, водночас етіологія АГ нині вивчена недостатньо [6, 7]. Багатофакторний і дуже складний патогенез АГ характеризується участю багатьох систем органів та численних незалежних і взаємозалежних механізмів і сигнальних шляхів [8]. Крім того, важливим компонентом патогенезу АГ є дисрегуляція нейрогормональних систем, що відповідають за регулювання СС гомеостазу, а саме СНС і ренін-ангіотензин-альдостеронової системи (РААС) [9]. Експерименти на тваринах продемонстрували наявність різноманітних реципрокних взаємозв’ язків між СНС і РААС, які відіграють важливу роль у регуляції функції СС системи й розвиненні АГ, однак у людей докази подібної взаємодії досі не отримані [10, 11].
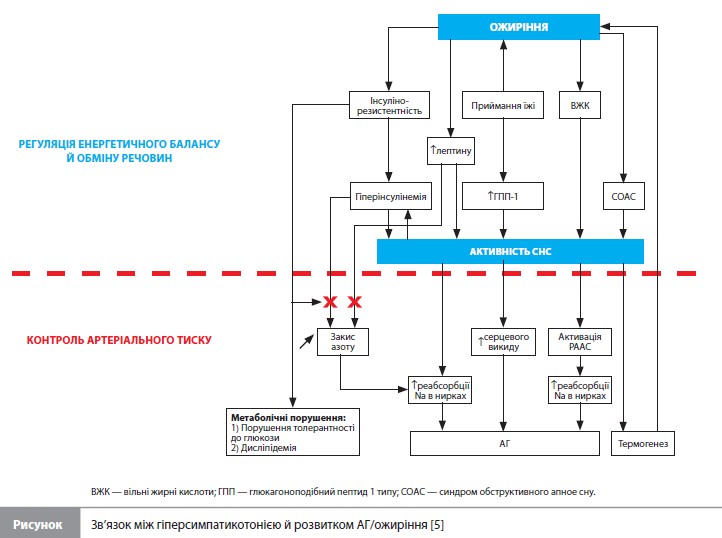
РААС бере участь у підтримці АТ, регуляції рівня натрію в плазмі й об’єму позаклітинної рідини, контролює функцію нирок та серця. З безлічі функцій СНС найбільш значущими в контексті контролю АТ і розвитку АГ/факторів ризику АГ є збільшення серцевого викиду й звуження периферійних судин у відповідь на системне зниження АТ (барорефлекс), а також регуляція метаболічних процесів у печінці (стимуляція глюконеогенезу), підшлункової залозі (інгібування секреції інсуліну, що веде до пригнічення гліколізу й ліпогенезу та стимуляції глюконеогенезу) і жировій тканині (посилення ліполізу) [12–15]. Характерна для АГ гіперактивність СНС має численні СС, ниркові й метаболічні наслідки (рис.) [16–18]. Точна причина виникнення хронічної гіперсимпатикотонії невідома, проте, як і у випадку з АГ, певну роль відіграють генетичні, поведінкові фактори й особливості способу життя [19, 20]. За реалізацію ефектів активації СНС відповідають адренергічні нейромедіатори норадреналін, адреналін і дофамін, які мають вазоконстрикторні властивості [18]. Ці молекули через вплив на органи, які беруть участь у контролі гомеостазу, зокрема на серце, нирки, вени й артеріоли, індукують зміни в СС системі та процесах обміну речовин. СС ефекти зазначених нейромедіаторів призводять до вивільнення реніну, затримки натрію, збільшення частоти серцевих скорочень (ЧСС), порушення серцевого ритму й розвитку гіпертрофії лівого шлуночка (ЛШ), що сприяє підвищенню АТ. Метаболічні ефекти включають індукцію ліполізу з посиленим вивільненням жирних кислот, стимуляцію глюконеогенезу й пригнічення секреції інсуліну, що в умовах хронічної гіперсимпатикотонії може призвести до розвитку інсулінорезистентності й АГ, а також збільшує ризик СС захворювань (ССЗ) [5]. Слід зазначити, що крім гіперактивації СНС для хворих на АГ характерний низький тонус парасимпатичної нервової системи (ПНС), що вказує на дисбаланс між цими двома компонентами вегетативної нервової системи [21–23]. На додаток до розвитку АГ подібна дисфункція сприяє збільшенню маси тіла (МТ), водночас надмірна вага/ожиріння (особливо вісцеральне ожиріння), у свою чергу, підтримують гіперактивність СНС, яка спрацьовує як компенсаторний механізм, що дозволяє відновити енергетичний баланс через збільшення витрати енергії [24, 25]. Результатом нерідко стають прогресуюча інсулінорезистентність з подальшою гіперінсулінемією, порушенням метаболізму глюкози й розвитком ЦД, а також дисліпідемія [26, 27]. Ожиріння також часто пов’язане з резистентною АГ, яка характеризується неможливістю контролювати АТ, незважаючи на призначення трьох або більше антигіпертензивних препаратів (АГП), зокрема діуретиків [27]. Водночас наслідком хронічної гіперсимпатикотонії при ожирінні часто стає зниження симпатичної реакції на різні подразники, наприклад на приймання їжі з високим вмістом вуглеводів або на фізичні навантаження, порівняно з худорлявими людьми [28–31]. Зниження симпатичного резерву може сприяти подальшому збільшенню МТ, зростанню інсулінорезистентності й гіперінсулінемії і, таким чином, підтримувати порочне коло: збільшення МТ – інсулінорезистентність – ослаблення реакції СНС на стимули – збільшення МТ тощо. Додатковим чинником, який стабілізує це порочне коло в людей з ожирінням, стає надмірна секреція адипоцитами гормону лептину [3, 4], який, крім регуляції процесу накопичення жиру, відіграє важливу роль у розвитку АГ за рахунок додаткової стимуляції СНС в тканинах, що беруть участь у регуляції функції СС системи, зокрема в нирках, де вазоконстрикція викликає активацію РААС [32, 33]. Отже, при тривалому існуванні гіперактивність СНС стає самопідтримуючим процесом, що призводить до розвитку й прогресування більшості компонентів метаболічного синдрому, таких як ожиріння, інсулінорезистентність, гіперглікемія, дисліпідемія та АГ [34]. У деяких випадках заходи щодо зміни способу життя (дієта й фізичні вправи) можуть призвести до зворотного розвитку перерахованих вище процесів за рахунок зниження МТ, що веде до покращення ліпідного профілю, метаболізму глюкози, підвищення чутливості тканин до інсуліну та зниження САТ і ДАТ [35]. Однак у значної частини пацієнтів з АГ, пов’язаною з ожирінням, зміни способу життя недостатньо для контролю АТ і необхідно застосовувати фармакотерапію [27].
Вплив стратегій АГТ на активність СНС Рекомендації щодо лікування АГ включають зміну способу життя (дієта, зниження МТ, фізичні вправи), яка застосовується як окрема стратегія або у поєднанні з фармакотерапією [1]. Є докази, які підтверджують, що усунення гіперсимпатикотонії внаслідок застосування деяких стратегій АГТ викликає низку сприятливих змін у СС системі та метаболізмі [36]. Зміна способу життя. Незважаючи на велику кількість АГП, доступних пацієнтам з АГ, зміна способу життя залишається обов’язковою й необхідною умовою ефективної АГТ [1]. Було показано, що фізичні вправи знижують рівень АТ і захищають від ССЗ [21], а дієта Dietary Approach to Stop Hypertension (DASH; раціон з акцентом на фрукти й овочі, знежирені молочні продукти, цільнозернові злаки, горіхи, нежирне м’ясо, птицю та рибу) при використанні в рамках програми зниження МТ зменшує рівні АТ і атерогенних ліпідів, а також покращує маркери метаболізму [37]. Крім того, встановлено, що зменшення МТ зменшує активність СНС, що призводить до зниження периферійного судинного опору й підвищення чутливості тканин до інсуліну [37]. Також корисний контроль споживання кухонної солі, оскільки надмірне споживання натрію пов’язане з гальмуванням ПНС, дисліпідемією й запаленням [38]. Результати клінічних досліджень підтверджують, що зниження МТ сприяє відновленню балансу СНС/ПНС, особливо коли обмеження калорійності раціону поєднується з фізичними вправами. Катетерна денервація ниркових артерій. У дослідженнях ниркової денервації як методу лікування резистентної АГ процедура забезпечувала зниження АТ і зменшення ризику ССЗ [39–42]. Крім впливу на АТ ниркова денервація демонструвала такі наслідки інгібування активності СНС, як покращення контролю глікемії та чутливості тканин до інсуліну, а також зниження загального периферійного судинного опору [39, 40, 43]. Паралельно спостерігалися зниження жорсткості стінок артерій (зменшення швидкості пульсової хвилі), зниження маси ЛШ, зменшення тяжкості симптомів серцевої недостатності, покращення діастолічної функції міокарда, а також збільшення фракції викиду ЛШ і зниження ЧСС [39, 43, 44]. До цього ж було показано, що ниркова денервація знижує концентрацію норадреналіну в тканинах нирки й рівень реніну в плазмі [45]. Фармакологічні стратегії. До АГП, що пригнічують надмірну активність СНС, відносяться бета-адреноблокатори (БАБ) і агоністи імідазолінових (I1) рецепторів [46, 47]. Ефекти БАБ більшою мірою затребувані у пацієнтів із серцевою недостатністю й зниженою фракцією викиду ЛШ, у яких ці препарати доведено знижують ризик розвитку СС ускладнень [5]. При АГ їх застосування можуть обмежувати такі метаболічні побічні ефекти, як інсулінорезистентність, дисліпідемія, гіперглікемія [46, 48, 49] і збільшення МТ [2, 27]. З точки зору корекції активності СНС задля лікування АГ найбільший інтерес представляють агоністи імідазолінових рецепторів, що впливають на рецептор I1, наприклад, клонідин, моксонідин, рилменідин. Рецептори I1 знаходяться в ростральній зоні вентролатеральної частини довгастого мозку, що бере участь у симпатичному контролі АТ, і відіграють важливу роль у регуляції активності СНС [5, 50]. Слід зазначити, що клонідин одночасно стимулює й імідазоліновий рецептор I1, і α2-адренорецептори, у той час як моксонідин і рілменідин вважаються селективними агоністами, які активують тільки імідазолінові рецептори I1 [46, 51], що дозволяє уникати побічних ефектів, пов’язаних із стимуляцією α2-адренорецепторів і характерних для клонідину (переважно це втома, сонливість і седативний ефект). Збільшення активності нейронів у ростральній зоні вентролатеральної частини довгастого мозку за рахунок прямої стимуляції I1-рецепторів відповідними агоністами пригнічує тонус СНС, що через зниження інтенсивності вивільнення норадреналіну й тонусу судин (усунення вазоконстрикції) призводить до зниження АТ [5]. I1-рецептори також представлені на клітинній мембрані нейронів мозкової речовини надниркових залоз, ниркового епітелію, панкреатичних острівців, тромбоцитів і передміхурової залози [50, 52]. Крім зниження АТ рилменідин забезпечував зниження ЧСС (через вплив на чутливість барорефлексу) [53], а моксонідин збільшував екскрецію натрію, підвищував чутливість тканин до інсуліну [54] і покращував толерантність до глюкози, а також забезпечував захист від пошкодження органів-мішеней підвищеного АТ (тобто знижував ризик розвитку хронічної хвороби нирок і гіпертрофії міокарда) [56]. У клінічних дослідженнях за участю пацієнтів з АГ моксонідин сповільнював прогресування ниркової недостатності, зменшував вираженість гіпертрофії ЛШ і покращував функцію ендотелію [51, 55]. У дослідженні MERSY [56] щоденне застосування моксонідину (0,2-0,4 мг) протягом 6 міс у вигляді монотерапії або в комбінації з іншим АГП було пов’язано з покращенням контролю АТ, зниженням МТ та оптимізацією таких параметрів метаболізму, як рівні ліпідів і рівень глюкози в плазмі натщесерце. Відповідно до цих даних нещодавно опубліковане міжнародне дослідження STRAIGHT, засноване на опитуванні лікарів в умовах реальної клінічної практики, показало, що у включених до дослідження країнах опитані лікарі розглядали селективні агоністи імідазолінових рецепторів як корисний варіант терапії, особливо в пацієнтів з комбінацією АГ і порушень метаболізму [57].
Висновки Артеріальна гіпертензія – це складний патологічний процес, який є загальновизнаним фактором серцево-судинного ризику. Гіперактивація СНС відіграє провідну роль в етіопатогенезі АГ, а також пов’язана з цілою низкою захворювань і станів, що супроводжують АГ, таких як ожиріння, ЦД та дисліпідемія. Деякі антигіпертензивні препарати, зокрема селективні агоністи імідазолінових рецепторів, інгібують гіперактивність СНС, що не тільки призводить до зниження підвищеного АТ, а й викликає сприятливі зміни в роботі СС системи й нирок, а також сприяє регуляції обміну речовин.
Список літератури знаходиться в редакції
Автор огляду Віктор Міцьо |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2026. Усі права захищені.
|
мапа сайту корисні посилання |