Переваги застосування монотерапії тикагрелором в окремих групах пацієнтів після черезшкірного коронарного втручання: огляд результатів субаналізів TWILIGHT-HBR і TWILIGHT-COMPLEX PCIПонад 20 років призначення комбінації ацетилсаліцилової кислоти (АСК) й інгібітора P2Y12 було основною стратегією дезагрегантної терапії у пацієнтів, які перенесли черезшкірне коронарне втручання (ЧКВ) [1]. Ця комбінація препаратів, яка називається подвійною антитромбоцитарною терапією (ПАТ), була доведено краще, ніж АСК окремо у попередженні розвитку серцево-судинних (СС) подій після імплантації стента, хоча і за рахунок посилення ризику кровотечі [2, 3]. Імплементація потужних інгібіторів P2Y12 у рутинну клінічну практику ще більше ускладнила досягнення компромісу між ризиками ішемії та кровотечі. Так, застосування прасугреля або тикагрелора в комбінації з АСК порівняно з клопідогрелем демонструвало кращий захист пацієнтів із гострим коронарним синдромом (ГКС) від повторних ішемічних подій [4, 5], однак ця користь була врівноважена підвищеним ризиком кровотеч внаслідок посиленого пригнічення функції тромбоцитів, що має клінічну значущість, оскільки геморагічні ускладнення після ЧКВ так само негативно впливають на прогноз, як і ішемічні події [6, 7]. Поява нових поколінь коронарних стентів та останні досягнення в розробці фармакологічних стратегій дозволили проводити ЧКВ у старших за віком та більш уразливих груп пацієнтів [8, 9], унаслідок чого все більше кандидатів на проведення ЧКВ мають супутні захворювання і стани, пов’язані з високим ризиком кровотечі (ВРК), за наявності яких виникають сумніви в доцільності використання стандартної схеми ПАТ у повному обсязі [10, 11]. Однією з альтернативних схем у такому випадку може бути монотерапія тикагрелором, на користь якої свідчать результати дослідження TWILIGHT, згідно з якими монотерапія тикагрелором після короткого курсу ПАТ є ефективною та безпечною стратегією уникнення кровотечі серед пацієнтів із групи високого ризику ішемічних і геморагічних подій (відповідно до широкого діапазону клінічних та ангіографічних критеріїв), які перенесли ЧКВ [12, 13]. Щоб дослідити лікувальні ефекти монотерапії тикагрелором порівняно з комбінацією тикагрелор + АСК у сучасній вибірці хворих із ВРК, група вчених Escaned et al. провела попередньо запланований аналіз дослідження TWILIGHT з використанням критеріїв ВРК від Академічного консорціуму (Academic Research Consortium, ARC) (далі – аналіз TWILIGHT-HBR) [14]. Трохи раніше за Escaned et al. друга група вчених, Dangas et al. провела ретроспективний аналіз даних TWILIGHT, щоб з’ясувати чи буде стратегія, яка вивчалася в TWILIGHT, корисною для окремої групи хворих з підвищеними ризиками тромботичних ускладнень – пацієнтів після складного ЧКВ (далі – аналіз TWILIGHTCOMPLEX PCI) [15]. Результати цих двох аналізів будуть стисло представлені в цьому огляді.
Загальні відомості про дослідження TWILIGHT TWILIGHT було рандомізованим плацебо-контрольованим дослідженням, яке проводилося в 11 країнах. Для участі у дослідженні підходили пацієнти, які успішно пройшли ЧКВ з імплантацією стента з лікарським покриттям і відповідали принаймні одному клінічному та одному ангіографічному критеріям, пов’язаним з високим ризиком ішемії або кровотечі. Клінічні критерії включали вік ≥65 років, жіночу стать, тропонін-позитивний ГКС, атеросклеротичне захворювання судин (перенесений інфаркт міокарда [ІМ], коронарна реваскуляризація або захворювання периферичних артерій), цукровий діабет, який потребує лікування, та хронічну хворобу нирок (ХХН). Ангіографічні критерії включали багатосудинну ішемічну хворобу серця (ІХС), загальну довжину стента >30 мм, тромботичний характер цільового ураження, біфуркаційне ураження, яке вимагає встановлення двох стентів, обструктивне ураження стовбура лівої коронарної артерії або проксимального відділу лівої передньої низхідної коронарної артерії та кальцифіковане цільове ураження, що вимагає апаратного видалення кальцінатів. Також використовувалися такі ключові критерії виключення: наявність ІМ з елевацією сегмента ST, кардіогенний шок, попередній інсульт або потреба в пероральній антикоагулянтній терапії [12, 13]. Протягом трьох місяців після індексного ЧКВ усі зареєстровані пацієнти отримували відкриту терапію комбінацією тикагрелору (90 мг двічі на добу) і АСК (81–100 мг на добу). Після вказаного періоду пацієнти, які були прихильними до лікування і не мали великих кровотеч або ішемічних явищ, продовжили відкриту терапію тикагрелором у попередньому режимі, а також були рандомізовані у співвідношенні 1:1 для отримування АСК або відповідного плацебо протягом додаткових 12 місяців. Усі учасники проходили опитування телефоном через місяць після рандомізації та приходили на візит до клініки через 6 і 12 місяців після рандомізації [13].
Первинною кінцевою точкою дослідження TWILIGHT була кровотеча 2, 3 або 5 типу за класифікацією Академічного консорціуму з вивчення кровотеч (Bleeding Academic Research Consortium, BARC) протягом року після рандомізації. Ключовою вторинною кінцевою точкою була сукупність смерті від усіх причин, ІМ та інсульту. Крім того, вивчали частоту кровотеч 3 або 5 типу за BARC і сукупність СС смерті, ІМ та ішемічного інсульту. Іншими вторинними геморагічними кінцевими точками були велика кровотеча за класифікацією Thrombolysis in Myocardial Infarction (TIMI), помірна або важка кровотеча за класифікацією Global Use of Strategies to Open Occluded Arteries (GUSTO) і велика кровотеча за класифікацією Міжнародного товариства з тромбозу та гемостазу (ISTH). Інші вторинні ішемічні кінцеві точки включали смерть від усіх причин, СС смерть, нефатальний ІМ, ішемічний інсульт та доведений або ймовірний тромбоз стента [13].
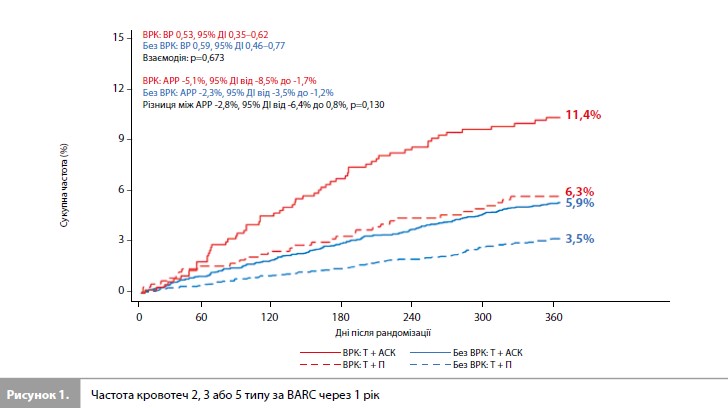
Основні характеристики і результаті аналізу TWILIGHT-HBR В аналізі TWILIGHT-HBR учасниками з ВРК вважалися пацієнти, які відповідали принаймні одному великому або двом малим критеріям ARC. Великими доступними для аналізу критеріями були тяжка або термінальна стадія ХХН (розрахункова швидкість клубочкової фільтрації [рШКФ] <30 мл/ хв/1,73 м2 або діаліз), рівень гемоглобіну <11 г/дл, помірна або тяжка тромбоцитопенія (кількість тромбоцитів <100х109/л), попередні серйозні кровотечі та захворювання печінки. Малі критерії включали: вік ≥75 років, помірну ХХН (тобто рШКФ ≥30 і <60 мл/хв/1,73 м2), рівень гемоглобіну ≥11 і <13 г/дл для чоловіків і ≥11 і <12 г/дл для жінок, а також застосування нестероїдних протизапальних препаратів [14] (табл. 1). У ході попередньо запланованого аналізу проводили оцінку результатів монотерапії тикагрелором порівняно з ПАТ (тикагрелор + АСК) відповідно до ризику кровотечі. Отримані результати подавали як середні значення (стандартне відхилення [СВ]) для безперервних змінних і показники частоти для категоріальних змінних. Для оцінки кумулятивної частоти первинних та вторинних кінцевих точок використовували метод Каплана – Меєра. Були розраховані відношення ризику (ВР) та 95% довірчі інтервали (ДІ), абсолютна різниця між рівнями ризику (АРР) для ішемічних подій і кровотеч, а також р-значення для взаємодії. Крім того, був проведений пошуковий аналіз для вивчення ефектів монотерапії тикагрелором у підгрупах із різною кількістю критеріїв ВРК за ARC (пацієнти без критеріїв ВРК vs пацієнти лише з одним малим критерієм vs пацієнти з одним великим або двома малими критеріями vs пацієнти з кількома критеріями ВРК) [14]. Для аналізів геморагічних подій використовували вибірку рандомізованих пацієнтів, для аналізів ішемічних подій – вибірку учасників, які виконали вимоги протоколу. Двостороннє р-значення <0,05 вважали статистично значущим [14]. У цілому до дослідження TWILIGHT було включено 9006 пацієнтів після ЧКВ, з них 7119 пацієнтів через три місяці після ЧКВ були рандомізовані для отримання монотерапії тикагрелором або продовження ПАТ, з яких 6178 пацієнтів були включені в аналіз TWILIGHT-HBR, а решта 941 не увійшли в аналіз через нормативні причини або через відсутню інформацію про великі або малі критерії ВРК [14]. З 6178 пацієнтів, яких було включено в аналіз, 1064 (17,2%) мали ВРК. Пацієнти з ВРК були старшими за віком, частіше були жінками та представниками неєвропеоїдної раси, мали більше СС факторів ризику та супутніх захворювань, рідше були активними курцями і піддавалися ЧКВ через радіальний доступ і частіше мали багатосудинну ІХС, ЧКВ у стовбурі лівої коронарної артерії та кальцифіковані ураження порівняно з пацієнтами без ВРК. Серед пацієнтів з ВРК помірна ХХН та вік .75 років були двома найпоширенішими малими критеріями (55,4 і 49,4% відповідно), тоді як рівень гемоглобіну <11 г/дл був найпоширенішим великим критерієм ВРК (24,2%). Через 12 місяців після рандомізації пацієнти з ВРК порівняно з пацієнтами без ВРК демонстрували менший рівень прихильності до досліджуваного препарату, який приймали в сліпому режимі (74,5 vs 83,7%, p<0,001), і до тикагрелору (79,2 vs 87,7%, p<0,001) [14]. Кровотечі. Події первинної кінцевої точки – кровотеча 2, 3 або 5 типу за BARC – розвинулися у 8,9% пацієнтів із ВРК і у 4,7% пацієнтів без ВРК (ВР 1,95, 95% ДІ 1,54–2,48, p<0,001), при цьому спостерігалося значне зниження частоти первинної кінцевої точки у пацієнтів із ВРК, рандомізованих для приймання тикагрелору і плацебо, порівняно з пацієнтами, рандомізованими для приймання тикагрелору й АСК (6,3 vs 11,4%, ВР 0,53, 95% ДІ 0,325–0,82, р=0,004), з АРР -5,1% на користь монотерапії тикагрелором (95% ДІ від -8,5% до -1,7%) [14]. Ефекти лікування на кровотечі 2, 3 або 5 типу за BARC серед пацієнтів без ВРК були зіставними (3,5 vs 5,9%; АРР -2,3%, 95% ДІ від -3,5% до -1,2%; ВР 0,59, 95% ДІ 0,46– 0,77, p<0,001) без ознак гетерогенності (рвзаєм.= 0,673) (рис. 1). Частота кровотеч 3 або 5 типу за BARC була так само значно вищою у пацієнтів із ВРК, ніж серед пацієнтів без ВРК (3,4 vs 1,0%; ВР 3,30, 95% ДІ 2,15–5,07, р<0,001) [14]. Застосування комбінації тикагрелор + плацебо призвело до зниження частоти кровотеч 3 або 5 типу за BARC як у пацієнтів із ВРК (1,6 vs 5,0%; ВР 0,31, 95% ДІ 0,14–0,67, р=0,003), так і у пацієнтів без ВРК (0,8 vs 1,3%; ВР 0,62, 95% ДІ 0,36–1,09, p=0,098; рвзаєм.=0,148), але зі значно більшим значенням АРР у підгру пі учасників із ВРК (-3,5%, 95% ДІ від -5,6% до -1,3% проти -0,5%, 95% ДІ від -1,0% до 0,1%; різниця між АРР -3,0%, 95% ДІ від -5,2% до -0,8%, p=0,008) [14]. Подібна картина спостерігалася для інших кінцевих точок у вигляді великої кровотечі за шкалами TIMI, GUSTO та ISTH [14].
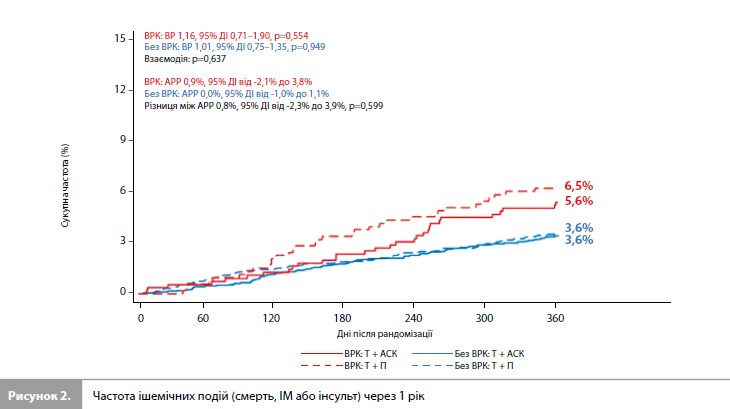
Ішемічні події. У цілому 66 (6,1%) подій ключової вторинної кінцевої точки відбулися у пацієнтів із ВРК порівняно з 181 (3,6%) подією у пацієнтів без ВРК (ВР 1,70, 95% ДІ 1,27–2,26, p<0,001) [14]. Показники сукупного ризику смерті від усіх причин, ІМ або інсульту істотно не відрізнялися між пацієнтами із ВРК, рандомізованими для застосування комбінації тикагрелор + плацебо, і пацієнтами, які приймали комбінацію тикагрелор + АСК (6,5 vs 5,6%; ВР 1,16, 95% ДІ 0,71–1,90, p=0,554; АРР 0,9%, 95% ДІ -2,1% до 3,8%) (рис. 2), як і показники сукупного ризику СС смерті, ІМ або ішемічного інсульту (5,9 vs 5,5%), а також індивідуальні показники ризику СС смерті (1,8 vs 2,6%), ІМ (4,5 vs 3,6%), ішемічного інсульту (0,4 vs 0,2%) і доведеного або ймовірного тромбозу стента (0,8 vs 0,6%) [14]. Під час оцінки підгрупи пацієнтів без ВРК були отримані зіставні результати для ключової вторинної кінцевої точки (3,6 vs 3,6%; АРР -0,0%, 95% ДІ від -1,0% до 1,1%; ВР 1,01, 95% ДІ 0,75–1,35, p=0,949; рвзаєм.=0,637) та інших ішемічних кінцевих точок [14]. Пошукові аналізи. Після стратифікації пацієнтів за кількістю критеріїв ВРК виявилося, що 58,4% не мали жодного критерію, 24,4% – мали один великий критерій, 11,7% – мали один великий або два малих критерії и 5,5% мали більшу кількість критеріїв ВРК [14]. Аналіз виявів прогресивне зростання ризику кровотеч 2, 3 або 5 типу за BARC із ростом кількості критеріїв ВРК: частота подій за 1 рік сягала 4,6, 5,1, 6,9 і 13,3% у чотирьох підгрупах, виділених за кількістю критеріїв ВРК. Аналогічно, частота кровотечі 3 або 5 типу за BARC становила 0,8, 1,6, 2,1 і 6,0%. Схожа картина спостерігалася для ішемічних подій. Відносний вплив монотерапії тикагрелором на геморагічні та ішемічні кінцеві точки був однаковим у всіх підгрупах пацієнтів із ВРК [14]. Нижче наведено основні результати попередньо запланованого аналізу TWILIGHT-HBR [14]. 1. У пацієнтів із ВРК порівняно з пацієнтами без ВРК збільшувався не тільки ризик кровотечі, а й ризик ішемічних подій, при чому зріст цих ризиків був пропорційним кількості критеріїв ВРК. 2. Монотерапія тикагрелором знижувала ризик клінічно значущих кровотеч BARC 2, 3 або 5 типу без збільшення ризику ішемічних подій, включаючи смерть, ІМ і інсульт, незалежно від статусу ризику ВРК. 3. Абсолютне зниження ризику серйозних кровотеч на тлі монотерапії тикагрелором було більш вираженим у пацієнтів із ВРК, ніж у пацієнтів без ВРК. 4. Вплив лікування на випадки ішемії та кровотечі був однаковим у різних категоріях ризику, виділених відповідно до кількості критеріїв ВРК. Загалом, результати аналізу TWILIGHT-HBR підтверджують, що 3-місячна ПАТ з подальшою монотерапією тикагрелором є безпечною та ефективною стратегією уникнення кровотечі серед пацієнтів із ВРК і високим ішемічним ризиком, які піддаються ЧКВ з імплантацією стента з лікарським покриттям, і яким лікар призначив потужній інгібітор P2Y12 [14].

Результаті аналізу TWILIGHT-COMPLEX PCI Статистичні методи, які використовували в аналізі TWILIGHT-COMPLEX PCI, відповідали таким у дослідженні TWILIGHT і заздалегідь запланованому аналізі TWILIGHTHBR. На проведення складного ЧКВ вказувала наявність принаймні 1 з наступних характеристик: 3 проліковані судини, ≥3 проліковані ураження, загальна довжина стента >60 мм, імплантація 2 стентів у зоні біфуркації, використання будь-якого пристрою для атеректомії, ураження стовбура лівої коронарної артерії, цільове ураження в зоні хірургічного шунтування або хронічної повної оклюзії (табл. 2). Послідовність лікувального ефекту монотерапії тикагрелором порівняно з ПАТ (тикагрелор + АСК) у підгрупах пацієнтів після складного и нескладного ЧКВ оцінювали за допомогою формального тестування взаємодії. Значення p <0,05 вказує на статистичну значущість [15].
Із 7119 пацієнтів після ЧКВ, які були рандомізовані для отримання комбінації тикагрелор + плацебо або тикагрелор + АСК, 2956 (32,8%) та 2342 (32,9%) відповідно пройшли складне ЧКВ під час індексної госпіталізації [15]. Пацієнти, які перенесли складне стентування, частіше реєструвалися в Азії, мали більше супутніх захворювань, більший ступінь важкості ІХС і більшу складність ЧКВ. У когорті пацієнтів після складного ЧКВ частота постійної відміни тикагрелору згідно з даними через 1 рік становила 13,0% і 13,6% у групах, які приймали тикагрелор + плацебо або тикагрелор + АСК відповідно (p=0,69). Відповідні результати для припинення приймання досліджуваного препарату (плацебо або АСК) становили 18,4% та 18,2% (р=0,88) [15]. Кровотечі. Серед пацієнтів, які перенесли складне ЧКВ, терапія комбінацією тикагрелор + плацебо асоціювалася з нижчою частотою подій первинної кінцевої точки (кровотечі 2–5 типів за BARC: 4,2 vs 7,7%; АРР 3,5%; ВР 0,54, 95% ДІ 0,38–0,76) і частотою кровотеч 3 і 5 типів за BARC (1,1 vs 2,6%; АРР 1,5%; ВР 0,41, 95% ДІ 0,21–0,80) (рис. 3) [15]. При цьому, зниження геморагічного ризику в групі монотерапії тикагрелором зберігалось при використанні різних шкал оцінки кровотеч. Наявність статистично значущої взаємодії між впливом лікування на геморагічні кінцеві точки і складністю стентування не доведена [15]. Ішемічні події. Серед пацієнтів, яким було проведено складне ЧКВ, комбінації тикагрелор + плацебо і тикагрелор + АСК надавали зіставну дію на кінцеві точки у вигляді сукупності смерті, ІМ та інсульту (3,8 vs 4,9%; АРР 1,1%; ВР 0,77, 95% ДІ 0,52–1,15) і сукупності СС смерті, ІМ та ішемічного інсульту (3,6 vs 4,8%; АРР 1,2%; ВР 0,75, 95% ДІ 0,50–1,12), а також на смертність від усіх причин (0,9 vs 1,5%; АРР 0,6%; ВР 0,59, 95% ДІ 0,27–1,29) і частоту доведеного або ймовірного тромбозу стента (0,4 vs 0,8%; АРР 0,4%; ВР 0,56, 95% ДІ 0,19–1,67) (рис. 3) [15]. Наявність статистично значущої взаємодії між впливом лікування на ішемічні кінцеві точки і складністю стентування не доведена. Більш того, ефект монотерапії тикагрелором порівняно з терапією комбінацією тикагрелор + АСК на первинну кінцеву точку дослідження TWILIGHT (смерть, ІМ або інсульт) був однаковим для різних компонентів визначення складного ЧКВ [15].
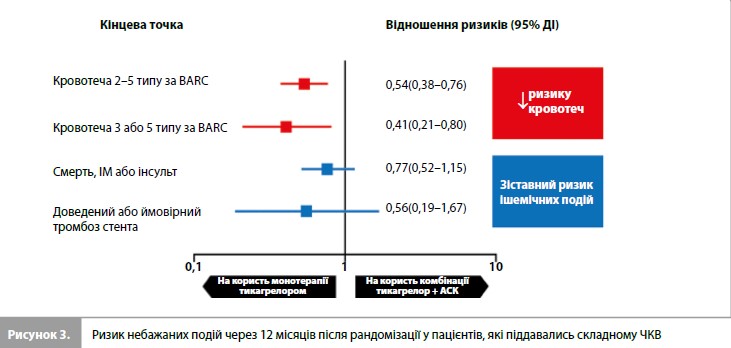
Отже, основні результати ретроспективного аналізу TWILIGHT-COMPLEX PCI свідчать про те, що [15]: 1) перехід на монотерапію тикагрелором після 3-місячної ПАТ призвів до значно менших ускладнень у вигляді великої кровотечі порівняно з продовженням ПАТ и цей ефект не залежав від складності ЧКВ та визначення кровотечі; 2) у пацієнтів, яким було проведено складне ЧКВ, монотерапія тикагрелором не була пов’язана з підвищеним ризиком ішемічних подій порівняно з довгостроковим прийманням комбінації тикагрелор + АСК; крім того, жоден з критеріїв визначення складного ЧКВ не був пов’язаний з підвищенням ризику ішемічних подій, включно з тромбозом стента, при застосуванні монотерапії тикагрелором.
Висновок Заздалегідь запланований (TWILIGHT-HBR) і ретроспективний (TWILIGHT-COMPLEX PCI) аналізи дослідження TWILIGHT показали, що серед вибраних пацієнтів, що пройшли ЧКВ із встановленням стентів з лікарським покриттям і перенесли 3-місячну ПАТ комбінацією тикагрелор + АСК, стратегія, пов’язана з відміною АСК та продовженням монотерапії тикагрелором, значно зменшила ризик клінічно значущих і серйозних кровотеч без збільшення рівня ішемічного захисту порівняно зі стратегією подальшої ПАТ як у когорті пацієнтів з високим геморагічним ризиком, так і в когорті пацієнтів після складного ЧКВ. Ефект монотерапії тикагрелором, який спостерігався у пацієнтів після складного стентування, був стабільним незалежно від конкретних критеріїв складності ЧКВ, яким відповідав індивідуальний пацієнт. Крім того, як стратегія уникнення кровотечі, монотерапія тикагрелором була пов’язана з більшим абсолютним зниженням частоти серйозних кровотеч у пацієнтів з високим геморагічним ризиком порівняно з пацієнтами без високого ризику кровотеч.
Список літератури знаходиться в редакції
Автор огляду Микола Горін Medicine Review 2022; 2 (65): 6 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2025. Усі права захищені.
|
мапа сайту корисні посилання |