Сучасна тактика ведення пацієнтів із клапанними хворобами серця: основні аспекти оновленного руководства ESC/EACTS (2021)У серпні 2021 р. на щорічному конгресі Європейської асоціації кардіологів (ESC) була представлена настанова з ведення пацієнтів із клапанною хворобою серця (КХС), розроблена експертами ESC та Європейської асоціації кардіо-торакальних хірургів (EACTS). Це третя редакція настанови, в основу якої лягли нові науково-обґрунтовані дані, зібрані за 5 років, що минули після публікації попередньої версії документа у 2017 р. Рекомендації спрямовані на організацію діагностичного пошуку, оцінку ризиків, вибір найбільш відповідного виду та терміну втручання, а також на оптимізацію диспансерного спостереження за хворими до та після хірургічного або інтервенційного лікування КХС. Документ зосереджений на проблемах придбаної КХС, у ньому не розглядаються питання, пов’язані з діагностикою та лікуванням ендокардиту та вроджених клапанних вад. У цьому огляді стисло подаються основні положення настанови, що стосуються діагностики та лікування недостатності (регургітації) і стенозу мітрального (МК) та аортального (АК) клапанів, а також основні рекомендації щодо ведення хворих з патологією тристулкового клапана.
Аортальна регургітація (недостатність) Причиною аортальної регургітації (АР) може бути вроджена вада розвитку стулок АК, аномалія геометрії кореня або висхідного відділу аорти. За даними європейського регістру EURObservational Registry Programme Valvular Heart Disease II, найпоширенішим етіологічним фактором АР є дегенеративна недостатність три- або двостулкового аортального клапана. Інші причини представлені інфекційним і ревматичним ендокардитами. Основними причинами гострої тяжкої аортальної недостатності є інфекційний ендокардит і, рідше, розшарування аорти. Обстеження. Основним методом діагностики АР є ехокардіографія (ЕхоКГ), що дозволяє отримати уявлення про анатомію клапана, кількісно оцінити АР, механізми її розвитку, вивчити морфологію аорти та визначити доцільність проведення клапанзберігаючої операції на аорті або протезування клапана. Вимірювання кореня аорти та висхідної аорти при 2-мірній ЕхоКГ виконується на чотирьох рівнях: фіброзне кільце, синуси Вальсальви, синотубулярне з’єднання та тубулярний відділ висхідної аорти. Якщо розглядається можливість проведення пластики АК або клапанзберігаючої операції на корені аорти, то для оцінки анатомії стулок АК необхідно провести передопераційну черезстравохідну ехокардіографію (ЧСЕхоКГ). ЧСЕхоКГ також необхідно повторити під час зазначених втручань для оцінки досягнутих результатів. Додатковими обстеженнями при АР можуть бути комп'ютерна томографія (КТ) та магнітна томографія (МРТ) серця. МРТ слід використовувати для вимірювання фракції регургітації у випадках, коли результати ЕхоКГ є неоднозначними або розходяться з клінічними спостереженнями. У пацієнтів з дилатацією аорти рекомендується проводити КТ для оцінки максимального діаметра аорти на чотирьох рівнях, як при ЕхоКГ. МРТ можна використовувати для подальшого спостереження, але показання до хірургічного втручання бажано обґрунтовувати результатами КТ. Показання до хірургічного втручання. Показання до хірургічної операції при тяжкій АР та ураженні кореня аорти можуть бути засновані на симптомах, стані лівого шлуночка (ЛШ) або ступені дилатації аорти. У пацієнтів з симптомами АР хірургічне втручання рекомендується незалежно від величини фракції викиду (ФВ) ЛШ, якщо ризики, пов’язані з операцією, не вважаються непомірно високими (рекомендація I, B). Хірургічне втручання рекомендується симптомним та безсимптомним пацієнтам з тяжкою АР, які проходять аортокоронарне шунтування (АКШ) або хірургічне втручання на висхідній аорті або іншому серцевому клапані (I, C). У безсимптомних пацієнтів з тяжкою АР порушення функції ЛШ (ФВ ЛШ ≤50% або кінцево-систолічний діаметр лівого шлуночка [КСДЛШ] >50 мм) пов’язане з гіршими результатами, тому при досягненні цих порогових значень слід проводити хірургічне втручання. У пацієнтів із невеликою площею поверхні тіла (ППТ <1,68 м2) або з великою ППТ без надмірної маси тіла слід оцінювати КСДЛШ, скоригований по ППТ (КСДЛШ/ППТ); у цьому випадку граничним значенням вважається 25 мм/м2 ППТ (I, B). Результати кількох нещодавніх ретроспективних нерандомізованих досліджень наголосили на ролі скоригованого КСДЛШ та вказали на доцільність використання нижчого порогового значення – 20 або 22 мм/м2 ППТ, а в одному з них було представлено обґрунтування для використання вищого граничного значення (55%) для ФВ ЛШ. З урахуванням цих даних можна обговорювати виконання операції низького ризику у відібраних безсимптомних пацієнтів з КСДЛШ >20 мм/м2 ППТ або ФВ ЛШ ≤55% (IIb, C). Пацієнти з показниками ЕхоКГ нижчими за порогові значення потребують диспансерного спостереження; у відповідних випадках їм показане тестування з фізичним навантаженням. Виявлення прогресуючого збільшення розмірів або зменшення функції ЛШ у безсимптомних пацієнтів, які не досягли критеріїв проведення операції (за ФВ та КСДЛШ), але демонструють значну дилатацію ЛШ (кінцево-діастолічний діаметр ЛШ [КДДЛШ] >65 мм), також може бути сигналом для визначення термінів проведення операції. В окремих пацієнтів з АР, які не відповідають критеріям хірургічного протезування АК (SAVR), може розглядатися доцільність транскатетерної імплантації АК (TAVI) у центрах з високою активністю проведення цього втручання. Незалежно від ступеня АР та типу клапанної патології, пацієнтам із триабо двостулковим АК та з діаметром аорти ≥55 мм рекомендована операція на висхідній аорті. У осіб із двостулковим АК та додатковими факторами ризику або коарктацією хірургічне втручання слід розглядати при діаметрі аорти .50 мм. Також операція показана всім пацієнтам із синдромом Марфана при максимальному діаметрі аорти ≥50 мм (I, C); цей поріг може бути знижений до ≥45 мм за наявності додаткових факторів ризику у пацієнтів із синдромом Марфана та у пацієнтів з мутацією TGFBR1 або TGFBR2 (у тому числі синдром Лойса-Дитца), і до ≥40 у жінок з низькою ППТ, пацієнтів з мутацією TGFBR2 або пацієнтів з тяжкими позааортальними відхиленнями, що належать до групи особливо високого ризику (IIa, C). У пацієнтів з показаннями до операції на АК вважається, що діаметр аорти ≥45 мм вказує на необхідність проведення супутньої операції на корені або висхідному відділі аорти (IIa, C). Вибір втручання має враховувати досвід команди, наявність аневризм кореня аорти, характеристики стулок АК, очікувану тривалість життя і тип подальшої антикоагулянтної терапії (АКТ). Протезування клапана є стандартною процедурою для більшості хворих на АР. Клапанзберігаюче протезування кореня аорти і пластика АК дають хороші довгострокові результати в окремих пацієнтів з низькою частотою клапанних ускладнень та гарною якістю життя, якщо проводяться у спеціалізованих центрах. Клапанзберігаюче протезування кореня аорти, що виконується досвідченим хірургом, рекомендується молодшим пацієнтам з розширеним коренем аорти та нормальною рухливістю стулок АК (I, B). Медикаментозна терапія. Медикаментозна терапія, зокрема інгібітори ангіотензинперетворюючого ферменту (іАПФ) або дигідропіридинові блокатори кальцієвих каналів (БКК), можуть полегшити симптоми в осіб із хронічною тяжкою АР та протипоказаннями до операції. Можливість відстрочити хірургічне втручання у безсимптомних хворих з помірною або тяжкою АР за допомогою іАПФ або дигідропіридинових БКК не вивчена, і тому використовувати вказані препарати за цим показанням не рекомендується. Між тим, при збереженні серцевої недостатності (СН) або наявності артеріальної гіпертензії (АГ) у пацієнтів після операції застосування іАПФ, блокаторів рецепторів ангіотензину (БРА) та бета-блокаторів (БАБ) вважається корисним. У пацієнтів із синдромом Марфана основними препаратами для корекції симптомів, зменшення напруги зсуву та швидкості подальшої дилатації аорти залишаються БАБ, які слід застосовувати як у перед-, так і в післяопераційному періоді. БРА не показали переваги перед БАБ у цій ситуації, але їх можна використовувати при непереносимості БАБ. Незважаючи на відсутність досліджень, що підтримують застосування БАБ або БРА у пацієнтів з двостулковим АК та розширенням кореня або висхідного відділу аорти, застосування цих препаратів залишається загальноприйнятою клінічною практикою. Динамічне спостереження. Усім безсимптомним пацієнтам з вираженою АР та нормальною функцією ЛШ необхідно проходити обстеження не менше ніж 1 раз на рік. У пацієнтів з уперше встановленим діагнозом або суттєвими змінами розмірів та/або ФВ ЛШ, або при наближенні цих показників до порогових значень, що відповідають критеріям проведення операції, слід проводити обстеження з інтервалом у 3–6 місяців. При легкій та помірній АР можна проводити клінічний огляд щорічно, а ЕхоКГ виконувати 1 раз на 2 роки. Питання про направлення на операцію може розглядатися у безсимптомних пацієнтів зі значною дилатацією ЛШ (КДДЛШ >65 мм) та прогресуючим збільшенням розміру ЛШ або прогресуючим зниженням ФВ ЛШ за даними динамічного спостереження. Рівні мозкового натрійуретичного пептиду (BNP) можуть використовуватися як предиктор результатів (особливо при появі симптомів та погіршення функції ЛШ) і можуть бути корисні при подальшому спостереженні за безсимптомними пацієнтами. При дилатації висхідної аорти (>40 мм) рекомендується проводити КТ або МРТ серця з подальшим контролем розмірів аорти за допомогою ЕхоКГ та/або МРТ. Будь-яке збільшення діаметра на >3 мм має підтверджуватися результатами КТ-ангіографії/МРТ серця та порівнюватися з вихідними даними. Пацієнти з хворобою Марфана, які перенесли пластику аорти, залишаються в групі ризику розшарування аорти і потребують довічного спостереження мультидисциплінарною командою фахівців. Особливі групи пацієнтів. Якщо АР, яка потребує хірургічного втручання, супроводжується тяжкою первинною або вторинною мітральною регургітацією (МР), то обидва порушення необхідно скоригувати під час однієї операції. Існують різні думки про проведення корекції помірної АР під час АКШ або операції на МК, оскільки відомо, що за відсутності дилатації аорти прогресування помірної АР відбувається дуже повільно. У цьому випадку рішення має прийматися кардіологічною бригадою з урахуванням етіології АР, інших клінічних факторів, очікуваної тривалості життя та рівня операційного ризику в пацієнта. Рівень фізичної та спортивної активності за наявності дилатації аорти залишається предметом обговорень через відсутність науково-обґрунтованих даних. Сучасні настанови прагнуть обмежити фізичні навантаження, особливо виконання ізометричних вправ, щоб уникнути катастрофічних наслідків. Загалом такий підхід виправданий за наявності хвороб сполучної тканини, проте рекомендації для інших пацієнтів можуть бути ліберальнішими.
Аортальний стеноз Аортальний стеноз (АС) є найбільш часто діагностованою вадою серцевих клапанів, що потребує хірургічного або ендоваскулярного втручання. Основну інформацію щодо виявлення АС надає ЕхоКГ. Сучасні міжнародні рекомендації щодо ЕхоКГ-оцінки пацієнтів з АС засновані на вимірюванні середнього градієнта тиску (ΔPm), максимальної швидкості кровотоку на клапані (Vmax) та площі клапанного отвору (ПКО). Алгоритм ехокардографічної діагностики АС подається на рисунку 1. Як додаткові методи оцінки пацієнтів з АС можуть використовуватися аналіз на BNP, ЕхоКГ з фізичним навантаженням, КТ серця, МРТ серця та коронарна ангіографія. Вибір між TAVI та SAVR при АС має бути заснований на результатах КТ серця (табл. 1); при протипоказаннях до КТ (наприклад, хронічної ниркової недостатності) або труднощах з інтерпретацією результатів КТ як альтернатива може використовуватися ЧСЕхоКГ.
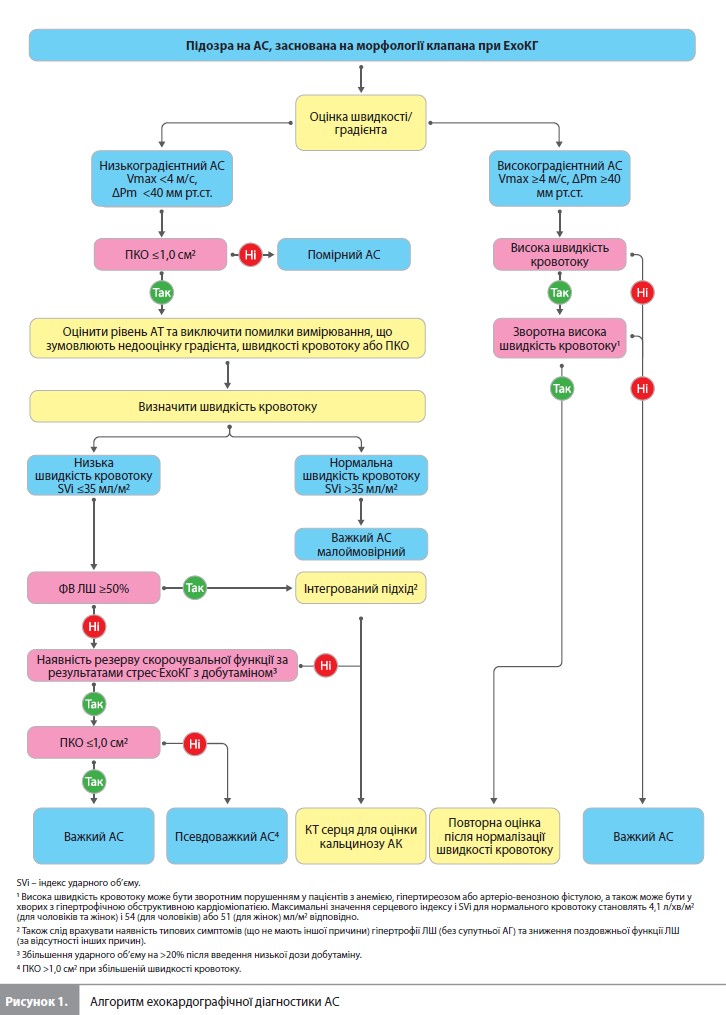
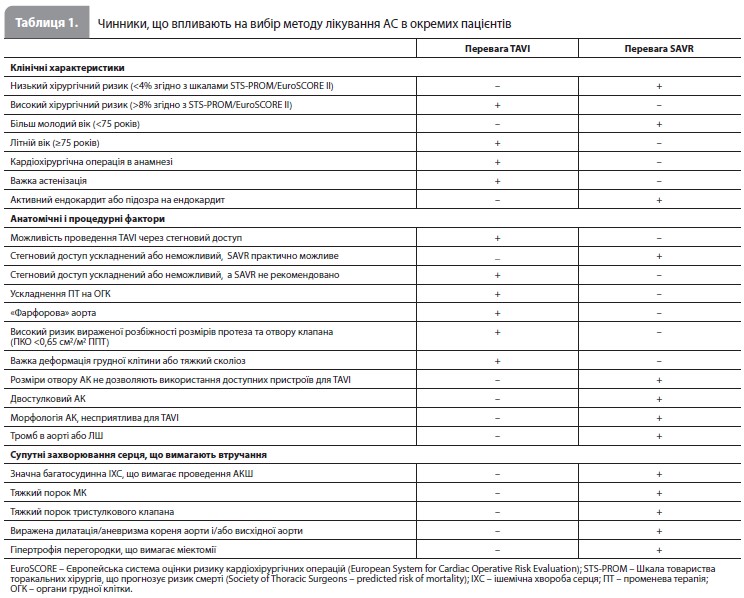
Лікування симптоматичного АС. Оскільки важкий симптоматичний АС має несприятливий прогноз, раннє втручання наполегливо рекомендується всім пацієнтам, за винятком хворих, у яких втручання навряд чи покращить якість життя або виживаність (через тяжкі супутні захворювання), та пацієнтів з очікуваною тривалістю життя менше ніж 1 рік (наприклад, при ракових захворюваннях). Корекція АС однозначно рекомендується симптомним пацієнтам з високим градієнтом тиску на клапані (градієнт ≥40 мм рт.ст., Vmax ≥4,0 м/с та ПКО ≤1,0 см2 або ≥40,6 см2/м2), незалежно від ФВ ЛШ (І, В). У симптомних пацієнтів з важким АС, низькою швидкістю кровотоку (SVi ≤35 мл/м2) та низьким градієнтом тиску (<40 мм рт.ст.) клас рекомендації щодо виконання втручання на клапані залежить від ФВ ЛШ та наявності резерву скорочувальної функції: при зниженій ФВ ЛШ (<50%) та наявності резерву втручання рекомендується до виконання (I, B), а при нормальному значенні ФВ ЛШ або зниженій ФВ ЛШ та відсутності резерву втручання рекомендується до розгляду (IIa, C). У пацієнтів з нормальною швидкістю кровотоку, низьким градієнтом тиску та збереженою ФВ ЛШ прогноз не відрізняється від такого в осіб з помірним АС, тому їм рекомендується регулярне клінічне та ЕхоКГ спостереження. Лікування безсимптомного АС. Втручання на клапані рекомендовано при безсимптомному тяжкому АС у поєднанні з порушенням функції ЛШ (ФВ ЛШ <50%), що не має іншої причини (I, B), або з появою симптомів під час проби з навантаженням (I, C). В інших випадках думки про тактику ведення важкого АС розходяться, тому рішення про проведення втручання потребує ретельної оцінки переваг та ризиків у окремого пацієнта. За відсутності несприятливих прогностичних ознак рекомендується дотримуватися вичікувальної тактики зі швидким проведенням корекції клапана після появи симптомів стенозу. За наявності несприятливих прогностичних ознак (наприклад, дуже важкого АС [середній градієнт ≥60 мм рт.ст. або Vmax ≥5,0 м/с], вираженого кальцинозу клапана у поєднанні зі збільшенням Vmax ≥0,3 м/с/рік або значно підвищеного рівня BNP) у пацієнтів з низьким процедурним ризиком слід розглядати можливість проведення раннього втручання навіть за збереженої ФВ ЛШ та нормальних результатів проби з навантаженням (IIa, B). Вибір між SAVR та TAVI. Результати низки рандомізованих клінічних досліджень, присвячених вибору оптимального методу корекції АС з урахуванням рівня хірургічного ризику, показали, що TAVI перевершує медикаментозну терапію у пацієнтів із вкрай високим ризиком, не поступається SAVR у пацієнтів з високим та середнім рівнями ризику за даними за 5 років наступного спостереження, а також не поступається SAVR у пацієнтів з низьким хірургічним ризиком за даними 2-річного спостереження. У цих дослідженнях частота судинних ускладнень, імплантації кардіостимулятора та приклапанної регургітації була стабільно вищою після TAVI, тоді як тяжкі кровотечі, гостра ниркова недостатність та дебют фібриляції передсердь частіше реєструвалися після SAVR. До переваг TAVI відносяться швидке відновлення пацієнтів, зменшення терміну госпіталізації та швидке повернення до нормальної діяльності, до недоліків – висока вартість пристрою та різна доступність втручання у країнах з різним рівнем розвитку охорони здоров’я. Відповідно до загальноприйнятої концепції, довговічність клапанного протеза є основним фактором у молодших пацієнтів (до 75 років) з низьким хірургічним ризиком, тому у них кращим варіантом лікування АС є SAVR; водночас довговічність протезу має менший пріоритет у літніх пацієнтів (≥75 років), неоперабельних хворих або пацієнтів з високим ризиком хірургічного втручання, і в цих випадках перевагу надають TAVI (особливо якщо процедура виконується через трансфеморальний доступ). Остаточний вибір між хірургічним і транскатетерним втручанням має ґрунтуватися на ретельній оцінці клінічних, анатомічних і процедурних факторів (табл. 1), співвідношення ризиків та переваг кожного підходу з обов’язковим обговоренням кожного варіанту з пацієнтом (I, C). Спостереження. Стан безсимптомних пацієнтів з тяжким АС потрібно контролювати не рідше одного разу на 6 місяців з метою раннього виявлення змін ЕхоКГ параметрів (зокрема ФВ ЛШ). Результати кількох досліджень показують, що прогноз при помірному дегенеративному АС може бути гіршим, ніж передбачалося раніше (особливо за наявності значного кальцинозу клапана), і таких пацієнтів слід обстежувати щонайменше щорічно. Обстеження раз на 2–3 роки може бути достатнім для молодших пацієнтів з легким АС без вираженого кальцинозу клапана.
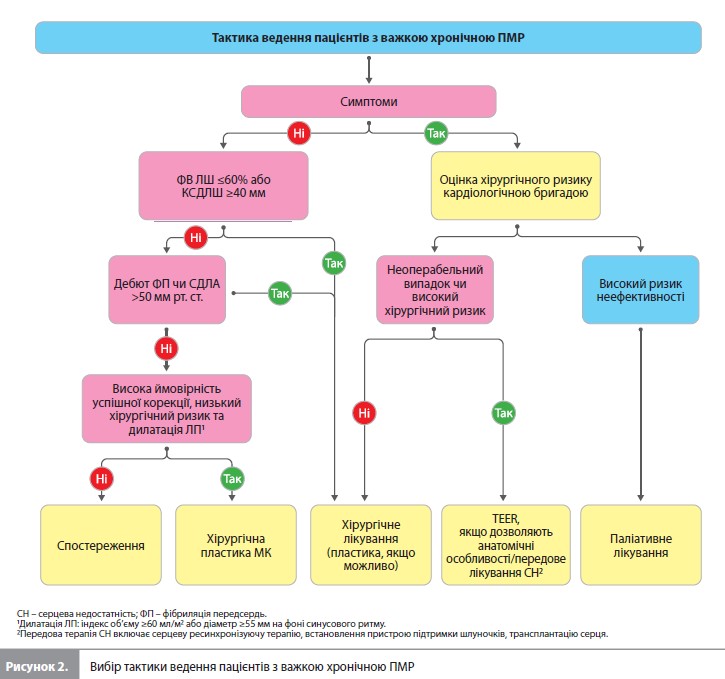
Мітральна регургітація (недостатність) Підхід до лікування мітральної регургітації (МР, другий [після АС] за частотою варіант КХС у Європі) залежить від різновиду вади, яка може бути первинною і вторинною. Первинна МР (ПМР). Основними причинами ПМР є дегенеративні процеси (у розвинених країнах), ревматизм (у країнах із низьким рівнем доходу) та ендокардит. Основним методом діагностики ПМР є ЕхоКГ з визначенням якісних, напівкількісних та кількісних показників МР, а також оцінкою розмірів ЛШ та лівого передсердя (ЛП). Стандартний показник «площа ефективного отвору регургітації» (EROA) тісно пов’язаний з ризиком смерті від усіх причин, що підвищується за величиною EROA ≥20 мм2. Виявлення конкретного ураження, що призвело до формування МР, має прогностичне значення і є дуже важливим для оцінки доцільності хірургічної або ендоваскулярної заміни клапана. Додаткову інформацію надають тривимірна ЧСЕхоКГ, МРТ серця та ЕхоКГ з навантаженням. Також може бути корисним динамічне спостереження за рівнями BNP, оскільки у безсимптомних пацієнтів з тяжкою ПМР без дилатації ЛШ та ЛП низькі значення BNP пов’язані з низьким ризиком смерті. Стандартними критеріями, що визначають тактику ведення пацієнтів з ПМР, є розміри та ФВ ЛШ. Однак дедалі більша кількість даних свідчить про високе прогностичне значення глобальної поздовжньої деформації ЛШ у пацієнтів, у яких планується проведення хірургічної корекції. Нещодавно для оцінки ризику смерті від усіх причин серед пацієнтів з тяжкою формою ПМР, пов’язаною з наявністю патологічно рухомої стулки (стулка, яка молотить), які отримують консервативне або хірургічне лікування, була запропонована шкала Mitral Regurgitation International Database (MIDA), у складі якої використовуються нові порогові значення для діаметра ЛП (≥55 мм) та КСДЛШ (≥40 мм), включені до поточних рекомендацій. Хворим з гострою важкою МР показано термінове хірургічне втручання; у разі розриву папілярного м’яза як основної причини МР зазвичай потрібна заміна клапана. Показання до хірургічного втручання при важкій хронічній ПМР подані в рисунку 2. У цілому ФВ ЛШ ≤60% та/або КСДЛШ ≥40 мм (I, B), індекс об’єму ЛП ≥60 мл/м2 або діаметр ЛП ≥55 мм (IIa, B), систолічний тиск у легеневій артерії (СДЛА) >50 мм рт.ст. або наявність ФП (IIa, B) пов’язані з найгіршими наслідками та вважаються факторами, що вказують на необхідність втручання, незалежно від наявності/відсутності симптомів. За відсутності відповідності цим критеріям у безсимптомних пацієнтів з тяжкою ПМР оптимальною та безпечною вважається вичікувальна тактика зі спостереженням у клініці, що спеціалізується на КХС. При виборі методу корекції МК перевагу має пластика клапана (I, B), оскільки це втручання при досягненні стійкого результату пов’язане з кращою виживаністю порівняно з протезуванням МК. Якщо проведення пластики недоцільно, пріоритет має протезування МК зі збереженням підклапанного апарату. Транскатетерна імплантація мітрального клапана при тяжкому ПМР є безпечною альтернативою для пацієнтів із протипоказаннями до хірургічного втручання або високим хірургічним ризиком (IIb, B). Найбільший обсяг даних зібраний для методики ендоваскулярної корекції МК методом «край у край» (TEER). Рекомендовані терміни спостереження за пацієнтами з ПМР мають бути такими: 1) безсимптомні пацієнти з тяжкою ПМР – обстеження раз на 6 місяців з оцінкою рівнів BNP, виконанням ЕхоКГ, холтерівського моніторування та, за показаннями, МРТ серця; 2) безсимптомні пацієнти з помірною МР та збереженою функцією ЛШ – обстеження 1 раз на рік, ЕхоКГ – 1 раз на 1–2 роки; 3) після ендоваскулярної пластики МК рекомендована щорічна ЕхоКГ. Вторинна МР (ВМР). При ВМР стулки клапанів і хорди мають нормальну будову, а МР виникає через дисбаланс між закриваючими і тягнучими силами, прикладеними до клапана, внаслідок змін геометрії ЛШ і ЛП. Найчастіше ця форма МР спостерігається при дилатаційній та ішемічній кардіоміопатіях, а також у пацієнтів із хронічною ФП та розширенням ЛП. Діагностичний пошук при ВМР відрізняється від такого при ПМР лише необхідністю ретельної оцінки ознак захворювання серця, що призвели до розвитку МР (наприклад, рубця міокарда). Лікування ВМР засноване на оптимізації науково-обґрунтованої медикаментозної терапії у поєднанні з електрофізіологічними, ендоваскулярними та хірургічними втручаннями, що проводяться з урахуванням показань та у порядку, визначеному їх пріоритетом. Докази на підтримку хірургічного втручання обмежені. Операція на МК рекомендується пацієнтам з тяжкою ВМР та показаннями до АКШ або інших кардіохірургічних операцій. Спосіб хірургічної корекції клапана має бути адаптований до індивідуальних потреб пацієнта. Так, у деяких пацієнтів без важкого ремоделювання ЛШ пластика МК із застосуванням замкнутого опорного кільця меншого діаметра дозволяє відновити спроможність клапана, полегшити симптоми та сприяє зворотному ремоделюванню міокарда. Протезування клапана дозволяє уникнути рецидиву МР, але не забезпечує більш вираженого зворотного ремоделювання та не покращує виживаність порівняно з пластикою клапана. Показання для проведення ізольованої операції на МК при ВМР обмежуються значним процедурним ризиком, високою частотою рецидиву МР та відсутністю доведеної користі для виживання. У пацієнтів з передсердною функціональною МР без зниження ФВ ЛШ та слабко вираженою дилатацією ЛШ ефективним може бути проведення анулопластики на опорному кільці (за необхідності – у поєднанні з абляцією з приводу ФП), проте цей підхід потребує подальшого вивчення.
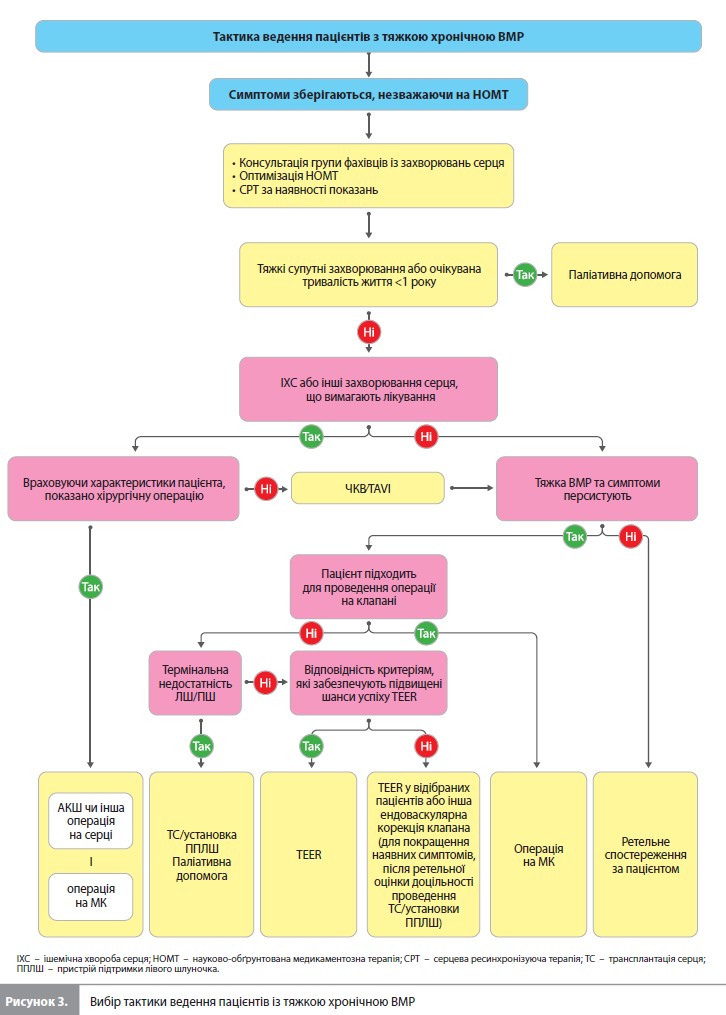
Варіантом мінімального інвазивного лікування ВМР є ендоваскулярна корекція МК з використанням системи MitraClip. Результати двох рандомізованих клінічних досліджень (COAPT та MITRA-FR; учасники з симптоматичною СН та тяжкою ВМР, що зберігаються на тлі медикаментозної терапії, які визнані не підходящими для хірургічного втручання) показали, що ця процедура безпечна та ефективно зменшує вираженість ВМР на строк до 3 років. Водночас у дослідженні MITRA-FR застосування системи MitraClip не впливало на первинну кінцеву точку (комбінація смерті від будь-якої причини та госпіталізації з приводу СН) через 1 рік та 2 роки порівняно з ізольованим застосуванням оптимальної медикаментозної терапії. У дослідженні COAPT імплантація MitraClip значно знизила ризик первинної кінцевої точки (сукупність госпіталізацій з приводу СН) та низки наперед визначених вторинних кінцевих точок, у тому числі смертності від усіх причин за 2-річний період. Подальший субаналіз даних дослідження COAPT підтвердив сприятливі ефекти TEER у кількох підгрупах пацієнтів, тоді як субаналіз даних дослідження MITRA-FR продемонстрував нейтральний ефект інтервенційного втручання у всіх виділених підгрупах пацієнтів. Обговоривши можливі причини таких розбіжностей, експерти ESC дійшли висновку про необхідність проведення подальших досліджень з метою виявлення пацієнтів, для яких TEER буде найбільш корисною. В цей час можливість проведення TEER рекомендується розглядати у окремих пацієнтів з тяжкою ВМР, які відповідають критеріям включення до дослідження COAPT. Крім того, виконання TEER може розглядатися в індивідуальному порядку у пацієнтів, які не відповідають критеріям відбору COAPT, з метою полегшення симптомів і поліпшення якості життя. У пацієнтів з менш тяжкою ВМР (EROA <30 мм2) та вираженою дилатацією/дисфункцією ЛШ прогностична перевага MitraClip залишається недоведеною. При термінальній стадії недостатності ЛШ та/або правого шлуночка (ПШ) та відсутності можливості реваскуляризації найкращим варіантом може бути трансплантація серця або імплантація пристрою підтримки ЛШ. При ФВ ЛШ <15% клапанні втручання, як правило, протипоказані. Алгоритм вибору тактики ведення при тяжкій хронічній ВМР подано в рисунку 3.
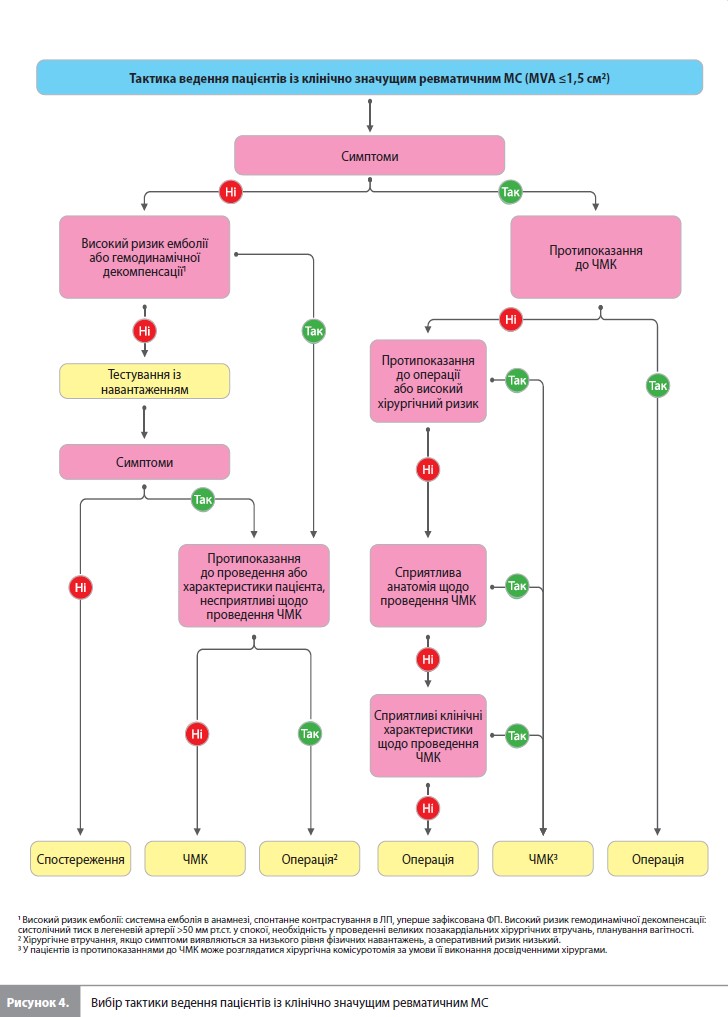
Мітральний стеноз Основними формами мітрального стенозу (МС) є ревматичний та дегенеративний МС, рідше до розвитку цієї вади призводять променева терапія на ділянку грудної клітки, карциноїдна хвороба серця та спадкові метаболічні захворювання. Ревматичний МС. Ознакою клінічно значущого МС є площа МК (МVА) ≤1,5 см2. Переважним методом діагностики МС вважається трансторакальна ЕхоКГ; додаткову інформацію (наявність/відсутність тромбу в ЛП, особливості анатомії МК) може надати ЧСЕхоКГ, а також тестування з навантаженням. Вид лікування (операція або черезшкірна мітральна комісуротомія [ЧМК]), а також його терміни мають визначатися на основі клінічних характеристик пацієнта, анатомії клапана та досвіду клініки (рис. 4). У цілому, втручання показані пацієнтам із клінічно значущим (помірним або тяжким) ревматичним МС (площа клапана <1,5 см2), у яких результати втручання вплинуть на тактику ведення хвороби. Проведення ЧМК слід розглядати як варіант лікування окремих пацієнтів з легким або середньо-тяжким кальцинозом або змінами у підклапанному апараті без протипоказань до ЧМК. До протипоказань до проведення ЧМК відносяться МVА >1,5 см2, наявність тромбу в ЛП, наявність помірної або тяжкої МР, виражений або бі-комісуральний кальциноз, відсутність зрощення комісур, тяжкий супутній аортальний порок серця або тяжкий комбінований трикуспідальний стеноз з регургітацією, що вимагає хірургічного лікування, а також супутня ІХС, що вимагає проведення АКШ. Пацієнтам із симптоматичним МС, які не підходять для проведення ЧМК, показане хірургічне клапанне втручання. Безсимптомні пацієнти з клінічно значущим МС підлягають щорічним обстеженням із проведенням ЕхоКГ; при середньо-тяжкому МС інтервал між обстеженнями можна збільшити до 2–3 років. Спостереження за пацієнтами після успішної ЧМК проводиться за аналогічним графіком, у разі виникнення безсимптомного рестенозу частоту обстежень слід збільшити. У разі розвитку симптоматичного рестенозу більшості пацієнтів показано хірургічну комісуротомію, хоча в окремих випадках (якщо основним механізмом рестенозу є зрощення комісур) можливе проведення ЧМК. Алгоритм вибору тактики ведення при клінічно значущому ревматичному МС подано в рисунку 4. Дегенеративний МС. Цей тип МС характеризується наявністю кальцинозу мітрального кільця (КМК), переважно літнім віком пацієнтів (і, як наслідок, більшою частотою важких супутніх, у тому числі клапанних, захворювань) і, в цілому, несприятливим прогнозом, у тому числі тому, що навіть після успішної корекції зі зниженням трансклапанного градієнта тиску середній тиск у передсерді може залишатися підвищеним унаслідок низької еластичності міокарда ЛП та ЛШ. Кальциноз знижує інформативність ЕхоКГ у зв’язку з чим, якщо у пацієнта з дегенеративним МС планується втручання на клапані, обов’язково проводиться КТ серця. Обидва варіанти корекції клапана (хірургічний і транскатетерний) при цій формі МС відносяться до процедур високого ризику та не вивчалися у рандомізованих клінічних дослідженнях. Через відсутність зрощення комісур ЧМК при дегенеративному МС не показана.
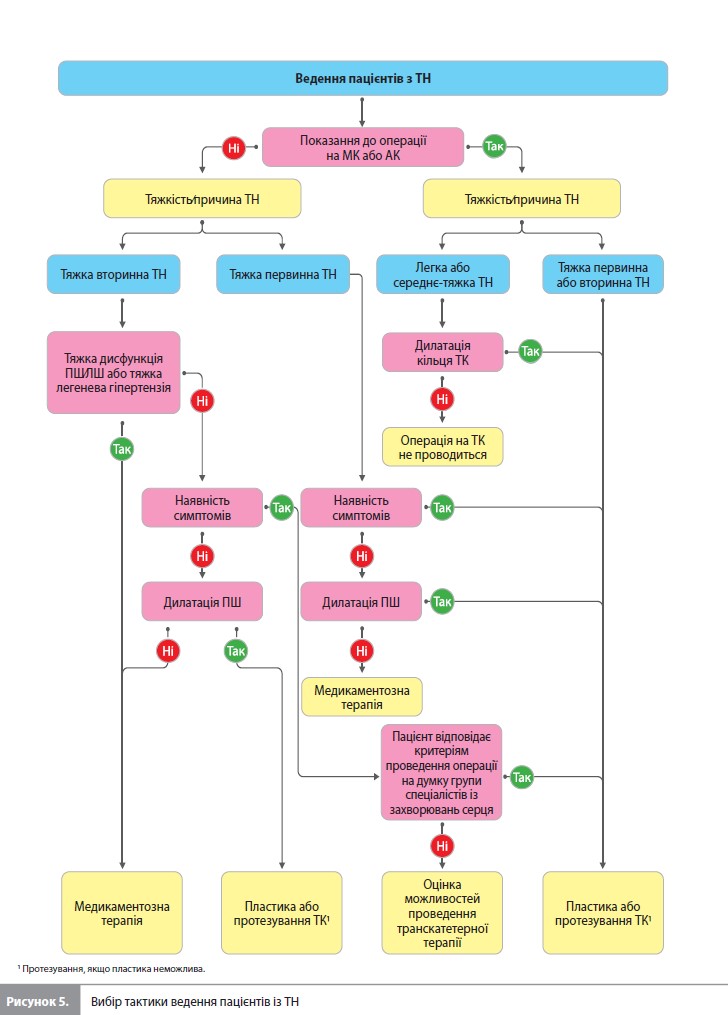
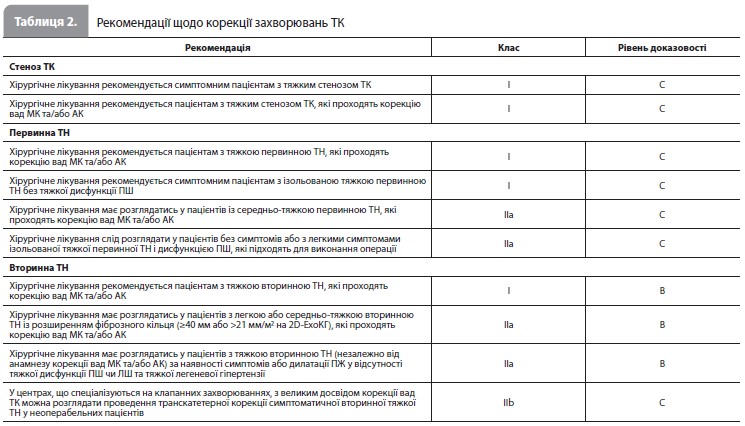
Патологія тристулкового клапана Сучасні рекомендації щодо корекції вад тристулкового клапана (ТК) подані в рисунку 5 (трикуспідальна недостатність – ТН) і таблиці 2 (стеноз тристулкового клапана [ТС] та ТН) вище. З повним текстом настанови англійською мовою можна ознайомитися на офіційному сайті ESC за адресою https://www.escardio.org/
Перелік літератури знаходиться в редакції |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2026. Усі права захищені.
|
мапа сайту корисні посилання |