Корекція ендотеліальної дисфункції в рамках профілактики і лікування ССЗ: потенційні можливості кверцетинуУ цьому огляді йдеться про кардіопротекторний потенціал кверцетину, який реалізується через вплив на ендотеліальну функцію, з акцентом на трьох основних патофізіологічних механізмах ендотеліальної дисфункції (ЕД): атеросклерозі, артеріальній гіпертензії (АГ) та старінні ендотелію. Також у статті представлений такий маловивчений, але потенційно корисний механізм терапевтичної дії кверцетину, як вплив на ендотеліальномезенхімальний перехід (ЕМП). Ці властивості також будуть розглядатися в контексті застосування кверцетину для вторинної і третинної профілактики серцево-судинних захворювань (ССЗ) на прикладі ішемічного пошкодження міокарда при ішемічній хворобі серця (ІХС) [1].
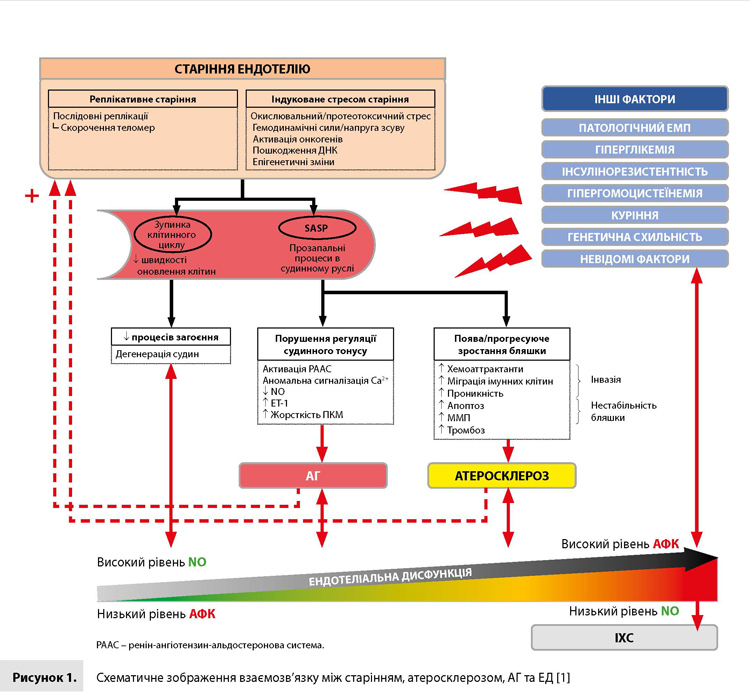
Корекція ЕД як метод профілактики ССЗ Ендотелій відіграє ключову роль у регуляції гомеостазу серцево-судинної системи (ССС): бар’єрну, гемостатичну, вазотонічну, імунну, секреторну, а також бере участь у процесах запалення і ремоделювання судинної стінки [2]. Основною ознакою ЕД є зниження рівня оксиду азоту (NO) унаслідок його недостатнього синтезу із L-аргініну в реакції з участю ендотеліальної NO-синтази (eNOS), яке супроводжується зростанням кількості вільних радикалів (так зване роз’єднання eNOS) [3]. Причини подібних змін численні і включають АГ, дисліпідемію, гіперглікемію, інсулінорезистентність, гіпергомоцистеїнемію, а також старіння і ЕМП. Найчастіше кілька зазначених факторів присутні одночасно і через синергічність ефектів призводять до швидкого прогресування дисфункції артеріальної стінки і розвитку ССЗ. Важливо, що корекція цих порушень веде до відновлення функції ендотелію з одночасним зниженням рівня серцево-судинного ризику [4]. ЕД при АГ і атеросклерозі. Наразі ЕД розглядається як ранній етап розвитку АГ і атеросклерозу і характеризується порушенням ендотелійзалежної вазодилатації і активацією клітинної проліферації, яка веде до розвитку прозапального стану і підвищенню протромбогенного потенціалу [5, 6]. Активовані ендотеліоцити переключаються з передачі сигналів NO на передачу сигналів окисного стресу, опосередковану активними формами кисню (АФК) [7]. На відміну від NO, що відповідає за пригнічення секреції прозапальних цитокінів, тромбозу, проліферації гладком’язових клітин і екстравазації імунних клітин, АФК індукують передачу сигналів ядерного транскрипційного фактора каппа-B (NFkB) – головного регулятора запалення [7]. Крім того, дисфункціональний ендотелій відрізняється підвищеною проникністю, що сприяє активному накопиченню в субінтимальному шарі окислених ліпопротеїнів низької щільності (окЛПНЩ) і макрофагів, що є характерним для початкової фази атеросклерозу [7]. Одночасно з цим відбувається перехід артеріальних судин до стану переважної вазоконстрикції, а підвищений артеріальний тиск (АТ) сприяє посиленню гемодинамічного стресу і додатково стимулює атеросклеротичні процеси. У свою чергу, атеросклероз підтримує дисфункцію eNOS, що підтверджується спостереженим у дослідженнях виробленням супероксиду замість NO (роз’єднання eNOS) в атеросклеротично змінених сегментах стінки судини [8]. Слід зазначити, що схожі зміни розвиваються в мікросудинах за відсутності атеросклерозу та АГ у міру старіння організму. Наявність описаного взаємозв’язку між ЕД, атеросклерозом і АГ у людини підтверджено клінічно зменшенням ступеня артеріальної дилатації (неінвазивний маркер ендотеліальної функції), індукованій ацетилхоліном, у пацієнтів з АГ і хворих з атеросклерозом [4, 9–12]. Більш того, в дослідженні Ludmer et al. результатом ацетилхолінового тесту стало не розширення, а парадоксальне звуження коронарних артерій у пацієнтів з ІХС різного ступеня тяжкості [10]. Нині ЕД усе частіше розглядається не як наслідок пошкодження судини, а як результат порушення функції судинної стінки, що пов’язано зі старінням клітин. Тобто, якщо ЕД лежить в основі розвитку АГ і атеросклерозу, то основою ЕД може бути недостатнє оновлення (старіння) клітин. Старіння клітин. Вичерпання ресурсу поділу і вплив негативних факторів, таких як пошкодження ДНК, окислювальний стрес і мітохондріальна дисфункція, в кінцевому результаті призводять до незворотної зупинки клітинного циклу [1]. Це явище, що отримало назву «сенесцентність», добре відоме як один з дев’яти ознак старіння [1]. Після зупинки клітинного циклу сенесцентні клітини (СК) піддаються глибоким фенотиповим змінам, але зберігають метаболічну активність. У відповідь на стрес вони виробляють набір білків, які формують фенотип, пов’язаний зі старінням (білки SASP) [13, 14], що включає прозапальні цитокіни (інтерлейкін [ІЛ]6, ІЛ-8, мембранні кофакторні білки [MCP] і запальні білки макрофагів), хемокіни, імуномодулятори, фактори росту і сотні сигнальних молекул, наприклад матриксні металопротеїнази (ММП), інгібітори серинових/цистеїнових протеїназ (SERPIN), тканинні інгібітори металопротеїназ, катепсини, брадикініни і гемостатичні фактори [13–15]. У процесі старіння неефективний кліренс подовжує термін життя СК, які накопичуються і завдяки виробленню SASP створюють прозапальне середовище, сприятливе для розвитку різних патологічних станів, включно з ЕД. Надходить усе більше відомостей про виявлення значної кількості СК в патологічно зміненій стінці судин, а також в інтактних артеріях хворих на ІХС [16–18]. При цьому, незважаючи на те що клітини судин мають кінцевий ресурс поділу, саме поєднання блокади реплікації, викликаної пошкодженням, і індукованого стресом старіння може мати пряме відношення до передчасного «зношення» судин і розвитку ЕД. Порочне коло ЕД. Крім індукції прозапального середовища за рахунок SASP, старіння судинної стінки призводить до ще одного наслідку – зниження швидкості відновлення судинних клітин (рис. 1) [1]. СК ендотелію беруть участь у процесі атерогенезу, запускаючи утворення бляшки за рахунок підвищеної секреції хемоаттрактантів і молекул адгезії, які сприяють початковій інвазії моноцитів у стінку судини [19]. Крім того, старіючий ендотелій не здатний підтримувати вибіркову проникність судинної стінки [20], що полегшує міграцію окЛПНЩ у субендотеліальні шари. SASP також можуть стимулювати клітини гладеньких м’язів судин до секреції еластази і ММП, які руйнують компоненти позаклітинного матриксу (ПКМ) [21], що сприяє утворенню вразливих атеросклеротичних бляшок. Таким чином, старіння клітин судин призводить до прогресування атеросклерозу. Багатоетапний зв’язок між старінням і АГ також існує, але менш вивчений, і може реалізуватися через порушення регуляції судинного тонусу (наприклад, активацію ренін-ангіотензин-альдостеронової системи) під дією SASP [16]. З віком імунна система втрачає здатність до активної утилізації СК, що веде до їх накопичення – старіння підтримує старіння (рис. 1) – і сприяє подальшому розвитку АГ і атеросклерозу. Паралельно з віком відбуваються важливі зміни білкового складу ПКМ, що ведуть до зростання артеріальної жорсткості.
Кверцетин Кверцетин є частиною великого сімейства молекулярних сполук, відомого як флавоноїди. Флавоноїди не можуть продукуватися в організмах людини або тварин, але вони активно синтезуються рослинами і у великій кількості присутні в нашому раціоні, наприклад в таких продуктах, як фрукти, овочі, насіння, горіхи, чай і червоне вино [22]. Кверцетин існує як у формі аглікону (вільний кверцетин), так і у вигляді кон’югатів з глікозидами і/або метиловими ефірами (ізокверцетин, гіперозид, ізорамнетин, тамариксетин), при цьому дослідження показали, що різні похідні мають різну ефективність. Так, було показано, що вільний кверцетин має найсильнішу антиоксидантну активність, що підтверджує важливу роль незв’язаних гідроксильних груп [23], а також найбільш ефективно пригнічує рекомбінантний людський ангіотензинперетворюючий фермент (АПФ) 2 типу [24]. Ці відмінності з точки зору біологічної активності обґрунтовують синтез аглікону і окремих похідних кверцетину, які мають максимально виражені цільові ефекти. Хімічна структура аглікону кверцетину робить молекулу гідрофобною – його розчинність у воді при 25°C становить 2,1 мг/л, а в етанолі збільшується до 2 г/л [25]. Ця фізична властивість обмежувала абсорбцію вільного кверцетину і його практичне використання в ролі харчової добавки, тому були розроблені різні комплекси, які дозволяють підвищити його розчинність у воді і біодоступність; деякі форми пов’язані із збільшенням відносної біодоступності при пероральному прийманні на 286% порівняно з вільним кверцетином [26]. Що стосується безпеки кверцетину: у 2010 р. Food and Drug Administration США визнало високоочищений кверцетин (QU995) «загальновизнаним безпечним продуктом» [27]. У більшості випадків кверцетин демонструє хорошу переносимість. При тривалому прийманні кверцетину в дозі 1000 мг/добу відзначалися незначні побічні ефекти, такі як легкий головний біль, нудота і поколювання в кінцівках. На сьогодні існує достатньо епідеміологічних досліджень, які продемонстрували позитивну кореляцію між споживанням кверцетину і зниженням частоти інсульту, інфаркту міокарда (ІМ) та смертності від ІХС [28], переважно за рахунок притаманних йому ефектів, зокрема протизапального, антиоксидантного, антитромбоцитарного, антидіабетичного, антигістамінного, антиканцерогенного, імуномодулюючого і нейропротекторного ефектів [29]. Однак, з огляду на роль патології ССС в сучасній структурі захворюваності та смертності, саме кардіопротекторні ефекти кверцетину, зокрема пов’язані з корекцією ЕД, викликають особливий інтерес.
Захисні ефекти кверцетину на ССС Антиатеросклеротичні ефекти кверцетину. До цього часу в експериментальних дослідженнях отримано великий обсяг даних, які доводять наявність у кверцетину механізмів, що зменшують прогресування атеросклерозу. Зокрема, в декількох експериментальних моделях спостерігалося зменшення площі атеросклеротичних бляшок при введенні тваринам кверцетину, а також зменшення частоти формування аневризм, розшарування і розривів аорти [1, 30]. Одним із способів реалізації антиатеросклеротичного ефекту кверцетину є регуляція метаболізму ліпідів, що підтверджується результатами метааналізу 16 рандомізованих контрольованих досліджень (РКД) впливу кверцетину на ліпідний профіль пацієнтів з метаболічним синдромом, опублікованих в період з 2007 по 2017 рік. Цей аналіз показав, що кверцетин (дози 3,12–3000 мг/добу, курс лікування 3–12 тижнів) приводить до значного зниження рівнів загального холестерину (ХС) і ХС ЛПНЩ, не впливаючи на рівень тригліцеридів [31]. Інший метааналіз, заснований на даних 9 РКД, що включали пацієнтів з надмірною масою тіла та ожирінням, виявив, що застосування кверцетину в дозах ≥250 мг/ добу з досягненням загальної дози ≥14 000 мг значно знижує рівень ХС ЛПНЩ в сироватці [32]. Цікаво, що схожі зміни спостерігали у метаболічно здорових дорослих людей без ожиріння після 8-тижневого приймання кверцетину, і що ці зміни були однаково виражені у чоловіків і жінок [33]. До потенційних механізмів гіполіпідемічного ефекту кверцетину відносяться: збільшення внутрішньокишкової концентрації коротколанцюгових жирних кислот, відомих своїм сприятливим впливом на ліпідний обмін, стимуляція процесу перетворення ХС в жовчні кислоти і еффлюксу ХС за рахунок активації ферменту цитохрому CYP7A1, альфа-форми Х-рецептора печінки (регулятор гомеостазу ХС ), а також індукції синтезу білків ABCG1, ABCA1, задіяних у метаболізмі і транспорті ліпідів, і рецептора ЛПНЩ [1]. Крім того, за деякими даними, кверцетин може діяти аналогічно сучасним гіполіпідемічним препаратам, інгібуючи пропротеїнову конвертазу субтилізинкексинового типу 9 (PCSK9) і 3-гідрокси-3-метилглутарилкоензим А-редуктазу [34–37]. Не менш важливою властивістю кверцетину є здатність стабілізувати атеросклеротичну бляшку за рахунок пригнічення експресії ММП-1, ММП-2 і ММП-9 і, як наслідок, деградації ПКМ, підтверджена в дослідженнях з використанням методів молекулярного моделювання, експериментах на культурах ендотеліоцитів [38–42]. Паралельно з цим кверцетин реалізує антиагрегантний ефект, перешкоджаючи утворенню тромбів на поверхні нестабільної бляшки і подальшому розвитку гострих ускладнень атеросклерозу [43, 44]. За даними дослідження in vitro, при сумісному використанні кверцетину з ацетилсаліциловою кислотою (АСК) спостерігалося синергетичне посилення антиагрегантного ефекту. Механізми реалізації антиагрегантного і антитромботичного ефектів кверцетину можуть включати вплив на процеси активації тромбоцитів, наприклад на внутрішньоклітинну мобілізацію іонів Ca2+, секрецію гранул і активацію інтегринів [45], що призводить до збільшення рівнів циклічного аденозинмонофосфату (цАМФ) і пригнічення агрегації, індукованої арахідоновою кислотою і аденозиндифосфатом (АДФ) [46, 47]. Ще один шлях реалізації антиатеросклеротичних ефектів кверцетину може бути пов’язаний з впливом на окЛПНЩ. У 2 РКД введення кверцетину супроводжувалося значним зниженням плазмових концентрацій окЛПНЩ [48, 49], що може пояснюватися прямим впливом на фермент параоксоназу 1 (PON1), синтез клітинних молекул адгезії (VCAM-1, ICAM1), та відновленням функції eNOS [50]. Ще однією мішенню кверцетину може бути лектин-подібний рецептор 1 типу (LOX-1), а також зменшення рівнів різних прозапальних цитокінів, таких як ІЛ-1., ІЛ-1., ІЛ-2, ІЛ-10, фактора некрозу пухлини (ФНП)-., білка-хемоаттрактанту макрофагів-1 і циклооксигенази2 [39], що важливо з огляду на природу атеросклерозу як хронічного запального захворювання [1]. Вазодилатуючі і антигіпертензивні ефекти кверцетину. Загалом зниження АТ на тлі приймання кверцетину може бути зумовлено ендотелійзалежною вазодилатацією і покращенням функції eNOS [51.53]. Ще одним механізмом вазоактивного ефекту кверцетину є вплив на іонні канали гладеньком’язових клітин судинної стінки, а саме на кальцієві канали L-типу (LTCC, беруть участь у м’язовому скороченні), потенціалзалежні калієві канали (VGKC, беруть участь у відновленні потенціалу спокою) і Ca2+-залежні калієві канали великої провідності (BK, які разом з VGKC беруть участь у вазодилатації коронарних артерій) [1]. Важливою властивістю кверцетину, що визначає його вазодилатуючу активність, є здатність значно пригнічувати експресію ендотеліну-1 (ЕТ-1), одного з найбільш сильнодіючих вазоконстрикторів, який в основному продукується ендотелієм судин і викликає надмірний окислювальний стрес і розвиток ЕД у людини, зокрема за рахунок посилення ефекту роз’єднання eNOS, стимуляції синтезу супероксиду і зниження біодоступності NO [1]. Про характер впливу кверцетину на АТ у людини дають змогу судити результати клінічних досліджень, узагальнені в ході систематичного огляду і метааналізу 7 РКД, опублікованих в період з 1998 по 2014 рік (Serban et al.). Проведений метааналіз виявив значне зниження системного АТ, пов’язане з пероральним прийманням добавок кверцетину (100–1000 мг/добу) [54]. Показники різниці середньозважених значень становили 3,04 мм рт.ст. (р=0,028) і 2,63 мм рт.ст. (р<0,001) для систолічного (САТ) і діастолічного (ДАТ) АТ відповідно, і це досить значущий результат, враховуючи, що у включених РКД в основному брали участь нормотензивні пацієнти. Цікаво, що при використанні метарегресійного аналізу ефект кверцетину на САТ був пов’язаний тільки з тривалістю приймання, але не з уведеною дозою препарату, на відміну від ефекту на рівень ДАТ. Сенолітичні властивості кверцетину. За даними доклінічних досліджень, видалення СК не тільки позитивно впливало на структуру и функцію судини, а й уповільнювало прогресування низки проявів старіння, таких як рак, катаракта, саркопенія, лордокіфоз, зниження жирової маси і зменшення скелетних м’язів, а також підвищувало фізичну витривалість тварин [55]. Ці результати лягли в основу концепції сенолітичної терапії, тобто терапевтичного застосування молекул, здатних специфічно індукувати загибель СК (сенолітики), імовірно, за рахунок цільового впливу на сигнальні шляхи виживання і антиапоптотичні механізми СК [56]. Альтернативна стратегія протидії старінню полягає в застосуванні молекул, що впливають на білки групи SASP. Наразі є підстави вважати, що кверцетин здатний викликати як видалення СК, так і зменшення рівнів SASP [57]. У 2015 р. сенолітичний потенціал кверцетину був підтверджений вченими з лабораторії Кіркланда: у ході досліджень 46 молекул-кандидатів багатообіцяючі результати показали лише кверцетин і дазатиніб (неспецифічний інгібітор тирозинкінази, який використовується для лікування раку) [58]. Цей експеримент проводився на преадипоцитах і ендотеліоцитах пупкової вени людини (HUVEC), і показав, що на відміну від дазатинібу, блокуючого залежне від ефрину В (EFNB) пригнічення апоптозу, кверцетин інгібує фосфатидилінозит-4,5-біфосфат-3-кіназу (PI3K), інші кінази й інгібітор активатора плазміногену 1 (PAI-1) з сімейства SERPIN, при цьому дазатиніб виявився більш ефективним в преадипоцитах, а кверцетин переважно знижував життєздатність сенесцентних HUVEC [58]. Важливо, що в спостережуваних паралельно культурах несенесцентних HUVEC аналогічний за тривалістю (3 дні) вплив кверцетину призвів до 2-3-кратного збільшення кількості клітин, що вказує на вибірковість апоптотичного ефекту кверцетину на СК. На жаль, до цього часу не було виконано жодного клінічного дослідження, спрямованого на оцінку зміни ЕД у людини з ССЗ під дією сенолітичних ефектів кверцетину. Захисні ефекти кверцетину на міокард. Сприятливий вплив кверцетину на дисліпідемію, АГ, старіння й інші чинники ризику можна розглядати як первинну профілактику ЕД. Однак після того як ЕД призводить до розвитку ССЗ, вирішального значення набувають стратегії вторинної (профілактика прогресування ССЗ і його ускладнень) та третинної (боротьба з ускладненнями ССЗ) профілактики, які здатні уповільнити швидкість прогресування захворювання і послабити його вплив на якість життя пацієнтів. Це повною мірою відноситься до ішемії міокарда, яка є наслідком дисфункції ендотелію коронарних артерій і стає причиною локальних порушень в інших клітинах серця, включаючи фібробласти і кардіоміоцити. ЕД і ішемія міокарда пов’язані з надмірним окислювальним стресом, дисбалансом іонів Са2+, а також активацією цитокінів, тромбоцитів і лейкоцитів. Крім того, наявність ЕД опосередковує розвиток дисфункції міокарда після реперфузійної терапії [59]. Відповіддю на ці зміни стають різні патологічні адаптивні реакції, у тому числі надмірне утворення компонентів ПКМ, яке веде до інтерстиціального фіброзу міокарда, змін морфології клітин міокарда і, в кінцевому результаті, до дилатації шлуночків, що, врешті-решт призводить до ремоделювання серця, яке знижує розслаблення і скорочення шлуночків [60]. Клінічно ці зміни проявляються розвитком потенційно інвалідизуючих захворювань, таких як стенокардія, ІМ і серцева недостатність (СН). У доклінічних дослідженнях з оцінкою функціональних гемодинамічних параметрів кверцетин нейтралізував викликані ішемією міокарда зниження систолічного тиску в лівому шлуночку (СТЛШ), зниження максимальної швидкості зміни внутрішньошлуночкового тиску під час ізоволюметричного скорочення (пікова dP/dt) і збільшення кінцево-діастолічного тиску в лівому шлуночку (КДТЛШ) [61–65]. В іншому доклінічному дослідженні з ехокардіографічною оцінкою функції лівого шлуночка (ЛШ) кверцетин значно уповільнив зниження фракції викиду (ФВ) і фракції укорочення (ФУ) ЛШ порівняно з контрольною групою [66]. Виявлене при макроскопічній оцінці значне зменшення розміру зони ІМ, пов’язане з уведенням кверцетину [67–69], підтримувалося виявленням більш низьких сироваткових рівнів ферментативних маркерів ІМ, у тому числі креатинкінази (КК), МВ-фракції КК (ККМВ), кардіотропоніну Т і лактатдегідрогенази [62, 65–67, 69–73]. Цим спостереженням відповідали результати гістопатологічної оцінки, які показали меншу вираженість набряку і лейкоцитарної інфільтрації зони інфаркту і загальну збереженість тканинної архітектури [67, 70, 71]. Усе це підтверджує великий ступінь збереження мембрани кардіоміоцитів, цілісності міокарда і загальне поліпшення міокардіальної функції після впливу кверцетину. Цікаво, що ці кардіопротекторні ефекти спостерігалися при введенні кверцетину як до індукції ішемії, так і під час реперфузії, що передбачає залучення кверцетину в механізми ішемічного пре- і посткондиціонування міокарда [1]. Незважаючи на те що своєчасна реперфузія міокарда необхідна для порятунку ішемізованої тканини, ця процедура супроводжується стресовою реакцією, відомою як «ішемічнореперфузійне пошкодження» (ІРП), яка парадоксальним чином збільшує ступінь ураження міокарда. В основі цього пошкодження лежить вибухове утворення АФК при відновленні кровопостачання раніше ішемізованих клітин; результатом цих процесів стає наростаючий каскад реакцій, пов’язаних з утворенням кисневих радикалів, ПОЛ, перевантаженням клітин іонами Са2+, активацією запальних процесів і апоптозу, які, в результаті, ушкоджують тканини далеко за межами вихідного вогнища ішемії [1]. Цей феномен має важливі клінічні наслідки, оскільки обмежує переваги існуючих методів реваскуляризації міокарда – тромболізису, ангіопластики і аортокоронарного шунтування [74]. Низка досліджень, що проводилися на моделях транзиторного ІМ, показали, що введення кверцетину зменшує тяжкість ІРП. Одним з механізмів впливу на тяжкість ІРП є підтверджений антиоксидантний ефект кверцетину, пов’язаний із захопленням вільних радикалів, таких як супероксид, перекис водню тощо. [75]. Крім того, кверцетин може пригнічувати утворення АФК, інгібуючи НАДФ-оксидазу (NOX) і ксантиноксидазу (XO), знижуючи тим самим активність циклооксигенази та LOX, а також регулюючи активність внутрішньоклітинних сигнальних каскадів, які беруть участь у запальних реакціях [76]. З іншого боку, кверцетин діє як хелатуючий агент: результатом взаємодії з двовалентним залізом може бути пригнічення реакції Фентона (яка веде до утворення вільних радикалів), а взаємодія з цинком може полегшувати доставку цинку в клітини, де він діє як антиоксидант [77–79]. У деяких дослідженнях повідомлялося, що кверцетин забезпечує захист від ланцюгової реакції ПОЛ шляхом нейтралізації пероксильних радикалів і зв’язування з іонами перехідних металів, які каталізують ПОЛ [72, 80, 81]. І нарешті, було показано, що під дією кверцетину зменшується вміст малонового диальдегіду (МДА), мутагенного продукту ПОЛ, і підвищується активність супероксиддисмутази (СОД) і глутатіонпероксидази (ГПО) – двох найважливіших антиоксидаз кардіоміоцитів [62, 65, 66, 70, 82, 83]. Усі ці властивості дають змогу кверцетину протидіяти «ефекту доміно», пов’язаному з пошкодженням міокарда вільними радикалами при ІРП. При ішемії міокарда та ІРП спостерігається активація NFkB, що сприяє експресії цитокінів та викликає збірку інфламасом. Можливим механізмом впливу на NFkB є стимуляція експресії γ-рецептора, що активується проліфератором пероксисом (PPAR-γ). У дослідженні на мишах було показано, що 10-денне попереднє введення кверцетину значно збільшує кількість клітин міокарда з рецепторами PPAR-γ в умовах тимчасового лігірування коронарної артерії [66]. При цьому кверцетин частково відміняв ефекти інгібітора PPAR-γ GW9662, що вело до поліпшення ФВ і ФУ ЛШ та зменшення рівнів маркерів пошкодження міокарда. На відміну від великої кількості експериментальних даних, клінічні дані, що свідчать про сприятливий вплив кверцетину на ІРП у людей, вельми обмежені. Так, в одному дослідженні застосування кверцетину (120 мг/добу протягом 2 місяців) пацієнтами зі стабільною стенокардією на додаток до оптимальної медикаментозної терапії призвело до зниження рівнів ІЛ-1β і ФНП-α порівняно з контрольною групою [84]. В іншому відкритому дослідженні внутрішньовенне введення кверцетину пацієнтам з гострим ІМ і симптомами СН супроводжувалося значним поліпшенням ФВ ЛШ і зниженням рівнів кардіомаркерів вже через 3 дні терапії [85]. У цілому, представлені експериментальні та клінічні дані дозволяють припустити наявність у кверцетину кардіопротекторного ефекту і формують базу для потенційного застосування кверцетину в профілактиці ІХС та її ускладнень. Однак ефективність такої стратегії потребує перевірки в ході добре організованих клінічних досліджень.
Вплив кверцетину на ЕМП Наприкінці 90-х років була виявлена можливість динамічної дедиференцировки ендотеліоцитів, відомої як ендотеліально-мезенхімальний перехід [86], у результаті якої ендотеліальні клітини поступово набувають широкого спектра фенотипових характеристик, типових для мультипотентних клітин [87]. Ця зміна фенотипу включає зниження активності експресії таких маркерів ендотеліальних клітин, як фактор фон Віллебранда, судинно-ендотеліальний кадгерин, і посилення експресії маркерів мезенхімальних клітин, таких як альфа-гладеньком’язовий актин, віментин і N-кадгерин [86, 88]. За своїми наслідками ЕМП – це палиця з двома кінцями. Клітини, що утворюються в результаті ЕМП, виявляють такі ознаки інвазивності, як реорганізація цитоскелета, активація синтезу компонентів ПКМ, зниження здатності до клітинної адгезії і, як наслідок, демонструють підвищений міграційний потенціал [89, 90]. Ці процеси корисні при розвитку ембріона і загоєнні ран, проте в певних умовах, наприклад при запаленні або травмі, ЕМП може призвести до прогресування раку, розвитку прогресуючої осифікуючої фібродисплазії, легеневої артеріальної гіпертензії, фіброзу серця і нирок. Найбільш вивченим медіатором ЕМП є ФНП-β, який діє безпосередньо через шляхи, залежні і не залежні від SMAD (білок-переносник сигналу ФНО-β, який бере участь у регуляції процесів клітинної проліферації, апоптозу і диференціювання), або опосередковано через ЕТ-1, кавеолін-1 (CAV-1) або NFkB. Отримано переконливі докази, що підтверджують наявність перехресних зв’язків між ЕД, атеросклерозом, АГ, старінням і ЕМП [91–96], у зв’язку з чим прицільний вплив на ЕМП може стати новою стратегією профілактики і лікування ССЗ. Нині існують обмежені результати оцінки впливу кверцетину на цей механізм розвитку ЕД. Наприклад, у дослідженні in vitro, проведеному Huang et al., кверцетин ефективно інгібував проліферацію і трансдиференцировку ендотеліальних клітин легеневої артерії людини, індуковані ФНП-β1 [96], що говорить про потенціал застосування кверцетину в лікуванні легеневої артеріальної гіпертензії, вторинної до надмірного росту ендотелію легеневої артерії. Крім того, в попередніх розділах були представлені експерименти, що проводилися поза контекстом ЕМП, але при цьому показали, що кверцетин здатний пригнічувати активність ЕТ-1 і NFkB, які є медіаторами ЕМП [1]. Також цікаві результати були отримані в дослідженнях інгібуючих ефектів кверцетину на процес, який є аналогічним ЕМП, але відбувається за участю епітеліальних клітин (епітеліально-мезенхімальний перехід) [97–99]. З огляду на перелічені дані, можливість використання ефектів кверцетину на процеси старіння, пов’язані з ЕМП, у профілактиці і лікуванні ССЗ становить інтерес і потребує подальшого вивчення.
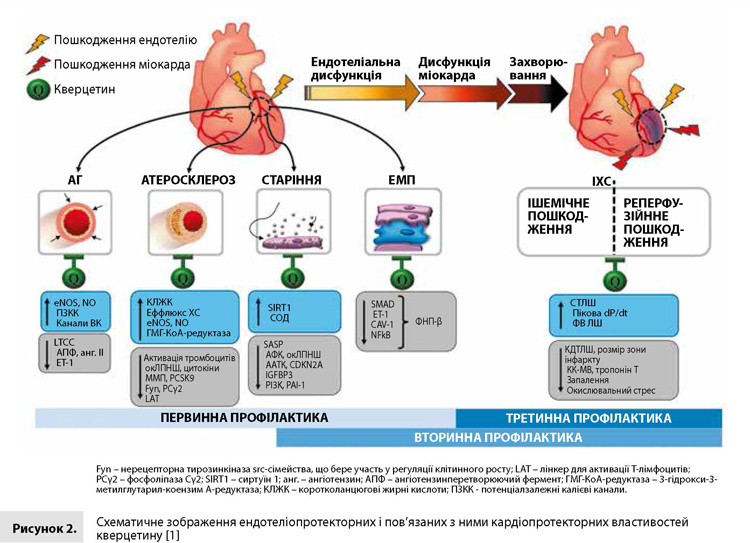
Обговорення і висновки Роль ЕД у виникненні та прогресуванні ССЗ, а також значимість судинного старіння, АГ і атеросклерозу в розвитку ЕД добре вивчені й описані вченими, при цьому атеросклероз і АГ вже є мішенями сучасної терапії, у той час як розробка препаратів проти старіння (сенолітиків) є поки лише багатообіцяючою, але далекою від практичної реалізації галуззю наукових досліджень. Внесок ЕМП у цей каскад патологічних процесів також підлягає подальшому вивченню, але потенційно ЕМП теж може стати точкою застосування ефектів майбутніх фармакологічних стратегій. В очікуванні чергового прориву в галузі профілактики і корекції зазначених порушень доцільно звернути увагу на корисні властивості вже відомих і вивчених речовин і препаратів. У цьому огляді представлені механістичні, експериментальні та клінічні дані, що доводять наявність у кверцетину низки кардіопротекторних ефектів, які можуть бути корисні для пацієнтів з ССЗ або підвищеним ризиком ССЗ, включно з антигіпертензивною і антиатеросклеротичною дією, а також з гальмуванням процесів старіння ендотелію і захистом від ІРП. Крім того, описані обмежені, але обнадійливі дані, які передбачають здатність кверцетину протидіяти розвитку аномального ЕМП – маловивченого, але потенційно дуже важливого етапу розвитку ЕД. Ці властивості представлені на рисунку 2 і становлять основу корисних ефектів кверцетину проти зумовленої старінням ЕД і розвитку/прогресування ССЗ [1]. Така багатоцільова активність кверцетину, спрямована проти різноманітних патологічних процесів, які призводять до розвитку ЕД, а саме процесів старіння, вазомоторної дисфункції, атеросклерозу, ЕМП, запалення, окислювального стресу і порушеного внутрішньоклітинного метаболізму ендотеліоцитів, відкриває перспективи його застосування з метою первинної, вторинної та третинної серцево-судинної профілактики, включаючи захист від дисфункції ендотелію і дисфункції міокарда в умовах ІРП [1]. З огляду на відсутність молекулярної специфічності, велику різноманітність біологічних активностей, а також малу кількість клінічних досліджень кверцетину, на цей час його, можливо, варто розглядати як добре вивчений безпечний агент з доведеними протизапальними, антиоксидантними та іншими властивостями, що знижує уразливість ендотелію перед пошкодженням і процесами старіння і тим самим підсилює корисні ефекти інших кардіологічних препаратів.
Висновок У цілому, кверцетин є багатообіцяючою природною сполукою, яка, вочевидь, задовольняє всім вимогам до нутрицевтиків, що застосовуються для захисту судин від процесів, які призводять до розвитку і підтримують існування ендотеліальної дисфункції. Водночас, інтригуючий потенціал кверцетину як сенолітика і його здатність до захисту міокарда вимагають подальшого вивчення в добре організованих клінічних дослідженнях. Список літератури знаходиться в редакції
Автор огляду Віктор Мицьо
 Medicine Review 2021; 3 (62): 45 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2025. Усі права захищені.
|
мапа сайту корисні посилання |