Кардіоренальні ефекти інгібітора натрій-глюкозного котранспортера 2 типу у пацієнтів з систолічною дисфункцією лівого шлуночка: результати дослідження EMPEROR-ReducedЯк відомо, інгібітори натрій-глюкозного котранспортера 2 типу (іНГКТ-2) є новою групою цукрознижувальних препаратів, призначених для лікування пацієнтів з цукровим діабетом 2 типу (ЦД2). Однак по завершенні фундаментальних досліджень препаратів цієї групи виявилося, що застосування іНГКТ-2 крім власне гіпоглікемічного ефекту супроводжується зниженням ризику госпіталізації з приводу серцевої недостатності (СН) та ризику серйозних небажаних явищ з боку нирок, тобто, що іНГКТ-2 демонструють переваги, нехарактерні для інших антигіперглікемічних препаратів. Зокрема, в метааналізі результатів великомасштабних рандомізованих плацебо-контрольованих досліджень EMPA-REG OUTCOME, CANVAS і DECLARE-TIMI 58, проведеному Zelniker et al., застосування іНГКТ-2 знижувало ризик госпіталізації з приводу СН (ГСН) на 30–35% , а ризик прогресування хвороби нирок (включно із смертю від захворювання нирок, виникненням показань до проведення діалізу або трансплантації нирки) – на 35–50% порівняно з групою плацебо [1]. Слід зазначити, що ці кардіоренальні корисні ефекти не можуть пояснюватися зниженням рівня глюкози в крові, оскільки застосування інших протидіабетичних препаратів з більш сильним антигіперглікемічним ефектом не супроводжувалося подібними змінами серцево-судинних (СС) і ниркових результатів [2]. На основі накопичених доказових даних була висловлена гіпотеза про те, що іНГКТ-2 можуть уповільнювати прогресування хвороб серця і нирок незалежно від їх причини і від наявності або відсутності ЦД [2]. Ця гіпотеза частково підтвердилася в дослідженні Dapagliflozin and Prevention of Adverse Outcomes in Heart Failure (DAPAHF), яке продемонструвало зниження ризику смерті від СС причин і ризику ГСН на тлі застосування дапагліфлозину, незалежно від наявності ЦД [3]. Слід зазначити, що в DAPAHF в основному включалися пацієнти з легким і середньотяжким ступенем систолічної дисфункції лівого шлуночка (ЛШ) і збільшеним рівнем натрійуретичних пептидів. Для перевірки зазначеної гіпотези у пацієнтів з більш тяжким порушенням систолічної функції ЛШ було проведено дослідження Empagliflozin Outcome Trial in Patients with Chronic Heart Failure and a Reduced Ejection Fraction (EMPERORReduced), спрямоване на оцінку результатів застосування іНГКТ-2 емпагліфлозину у вибірці пацієнтів із хронічною СН (з ЦД2 і без ЦД2) і зниженою фракцією викиду (ФВ) ЛШ, яка відрізнялася значною часткою пацієнтів з більш тяжкою дисфункцією міокарда ЛШ [4].
Методологія дослідження EMPEROR-Reduced EMPEROR-Reduced представляло собою рандомізоване подвійне сліпе плацебо-контрольоване дослідження, що проводилося в 520 дослідницьких центрах у 20 країнах світу. У дослідження включали дорослих (≥18 років) пацієнтів з хронічною СН (II, III або IV функціональний клас за класифікацією Нью-Йоркської кардіологічної асоціації) з ФВ ЛШ ≤40%. Усі пацієнти отримували відповідне лікування СН, у тому числі діуретики, інгібітори ренінангіотензинової системи, інгібітор неприлізину, бета-адреноблокатори, антагоністи мінералокортикоїдних рецепторів, а також, при наявності показань, апаратну терапію СН. Оскільки цільовим контингентом цього дослідження були пацієнти з підвищеним ризиком серйозних ускладнень СН, набір учасників з ФВ ЛШ >30% був обмежений пацієнтами, які за останні 12 місяців перенесли ГСН або мали дуже високий рівень N-термінального фрагмента попередника мозкового натрійуретичного пептиду (NT-proBNP; ≥1000 пг/мл для пацієнтів з ФВ ЛШ 31–35% і ≥2500 пг/мл для пацієнтів з ФВ ЛШ 36–40%; у той час як для пацієнтів з ФВ ЛШ ≤30% необхідний рівень NT-proBNP становив ≥600 пг/мл) [4]. Після періоду скринінгу тривалістю 4–28 днів пацієнти, що відповідали критеріям відбору, були рандомізовані у співвідношенні 1:1 для отримання емпагліфлозину (10 мг/добу) або плацебо на додаток до поточної терапії СН. Вибір дози емпагліфлозину був заснований на даних про зниження ризику смерті від СС причин та ГСН, раніше отриманих на тлі застосування емпагліфлозину 10 мг/добу у пацієнтів з ЦД2 [5]. Рандомізація була стратифікована з урахуванням географічного регіону (Північна Америка, Латинська Америка, Європа, Азія чи інший регіон), статусу ЦД2 (наявність або відсутність) на момент скринінгу і розрахункової швидкості клубочкової фільтрації (рШКФ) на момент скринінгу (<60 або ≥60 мл/хв /1,73 м2). Після рандомізації лікарі могли призначати будь-які препарати, схвалені для лікування СН, або змінювати схему їх застосування з урахуванням потреби кожного пацієнта [4]. Обстеження пацієнтів проводилося з частотою раз на 2–3 місяці для оцінки ефективності проведеного лікування і побічних ефектів і включало оцінку основних показників життєдіяльності, маси тіла, рівня глікозильованого гемоглобіну, рівня NT-proBNP, показників ниркової функцій, а також оцінку за Канзаським опитувальником для хворих на кардіоміопатію (KCCQ). Крім того, через 23–45 днів після відміни досліджуваної терапії (емпагліфлозину або плацебо) проводилася підсумкова оцінка рШКФ для оцінки ефекту лікування, незалежного від іНГКТ-2 [4].
Первинною кінцевою точкою дослідження була комбінація смерті від СС причин і ГСН. Вторинними кінцевими точками були всі ГСН (перша і повторні), а також швидкість зниження рШКФ (кут нахилу графіка зміни рШКФ) протягом періоду лікування в подвійному сліпому режимі (емпагліфлозин vs плацебо). Також оцінювалися додаткові кінцеві точки, включно з комбінованим нирковим наслідком (хронічний діаліз, трансплантація нирки або важке стійке зниження рШКФ), загальною кількістю госпіталізацій з будь-якої причини і якістю життя [4]. Первинний аналіз проводився з урахуванням лікування, призначеного під час рандомізації (підхід intention-to-treat) і включав усі дані, отримані до кінця запланованого періоду лікування у всіх пацієнтів, які пройшли рандомізацію. При оцінці міжгрупових відмінностей за первинною кінцевою точкою враховувалися такі заплановані коваріати, як вік, стать, географічний регіон, наявність ЦД на вихідному рівні, ФВ ЛШ і рШКФ на вихідному рівні [4].
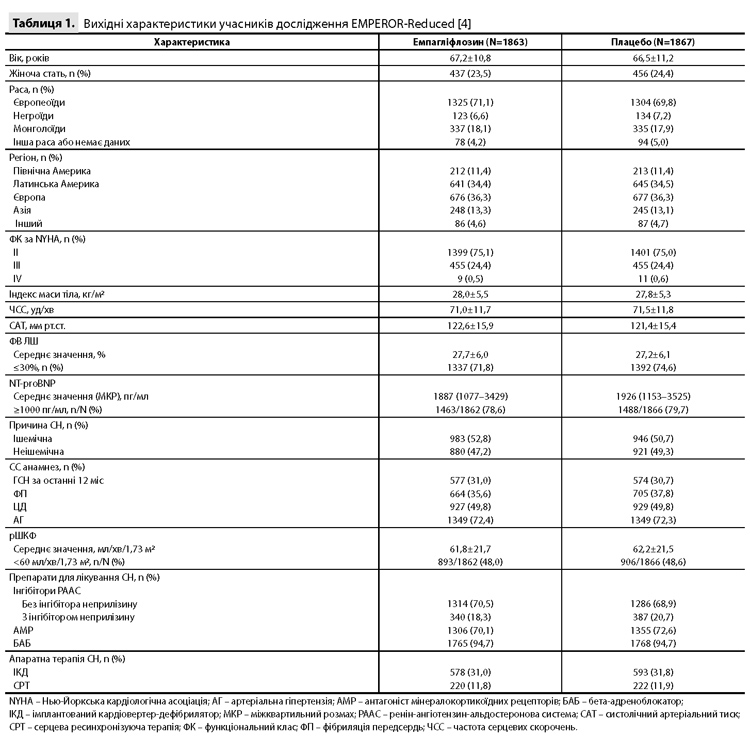
Результати дослідження EMPEROR-Reduced З квітня 2017 р. по листопад 2019 р. скринінг на відповідність критеріям відбору пройшли в цілому 7220 пацієнтів, з яких 3730 були рандомізовані для лікування емпагліфлозином (1863 пацієнти) або плацебо (1867 пацієнтів). Отримані групи були добре збалансовані за вихідними характеристиками учасників (табл. 1) [4]. У половини пацієнтів був ЦД, у 73% – ФВ ЛШ ≤30%, у 79% – рівень NT-proBNP ≥1000 пг/мл, у 48% – рШКФ <60 мл/хв/1,73 м2; майже 20% учасників отримували терапію комбінацією блокатора рецепторів ангіотензину та інгібітора неприлізину (сакубітрил/валсартан). Згідно з остаточними даними, передчасне скасування досліджуваного препарату з причин, відмінних від смерті учасника, сталося у 303 пацієнтів (16,3%) у групі емпагліфлозину і у 335 пацієнтів (18,0%) у групі плацебо. Подальше спостереження після скасування лікування не пройшли 42 пацієнти (20 з групи плацебо і 22 з групи емпагліфлозину). Медіана подальшого спостереження становила 16 місяців [4].
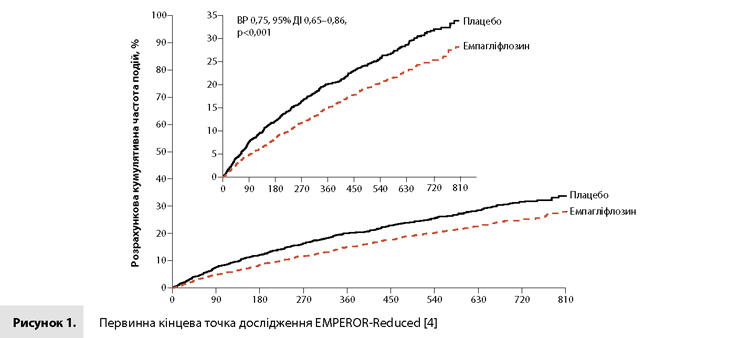
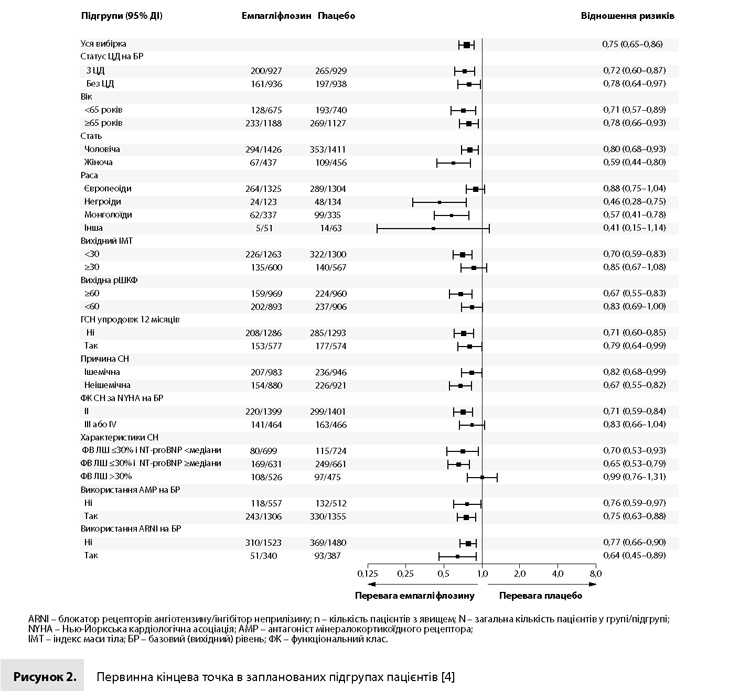
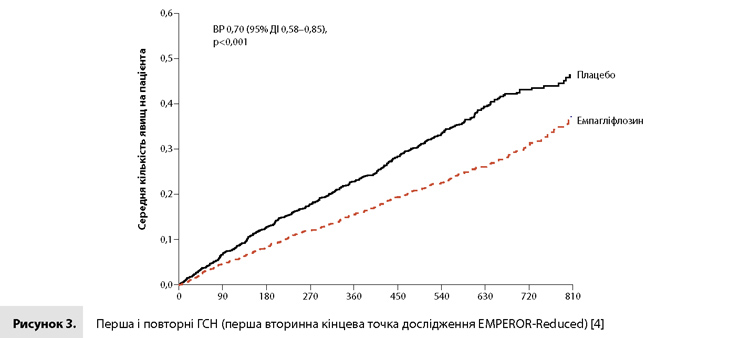
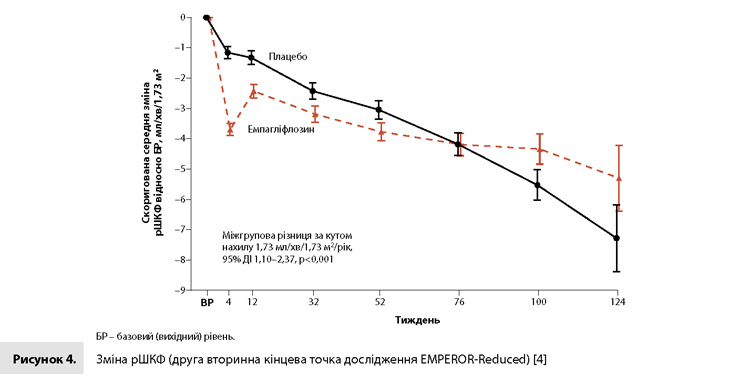
Первинна комбінована кінцева точка (смерть від СС причини або ГСН) була зареєстрована у 19,4% пацієнтів у групі емпагліфлозину і у 24,7% пацієнтів у групі плацебо (відношення ризиків [ВР] 0,75, 95% довірчий інтервал [ДІ] 0,65–0,86, р<0,001) (табл. 2, рис. 1) [4]. ВР для окремих компонентів цієї кінцевої точки (смерть від СС причин і перша ГСН) становили 0,92 (95% ДІ 0,75–1,12) і 0,69 (95% ДІ 0,59–0,81) відповідно (табл. 2) [4]. Упродовж дослідження кількість пацієнтів, яких необхідно було пролікувати для запобігання однієї події первинної кінцевої точки, дорівнювала 19 (95% ДІ 13–37). Вплив емпагліфлозину на первинну кінцеву точку був однаковим у всіх запланованих підгрупах, у тому числі у хворих з ЦД2 і без ЦД на вихідному рівні (рис. 2) [4]. Емпагліфлозин також демонстрував сприятливий вплив на дві вторинні кінцеві точки. Загальна кількість ГСН у групі емпагліфлозину (388 подій) була нижчою, ніж у групі плацебо (553 події, ВР 0,70, 95% ДІ 0,58–0,85; р<0,001) (табл. 2, рис. 3) [4]. Аналогічним чином у групі емпагліфлозину темпи зниження рШКФ протягом періоду лікування в подвійному сліпому режимі були нижчими, ніж у групі плацебо (–0,55 мл/хв/1,73 м2 на рік vs –2,28 мл/хв/1,73 м2 на рік; міжгрупова різниця 1,73 мл/хв/1,73 м2 на рік, 95% ДІ 1,10–2,37; р<0,001) (табл. 2, рис. 4) [4]. Події комбінованого ниркового наслідку (хронічний діаліз, трансплантація нирки або важке стійке зниження рШКФ) рідше реєструвалися в групі емпагліфлозину, ніж у групі плацебо (1,6 vs 3,1%, ВР 0,50, 95% ДІ 0,32–0,77). Серед 966 пацієнтів, у яких були отримані результати парної оцінки рШКФ (до лікування і через 23–45 днів після відміни досліджуваного препарату) рШКФ змінилася на –0,93 мл/хв/1,73 м2 (95% ДІ від –1,97 до 0,11) у групі емпагліфлозину і на –4,21 мл/хв/1,73 м2 (95% ДІ від –5,26 до –3,17) у групі плацебо. У таблиці 2 наводяться результати оцінки впливу емпагліфлозину на якість життя пацієнтів, загальну кількість госпіталізацій з будь-якої причини і частоту реєстрації вперше виявленого ЦД. Загальна смертність під час дослідження становила 13,4% у групі емпагліфлозину і 14,2% у групі плацебо (ВР 0,92, 95% ДІ 0,77–1,10) [4].
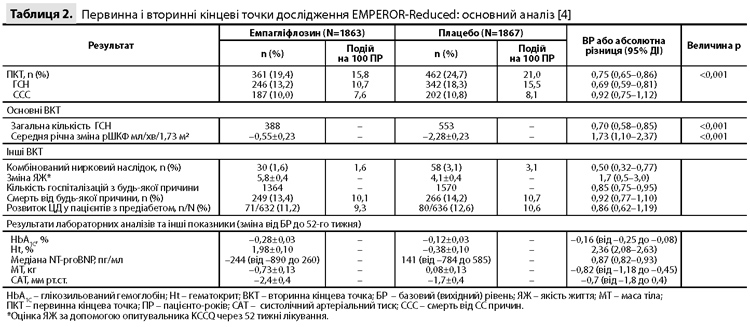
Інформація про зміни рівнів глікозильованого гемоглобіну, гематокриту, NT-proBNP, маси тіла і систолічного артеріального тиску в групах лікування за період від вихідного рівня до 52-го тижня терапії представлена в таблиці 2 [4]. Аналіз даних з безпеки показав, що неускладнені інфекції статевих шляхів виявлялися частіше в групі емпагліфлозину порівняно з групою плацебо. Водночас гіпоглікемія, ампутації кінцівок і переломи кісток – небажані явища, пов'язані із застосуванням іНГКТ-2 у деяких дослідженнях за участю хворих на ЦД2 [6, 7] – реєструвалися з однаковою частотою в групах плацебо і емпагліфлозину. Проблеми з безпекою, що спостерігалися при використанні інших препаратів для лікування СН (наприклад, гіпотензія, гіповолемія, ниркова дисфункція, брадикардія і гіперкаліємія), не виникали при використанні емпагліфлозину. Результати аналізу чутливості, проведеного після виключення даних 42 пацієнтів, які вибули з періоду подальшого спостереження, були зіставні з представленими вище результатами основних аналізів [4].
Аналізи в підгрупах: вплив комбінації сакубітрил/валсартан на ефективність і безпеку терапії емпагліфлозином Дані дослідження EMPEROR-Reduced додатково оцінювалися в ході декількох аналізів у підгрупах, серед яких особливе значення має аналіз ефектів емпагліфлозину залежно від застосування пацієнтами інгібітора неприлізину (сакубітрил у складі комбінації сакубітрил/валсартан) [8]. В основі зацікавленості до цього питання лежать відома ефективність монотерапії кожним з інгібіторів (сакубітрил і емпагліфлозин) у зниженні ризику смерті від СС причин і ГСН у пацієнтів з СН і зниженою ФВ ЛШ і очікуване (з урахуванням результатів моделювання) істотне зменшення ризику серйозних СС ускладнень при комбінованому застосуванні препаратів [9], яке, однак, до цього часу не перевірялося у великих клінічних дослідженнях (оскільки, наприклад, у дослідженні DAPA-HF тільки 10,7% учасників отримували на вихідному рівні сакубітрил/валсартан). Крім того, інтерес представляють досі невивчений характер взаємодії між ефектами іНГКТ-2 та інгібітора неприлізину (адитивний, потенціюючий або послабляючий) і, в цілому, можливість незалежної реалізації цих ефектів [8]. Вивчення цих аспектів в EMPEROR-Reduced стало можливим завдяки особливостям досліджуваної вибірки (більша кількість пацієнтів з важкою систолічною дисфункцією ЛШ в EMPEROR-Reduced порівняно з DAPA-HF), більшій кількості подій первинної кінцевої точки в групі плацебо (на 40% порівняно з групою плацебо в DAPA-HF) і більш ніж у 2 рази більшій кількості учасників, які отримували сакубітрил/валсартан на вихідному рівні [8]. Із 3730 рандомізованих пацієнтів 727 осіб (19,5%) приймали сакубітрил/валсартан перед початком лікування в подвійному сліпому режимі. Підгрупи пацієнтів, які отримували і не отримували сакубітрил, були зіставними за таким вихідним характеристикам, як вік, стать, функціональний клас СН, етіологія СН, функція нирок, наявність в анамнезі ГСН, наявність фібриляції передсердь і ЦД, а також використання бета-блокаторів та антагоністів мінералокортикоїдних рецепторів. Між тим, пацієнти, які отримували інгібітор неприлізину, частіше були жителями країн Північної Америки, мали більш низькі значення систолічного артеріального тиску, частоти серцевих скорочень і більш низькі рівні NTproBNP, і при цьому частіше отримували апаратне лікування СН (для всіх порівнянь р<0,001). І незважаючи на ці відмінності, порівняння пацієнтів, які отримували і не отримували сакубітрил у групі плацебо, продемонструвало порівнянність цих підгруп за ризиком смерті від СС причин і ГСН (р=0,79), загальною кількістю ГСН (р=0,67) і швидкістю зниження рШКФ (р=0,99). Слід зазначити, що серед пацієнтів, які не приймали комбінацію сакубітрил/валсартан на вихідному рівні, 8,9% пацієнтів у групі плацебо і 7,9% пацієнтів у групі емпагліфлозину почали лікування інгібітором неприлізину після рандомізації в EMPEROR-Reduced [8]. Результати оцінки залежності ефектів емпагліфлозину на
три основні (первинну і дві вторинні) кінцеві точки дослідження
EMPEROR-Reduced від фонової терапії комбінацією
сакубітрил/валсартан стисло представлені в таблиці 3 [8]. У
цілому, порівняно з плацебо, емпагліфлозин забезпечував зниження
сукупного ризику смерті від СС причин і ГСН на 23%
у пацієнтів, які не приймали інгібітор неприлізину (ВР 0,77,
95% ДІ 0,66–0,90, р=0,0008), і на 36% у пацієнтів, які приймали
інгібітор неприлізину (ВР 0,64, 95% ДІ 0,45–0,89, р=0,009).
Емпагліфлозин знизив загальну кількість ГСН на 29% (ВР 0,71, 95% ДІ 0,58–0,88, р=0,002) і 35% (ВР 0,65, 95% ДІ
0,42–1,00, р=0,052) відповідно (рис. 5) [8]. І, нарешті, емпагліфлозин у порівнянні з плацебо сповільнював швидкість
зниження рШКФ на 1,71±0,35 мл/хв/1,73 м2/рік (р<0,0001) і
на 1,92±0,80 мл/хв/1,73 м2
Обговорення результатів і висновки Отже, в дослідженні EMPEROR-Reduced застосування
іНГКТ-2 емпагліфлозину забезпечило зниження ризику смерті від СС причин і ГСН на 25% порівняно із застосуванням
плацебо. Ця різниця між групами лікування була перш за все
зумовлена 31% зниженням ризику ГСН і спостерігалася як
у пацієнтів з ЦД2, так і без ЦД на тлі отримання будь-якої
сучасної терапії СН. Додатково, терапія емпагліфлозином
асоціювалася зі зменшенням загальної кількості ГСН (перша
і повторні госпіталізації), а також з більш повільним зниженням рШКФ, причому останній ефект супроводжувався більш
низьким ризиком серйозних ниркових результатів (діаліз,
трансплантація нирок, важке стійке зниження рШКФ) [4]. Отримані результати можна порівняти з ефектами дапагліфлозину, що спостерігалися в дослідженні DAPA-HF [10],
з урахуванням того, що в досліджувану вибірку EMPERORReduced
входили пацієнти з більш низькою ФВ ЛШ і більш високими рівнями натрійуретичних пептидів порівняно з учасниками DAPA-HF, у результаті чого частота подій первинної
кінцевої точки в EMPEROR-Reduced була на 40% вищою, ніж
у DAPA-HF. Як наслідок, результати EMPEROR-Reduced підтверджують, що ефекти іНГКТ-2 поширюються на пацієнтів з більш важкими стадіями стабільної СН. Як в EMPERORReduced,
так і в DAPA-HF корисний вплив іНГКТ-2 на первинну
комбіновану кінцеву точку був зумовлений в основному
зниженням кількості перших ГСН (на 30% у DAPA-HF і
на 31% в EMPEROR-Reduced), у той час як зниження ризику
смерті від СС причин на тлі прийому іНГКТ-2 порівняно з
плацебо становило 8% в EMPEROR-Reduced і 18% у DAPAHF
[4, 10]. Слід зазначити, що в інших великомасштабних
дослідженнях за участю пацієнтів з ЦД2 зниження ризику
смерті від СС причин серед пацієнтів з аналогічним СС анамнезом
становило 41% на тлі приймання емпагліфлозину (ВР
0,59, 95% ДІ 0,44–0,79) і 8% – для дапагліфлозину (ВР 0,92,
95% ДІ 0,69–1,23) [5, 11], що підтверджує думку про неоднорідність
впливу іНГКТ-2 на виживання пацієнтів і відсутність
у одного представника класу переваг, пов'язаних із впливом
на смертність, перед іншими іНГКТ-2 [1]. Крім спостережуваних СС ефектів емпагліфлозин забезпечив
уповільнення темпів зниження рШКФ під час періоду
лікування в подвійному сліпому режимі, а також зниження
ризику подій комбінованого ниркового наслідку порівняно з
прийманням плацебо. Порівняння результатів оцінки рШКФ,
отриманих до початку лікування і через деякий час після
скасування емпагліфлозину/плацебо, показали більш виражене
зниження рШКФ у пацієнтів, які отримували плацебо.
Ці спостереження узгоджуються з результатами застосування
іНГКТ-2 у пацієнтів з ЦД2, але без СН [1]. Відповідно,
здатність емпагліфлозину сприятливо впливати на ниркову
функцію очевидна у пацієнтів з ЦД, хворих з СН і в осіб з
комбінацією ЦД + СН [4]. Результати аналізу в підгрупах, виділених з урахуванням
отримання фонової терапії інгібітором неприлізину
(сакубітрил в комбінації сакубітрил/валсартан), довели
здатність емпагліфлозину реалізовувати свої сприятливі
кардіоренальні ефекти навіть серед пацієнтів, які отримують
дуже якісне лікування СН, до яких відносяться хворі,
які приймають сакубітрил/валсартан. Важливо відзначити,
що поєднане застосування емпагліфлозину і комбінації
сакубітрил/валсартан демонструвало хорошу переносимість.
Відсутність несприятливої взаємодії між іНГКТ-2
і комбінацією сакубітрил/валсартан підтверджує існуючу
думку про те, що ці два класи препаратів мають абсолютно
різні механізми дії [8]. Висновок У дослідженні EMPEROR-Reduced, що проводилося за
участю пацієнтів з СН і важкою систолічною дисфункцією
ЛШ, застосування емпагліфлозину асоціювалося з більш
низьким ризиком комбінації смерті від СС причин і госпіталізації
з приводу СН і більш повільним прогресуванням ниркової
дисфункції порівняно з плацебо, незалежно від наявності
ЦД2. Важливо, що супутнє застосування комбінації сакубітрил/
валсартан (і, отже, оптимальна рекомендована терапія
СН) не зменшувало вираженість сприятливих кардіоренальних
ефектів емпагліфлозину; спільне застосування іНГКТ-2 і
інгібітора неприлізину було безпечним, добре переносилося
і, на думку авторів дослідження, є потенційно корисним для
пацієнтів з показаннями до такої терапії. Список літератури знаходиться в редакції Автор огляду Микола Горін Medicine Review 2021; 3 (62): 37 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2025. Усі права захищені.
|
мапа сайту корисні посилання |