Зменшення маси лівого шлуночка як один з механізмів реалізації кардіопротекторних ефектів емпагліфлозину: результати рандомізованого дослідження EMPA-HEART CardioLink-6На сьогоднішній день інгібітори натрій-глюкозного котранспортера 2 (іНГКТ2), початково призначені для корекції вуглеводних порушень при цукровому діабеті (ЦД), привертають дедалі більшу увагу як препарати, що знижують ризики несприятливих серцево-судинних (СС) подій при ЦД 2 типу (ЦД2) ефективніше, ніж стандартна протидіабетична терапія [1–5]. Зокрема, в дослідженні EMPA-REG OUTCOME (BI 10773 [Empagliflozin] Cardiovascular Outcome Event Trial in Type 2 Diabetes Mellitus Patients) за участю хворих на ЦД2 і встановленим діагнозом атеросклеротичного СС захворювання (АССЗ) іНГКТ2 емпагліфлозин демонстрував виражений кардіопротекторний ефект, забезпечуючи зниження частоти серйозних небажаних СС подій (МАСЕ) на 14%, ризику смерті від СС причин на 38%, ризику смерті від усіх причин на 32% і ризику госпіталізації з приводу серцевої недостатності (СН) на 35% [1]. Два інших іНГКТ2, канагліфлозин і дапагліфлозин, також пройшли оцінку у великих клінічних дослідженнях з аналізом СС наслідків у пацієнтів з і без АССЗ, а канагліфлозин додатково вивчався в дослідженні з оцінкою ниркових ефектів в учасників з ЦД2 і визначеним хронічним захворюванням нирок [6]. Ці великі дослідження підтвердили наявність у іНГКТ2 СС ефектів з особливо вираженим сприятливим впливом на ризик СН і комбінації госпіталізації з приводу СН і смерті від СС причин [2, 3]. Механізми реалізації СС клінічних ефектів іНГКТ2, зокрема ті, що сприяють зниженню ризику госпіталізації з приводу СН і смерті від СС причин, становлять значний інтерес [7–9]. Одним з таких механізмів, на думку вчених, може бути зумовлене пригніченням натрійзалежного транспорту глюкози зниження маси лівого шлуночка (МЛШ), оскільки, по-перше, МЛШ є сильним і незалежним предиктором розвитку СС подій, включно з інфарктом міокарда (ІМ), СН і СС смертю [10–16], по-друге, ступінь зменшення МЛШ у результаті фармакологічного або хірургічного втручання доведено корелює зі ступенем зниження СС ризику, і по-третє, згідно з попередніми даними, застосування іНГКТ2 емпагліфлозину асоціюється зі значним зниженням індексу МЛШ (іМЛШ, відношення МЛШ до площі поверхні тіла [ППТ] на початковому рівні). Щоб підтвердити або спростувати цю гіпотезу, Verma et al. провели подвійне сліпе плацебо-контрольоване рандомізоване дослідження з участю пацієнтів з ЦД2 та ішемічною хворобою серця (ІХС) (дослідження EMPA-HEART CardioLink-6), у якому за допомогою магнітно-резонансної томографії серця (сМРТ) відстежували динаміку зміни МЛШ на тлі терапії емпагліфлозином [17]. Нижче стисло викладена основна інформація про це дослідження.
Методи дослідження EMPA-HEART CardioLink-6 Набір учасників у дослідження EMPA-HEART CardioLink-6 проводився протягом періоду з 7 листопада 2016 р. по 5 квітня 2018 р. включно. До участі в дослідженні допускалися особи віком 40–80 років з рівнем глікозильованого гемоглобіну (HbA1c) 6,5–10,0%, діагнозом ІХС (перенесений ІМ або перенесена коронарна реваскуляризація методом черезшкірного коронарного втручання [ЧКВ] або аортокоронарного шунтування [АКШ]), розрахунковою швидкістю клубочкової фільтрації ≥60 мл/хв/1,73 м2, які одержували стабільну протидіабетичну терапію (ПДТ) протягом як мінімум 2 міс до зарахування в дослідження. Не допускалися до участі в дослідженні пацієнти з ЦД 1 типу, хворі, які вже отримують терапію іНГКТ2, агоністом рецептора глюкагоноподібного пептиду 1 або саксагліптином, особи з >4 епізодами помірної гіпоглікемії в місяць або з епізодом важкої гіпоглікемії протягом останніх 12 міс, пацієнти, які перенесли ЧКВ або АКШ протягом останніх 2 міс, пацієнти з індексом маси тіла >40 кг/м2, або фракцією викиду (ФВ) лівого шлуночка (ЛШ) <30%, або симптомами СН IV функціонального класу (ФК) за класифікацією Нью-Йоркської кардіологічної асоціації, хворі з анамнезом госпіталізації з приводу декомпенсованої СН протягом попередніх 3 міс або з важкою клапанною хворобою серця. На візиті вихідного рівня пацієнти проходили клінічне обстеження з оцінкою антропометричних даних, сМРТ, загальний клінічний і біохімічний аналізи крові і добове моніторування артеріального тиску (ДМАТ). Потім учасників рандомізували для отримання 6-місячної терапії емпагліфлозином 10 мг/добу або плацебо на додаток до стандартного лікування. Протягом 6-місячного періоду лікування були заплановані три візити в клініку, під час яких учасники також проходили клінічне обстеження і аналізи крові, а на останньому візиті повторювали сМРТ і ДМАТ. Результати сМРТ оцінювали два експерта, які не мали доступу до клінічних даних пацієнтів, а також до кодів рандомізації і відомостей про час проведення кожного сканування. Аналізи крові також включали визначення плазмових рівнів N-термінального фрагмента попередника мозкового натрійуретичного пептиду (NT-proBNP); результати аналізів оцінювали співробітники, які не мали доступу до коду рандомізації і даних про номер візиту [17]. Первинною кінцевою точкою дослідження була зміна іМЛШ за 6 міс відносно вихідного рівня; вторинні кінцеві точки включали міжгрупові відмінності по зміні (через 6 місяців лікування відносно вихідного рівня) кінцево-систолічного (КСО) і кінцево-діастолічного (КДО) об'ємів ЛШ (з корекцією і без корекції на ППТ), ФВ ЛШ і рівня NT-proBNP. Загальний запланований обсяг досліджуваної вибірки становив 96 осіб з урахуванням 5% передбачуваної частоти реєстрації неповних даних про первинну кінцеву точку. Статистичні аналізи проводилися з використанням підходу «intent-to-treat», згідно з яким дані всіх учасників аналізувалися в складі груп, визначених у ході рандомізації. Категоріальні дані представляли у вигляді абсолютної і відносної частоти, безперервні дані – у вигляді середнього значення зі стандартним відхиленням (СВ) або медіани з міжквартильним розмахом (МКР). Крім первинного аналізу даних проводили аналіз первинної кінцевої точки в підгрупах для оцінки впливу окремих характеристик учасників на ефективність емпагліфлозину. Також виконувалися додаткові аналізи чутливості для оцінки впливу альтернативних визначень іМЛШ, тривалості лікування, якості сканування або наявності гіпертрофії ЛШ на результати терапії [17].
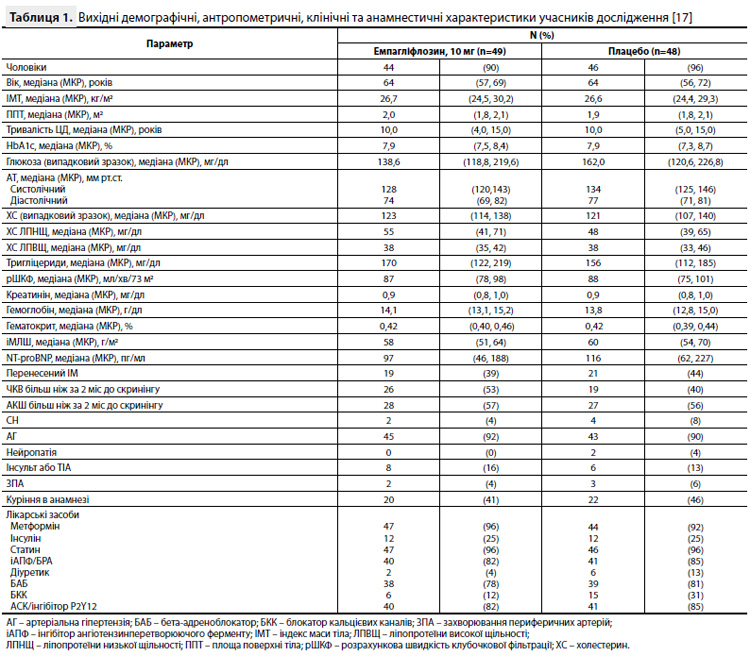
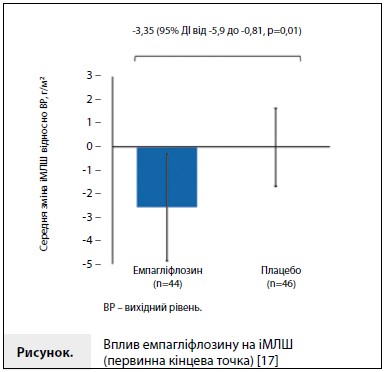
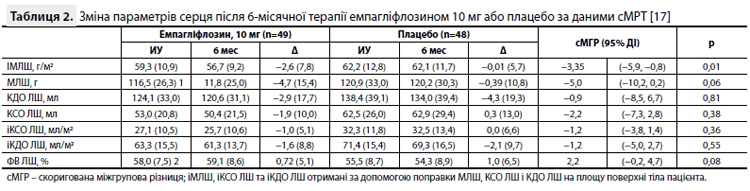
Результати дослідження EMPA-HEART CardioLink-6 У цілому 97 пацієнтів були рандомізовані (коефіцієнт рандомізації 1:1) для отримання емпагліфлозину 10 мг/добу (n=49) або плацебо (n=48); у результаті дані з первинної кінцевої точки через 6 міс були отримані у 90 пацієнтів. Демографічні дані і вихідні характеристики рандомізованих пацієнтів стисло представлені в таблиці 1 [17]. Середня тривалість ЦД2 в досліджуваній вибірці становила більше 10 років, 94% пацієнтів приймали метформін, 25% отримували інсулін. Більше 80% учасників отримували вторинну профілактику СС подій у вигляді науковообґрунтованої терапії, що включає застосування інгібіторів ангіотензинперетворюючого ферменту (іАПФ) або блокаторів рецепторів ангіотензину II (БРА), гіполіпідемічних і антитромбоцитарних препаратів [17]. Вихідний іМЛШ у пацієнтів у групах емпагліфлозину і плацебо становив 59,3 (10,9) і 62,2 (12,8) г/м2 відповідно. Зміна іМЛШ через 6 місяців лікування відносно вихідного рівня (первинна кінцева точка) становила -2,6 (7,8) і -0,01 (5,7) г/м2 у групах емпагліфлозину і плацебо відповідно. Скоригована міжгрупова різниця становила -3,35 г/м2 (95% довірчий інтервал від -5,9 до -0,81, p=0,01) (рис.). Аналіз чутливості з урахуванням використання різних способів обчислення іМЛШ підтвердив послідовне і значне зменшення МЛШ на тлі терапії емпагліфлозином [17]. Відомості про динаміку зміни КСО ЛШ, КДО ЛШ і ФВ ЛШ (вихідні значення, значення через 6 міс і 6-місячні зміни відносно вихідних значень) представлені в таблиці 2 [17]. Як видно з таблиці, зміни наведених показників у групах емпагліфлозину і плацебо були зіставними. Аналізи в підгрупах не виявили взаємодії між характеристиками пацієнтів і первинною кінцевою точкою дослідження, за винятком пацієнтів з вихідним значенням та іМЛШ >60 г/м2, у яких спостерігалося більш виражене зменшення іМЛШ порівняно з пацієнтами з іМЛШ <60 г/м2 на вихідному рівні (рвзаєм.=0,007) [17].
Аналіз лабораторних даних показав, що середній вихідний рівень HbA1c в обох групах становив приблизно 8,0%, при цьому середня зміна HbA1c за 6 міс лікування становила -0,4% (1,0%) і -0,3% (0,9%) у групах емпагліфлозину і плацебо відповідно (скоригована міжгрупова різниця -0,2%, 95% ДІ від -0,5% до 0,2%, р=0,41) [17]. Середній амбулаторний артеріальний тиск (АТ) на вихідному рівні становив 139/80 і 138/78 мм рт.ст. у групах емпагліфлозину і плацебо відповідно. У групі емпагліфлозину 6-місячна досліджувана терапія привела до зниження систолічного і діастолічного артеріального тиску на 7,9 (13,5) і 3,1 (7,5) мм рт.ст. відповідно, тоді як у групі плацебо середні показники систолічного і діастолічного АТ через 6 місяців лікування суттєво не відрізнялись від вихідних значень. Скоригована міжгрупова різниця становила -6,8 мм рт.ст. (95% ДІ від -11,2 до -2,3, р=0,003) і -3,2 мм рт.ст. (95% ДІ від -5,8 до -0,6, р=0,016) для систолічного і діастолічного АТ відповідно [17]. Середній вихідний показник гематокриту становив 42,6% (4,2%) і 41,3% (3,4%) у групах емпагліфлозину і плацебо відповідно. Через 6 місяців лікування показник збільшився на 2,4% (3,0%) і 0,4% (2,8%) відносно початкового рівня у групах емпагліфлозину і плацебо відповідно. У результаті, скоригована міжгрупова різниця за величиною гематокриту становила 2,3% (95% ДІ 1,1–3,6%, р=0,0003) [17]. У групі, що приймала емпагліфлозин, середня вихідна частота серцевих скорочень (ЧСС) становила 75 (9) уд/хв, а у групі плацебо – 70 (9) уд/хв; через 6 місяців лікування середня ЧСС знизилася на 0,3 (8,2) уд/хв у групі емпагліфлозину і збільшилася на 2,6 (7,5) уд/хв у групі плацебо порівняно з вихідним рівнем. Проте, показник скоригованої різниці, рівний -0,42 (95% ДІ від -3,54 до 2,7, р=0,79), не виявив істотних міжгрупових відмінностей [17]. Медіана (МКР) значень NT-proBNP на вихідному рівні становила 97,0 (46,3, 188,3) і 115,5 (61,8, 226,8) пг/мл у групах емпагліфлозину і плацебо відповідно. Через 6 місяців лікування відповідні значення становили 102 (58,5, 201,0) і 99 (62,0, 169,0) пг/мл відповідно зі скоригованою міжгруповою різницею, рівною 7,4 пг/мл (95% ДІ від -10,3 до 25,1, р=0,42), яка демонструє відсутність істотних відмінностей між групами емпагліфлозину і плацебо [17]. Аналіз даних про небажані явища показав, що емпагліфлозин добре переносився і не був пов'язаний з надмірною частотою розвитку побічних ефектів або відміни досліджуваного лікування порівняно з групою плацебо. За 6 міс спостереження у досліджуваній вибірці не було зареєстровано жодної СС події або летального наслідку [17].
Обговорення дослідження EMPA-HEART CardioLink-6 Отже, дослідження EMPA-HEART CardioLink-6 продемонструвало, що додавання емпагліфлозину до стандартної ПДТ у пацієнтів з ЦД2 і ІХС було пов'язане зі значним зниженням іМЛШ порівняно з плацебо. Застосування емпагліфлозину також приводило до значного зменшення середнього амбулаторного систолічного АТ і не впливало на циркулюючі рівні NT-proBNP [17]. Вважається, що до механізмів, які поліпшують наслідки СН на тлі терапії іНГКТ2, відносяться стимуляція натрійурезу і осмотичного діурезу, зниження перед- і постнавантаження на серце, інгібування Na+/H+ обміну в серці і оптимізація біоенергетичних процесів в міокарді [7, 9, 18, 19], проте до цього часу невідомо, чи здатні ці зміни впливати на структуру і функцію серця. І хоча звіти про результати експериментів і клінічні випадки свідчать про те, що іНГКТ2 потенційно можуть покращувати структуру і функцію серця [20, 21], дослідження EMPA-HEART CardioLink-6 стало першим рандомізованим клінічним дослідженням, яке переконливо довело, що іНГКТ2 емпагліфлозин сприяє значному зниженню МЛШ у пацієнтів з ЦД та ІХС. Примітно, що благотворний вплив на іМЛШ розвивався незабаром після початку терапії і зберігався протягом 6 місяців лікування, що узгоджується з ранньою розбіжністю кривих виживаності Каплана-Меєра, які відображали випадки смерті від СС причин і госпіталізації з приводу СН, у дослідженні EMPA-REG OUTCOME. Крім того, важливо, що таке зменшення МЛШ спостерігалося у вибірці стабільних пацієнтів, які отримували вторинну СС профілактику з нормальним вихідним іМЛШ і рівнем АТ, відносно добре контрольованим інгібіторами ренін-ангіотензинової системи. Слід зазначити, що значення МЛШ, визначене за допомогою сМРТ, залежить як від товщини стінок серця, так і від об’ємів ЛШ; тому виявлене зменшення МЛШ без зміни КДО ЛШ і КСО ЛШ говорить про те, що досліджувана терапія безпосередньо впливала на товщину серцевої стінки. Точні механізми, що лежать в основі зменшення товщини стінки ЛШ, ще тільки належить з'ясувати, але, ймовірно, вони пов'язані зі зменшенням маси кардіоміоцитів, зміною вмісту води в інтерстиціальному просторі або одночасно з обома цими процесами.
Використання ДМАТ дозволило виявити помітне зниження денного і нічного систолічного та діастолічного АТ у пацієнтів з групи емпагліфлозину, що узгоджується з даними дослідження SACRA (SGLT2 Inhibitor and ARB Combination Therapy in Patients With Diabetes and Uncontrolled Nocturnal Hypertension), яке продемонструвало аналогічне зниження загального, денного і нічного АТ на тлі застосування іНГКТ2 [22]. Однак подальший аналіз даних EMPA-HEART CardioLink-6 показав, що зниження іМЛШ, яке спостерігалось, не було пов'язане з антигіпертензивним ефектом емпагліфлозину (коефіцієнт кореляції Пірсона 0,08, 95% ДІ від -0,14 до 0,29). І хоча виключити певний вплив зниження АТ на процеси зворотного ремоделювання міокарда та зменшення МЛШ на цей час неможливо, отримані результати припускають наявність у іНГКТ2 інших механізмів дії на МЛШ, що підтверджують звіти з деяких досліджень, у яких спостерігалося зниження МЛШ за відсутності змін АТ [15, 23]. Наприклад, у дослідженні LIFE (Losartan Intervention for Endpoint Reduction) зменшення МЛШ (за даними електрокардіографії) не залежало від призначеного лікування та рівня АТ і було пов'язане зі зниженням загальної смертності, смертності від СС причин, ризику раптової серцевої смерті, ІМ, СН, фібриляції передсердь та інсульту [15]. Важливо відзначити, що аналіз у підгрупах виявив більш виражене зниження іМЛШ серед учасників з більш високим вихідним іМЛШ, які отримували емпагліфлозин. Це спостереження узгоджується з результатами нещодавно опублікованого ретроспективного аналізу в підгрупах дослідження EMPA-REG OUTCOME, який показав, що пацієнти з ехо-ознаками гіпертрофії ЛШ демонстрували більш виражене зниження ризику МАСЕ під дією емпагліфлозину [24], і додатково підтверджує гіпотезу про те, що зменшення МЛШ може вносити певний внесок у реалізацію сприятливих СС ефектів емпагліфлозину. Як і інші дослідження, EMPA-HEART CardioLink-6 має сильні сторони і обмеження, які необхідно враховувати при інтерпретації результатів. Основною перевагою дослідження є використання сМРТ, що забезпечує пряме вимірювання МЛШ. Обмеження дослідження включають переважання учасників чоловічої статі (при цьому, слід врахувати, що інші дослідження не виявили статевих відмінностей у результатах застосування іНГКТ2 або в динаміці зміни МЛШ під дією інших варіантів терапії), невелику досліджувану вибірку і порівняно короткий період спостереження, виключення з дослідження пацієнтів з хронічним захворюванням нирок і встановленою СН, а також представлену пацієнтам можливість змінювати тип, дозу і/або частоту приймання будь-яких супутніх лікарських препаратів під час участі в дослідженні. Також слід взяти до уваги, що з урахуванням характеристик досліджуваної вибірки (пацієнти з ЦД2 та ІХС без СН або значної дисфункції ЛШ) можливість емпагліфлозину зменшувати МЛШ у пацієнтів без АССЗ або в осіб із СН/дисфункцією ЛШ потребує подальшого вивчення [17].
Висновки Дослідження EMPA-HEART CardioLink-6, яке проводило рандомізоване порівняння ефектів емпагліфлозину і плацебо, показало, що інгібування натрійзалежного транспорту глюкози під дією емпагліфлозину приводить до значного зменшення іМЛШ у пацієнтів з ЦД2 та ІХС. Важливо, що цей ефект спостерігався в осіб з хорошим рівнем компенсації вуглеводних порушень на тлі стандартної ПДТ, які отримували вторинну профілактику СС ускладнень, і розвивався в ранні терміни після включення у схему лікування емпагліфлозину. Виявлений ефект на МЛШ може бути одним з факторів, що пояснюють кардіопротекторні ефекти емпагліфлозину, які спостерігалися в більших дослідженнях з оцінкою СС наслідків, зокрема в EMPA-REG OUTCOME.
Список літератури знаходиться в редакції
Автор огляду Віктор Мицьо
 Medicine Review 2021; 2 (61): 37 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2024. Усі права захищені.
|
мапа сайту корисні посилання |