Порівняння ефективності та безпеки антиагрегантів при гострому коронарному синдромі в умовах реальної практики: результати великого канадського реєстрового дослідженняДіючі керівництва з ведення пацієнтів з гострим коронарним синдромом (ГКС) вказують, що тікагрелор має перевагу перед клопідогрелем як компонент подвійної антитромбоцитарної терапії (ПАТ, ацетилсаліцилова кислота [АСК] плюс інгібітор P2Y12-рецепторів тромбоцитів), незалежно від стратегії (консервативна або інвазивна) ведення пацієнта [1, 2]. Ця рекомендація в основному базується на результатах дослідження Platelet Inhibition and Patient Outcomes (PLATO) [3], у якому пацієнти з ГКС, які отримували тікагрелор, демонстрували 16% зниження відносного ризику основних несприятливих коронарних подій (major adverse coronary events, MACE) і 22% зниження відносного ризику смерті від усіх причин порівняно з групою пацієнтів, які отримували клопідогрель. При цьому більш висока ефективність тікагрелора супроводжувалася 19% збільшенням відносного ризику великих кровотеч, не пов'язаних з аортокоронарним шунтуванням (АКШ), і 84% збільшенням відносного ризику задишки, яка, як правило, була нетривалим явищем легкого ступеня тяжкості [3–6]. Водночас, не зважаючи на високу інформативність, проспективні інтервенційні клінічні дослідження не можуть повною мірою спрогнозувати результати застосування того чи іншого препарату в реальній клінічній практиці, оскільки пацієнти, які отримують лікування в звичних умовах, часто мають значні відмінності від учасників клінічних досліджень, у тому числі більш високі ризики MACE та кровотечі, більшу кількість супутніх захворювань, менші шанси на отримання науково-обгрунтованої терапії та меншу прихильність до виконання призначень лікаря [7]. Так, за даними реєстрового дослідження Turgeon et al., 32% послідовно реєстрованих пацієнтів з інфарктом міокарда (ІМ) не відповідали критеріям участі в сучасних дослідженнях антиагрегантної терапії, у тому числі PLATO [8]. У зв’язку з цим спостережні дослідження можуть доповнювати інформацію, отриману в проспективних клінічних дослідженнях, за рахунок оцінки ефекту лікування в репрезентативних вибірках з урахуванням перерахованих факторів і виявлення перешкод на шляху до повторення результатів, які спостерігаються в рандомізованих клінічних дослідженнях. Одним з таких спостережних досліджень стала робота канадських вчених Turgeon et al., присвячена порівняльній оцінці впливу тікагрелору та клопідогрелю на ризик MACE на основі даних з популяційного регістру Alberta Provincial Project for Outcome Assessment in Coronary Heart Disease, що включає всіх пацієнтів, які пройшли черезшкірне коронарне втручання (ЧКВ) з приводу ГКС в географічному регіоні з універсальним доступом до медичної допомоги та ресурсів охорони здоров'я [9]. Автори припустили, що застосування тікагрелору буде пов'язано з меншим ризиком МАСЕ, ніж використання клопідогрелю. Другорядні цілі дослідження включали оцінку безпеки тікагрелору порівняно з клопідогрелем, а також зв’язки між прихильністю до лікування, постійністю дотримання рекомендацій і заміною антитромбоцитарного препарату з одного боку і подіями МАСЕ – з іншого.
Методологія дослідження та досліджувана вибірка пацієнтів У регістр Alberta Provincial Project for Outcome Assess ment in Coronary Heart Disease проспективно заносяться докладні клінічні дані про всіх пацієнтів, які пройшли коронарну ангіографію в провінції Альберта, Канада (населення приблизно 4,3 млн осіб) [10]. На основі даних з цього регістру були визначені досліджувана вибірка пацієнтів, вихідні характеристики учасників і параметри процедури, а також отримані дані про смерть і виконання коронарних втручань. Для збору даних про застосування інгібіторів P2Y12-рецепторів та інших рецептурних лікарських препаратів, а також відомостей про прихильність до прийому інгібіторів P2Y12-рецепторів, постійне дотримання рекомендацій і заміну антиагреганта використовували базу даних Pharmaceutical Information Network, у якій міститься інформація про всі рецептурні препарати, які надали амбулаторним пацієнтам в аптеках провінції Альберта, у тому числі дати продажу і кількість лікарського препарату. Джерелом інформації про результати лабораторних аналізів була база даних AlbertaHealth Services Laboratory Services, джерелом відомостей про досліджувані випадки – система Discharge AbstractDatabase and National Ambulatory CareReporting System (містить відомості про звернення до відділень невідкладної допомоги [ВНД] і госпіталізацію, у тому числі дати надходження в стаціонар і виписки зі стаціонару, а також код діагнозу згідно з класифікацією МКХ-10) [9].
У досліджувану когорту включали пацієнтів віком понад 18 років, що мали ЧКВ з приводу ГКС за період з 1 квітня 2012 р. по 31 березня 2016 р., які були виписані живими після індексної госпіталізації і реалізували перший рецепт на клопідогрель або тікагрелор протягом 31 дня після проходження ЧКВ. Особи, які одержували інгібітори P2Y12-рецепторів (клопідогрель, прасугрел або тікагрелор) протягом 120 днів до індексного ЧКВ, виключалися з досліджуваної вибірки, оскільки набір учасників у дослідження був обмежений пацієнтами після ЧКВ, яким препарати цієї групи призначалися вперше [9]. Прихильність до лікування оцінювали за допомогою показника прихильності до поповнення запасів препарату (medication refill adherence, MRA) [11, 12], який розраховувався за формулою: MRA (%) = (загальна кількість денних запасів препарату на інтервал часу/ загальна кількість днів у інтервалі часу) × 100%. Значення MRA ≥80% вказувало на прихильність пацієнта до лікування (аналогічний параметр використовувався в попередніх дослідженнях при ГКС) [3, 13]. Якщо інтервал між реалізаціями рецептів на інгібітор P2Y12-рецепторів не перевищував кількість денних запасів препарату плюс 15 днів, то таку ситуацію розцінювали як постійне дотримання призначень лікаря. Під заміною антиагреганта розуміли реалізацію одного або декількох рецептів на інгібітор P2Y12-рецепторів, відмінний від першого призначеного препарату, протягом 365 днів після індексного явища (ЧКВ) [9]. Оскільки в періоді дослідження прийом АСК в дозі 81 мг/добу був стандартом медичної допомоги для пацієнтів після ГКС без протипоказань до прийому АСК, малося на увазі, що всі учасники дослідження протягом періоду спостереження безперервно отримували цю дозу препарату. Первинною кінцевою точкою дослідження була комбінація подій MACE, визначена як сукупність смерті від усіх причин, госпіталізації з приводу нефатального ГКС, коронарної реваскуляризаціі (не враховуючи планове ЧКВ) чи тромбозу стента, протягом 365 днів після індексної госпіталізації. Вторинні кінцеві точки включали сукупність смерті від усіх причин, госпіталізації з приводу ГКС та ішемічного інсульту; госпіталізацію з приводу великої кровотечі; звернення до ВНД у зв'язку із задишкою [9]. Результати були представлені у вигляді часток (для категорійних змінних), медіан з міжквартильним розмахом (МКР, для безперервних змінних), відношень ризиків (ВР) і 95% довірчих інтервалів (ДІ) [9].
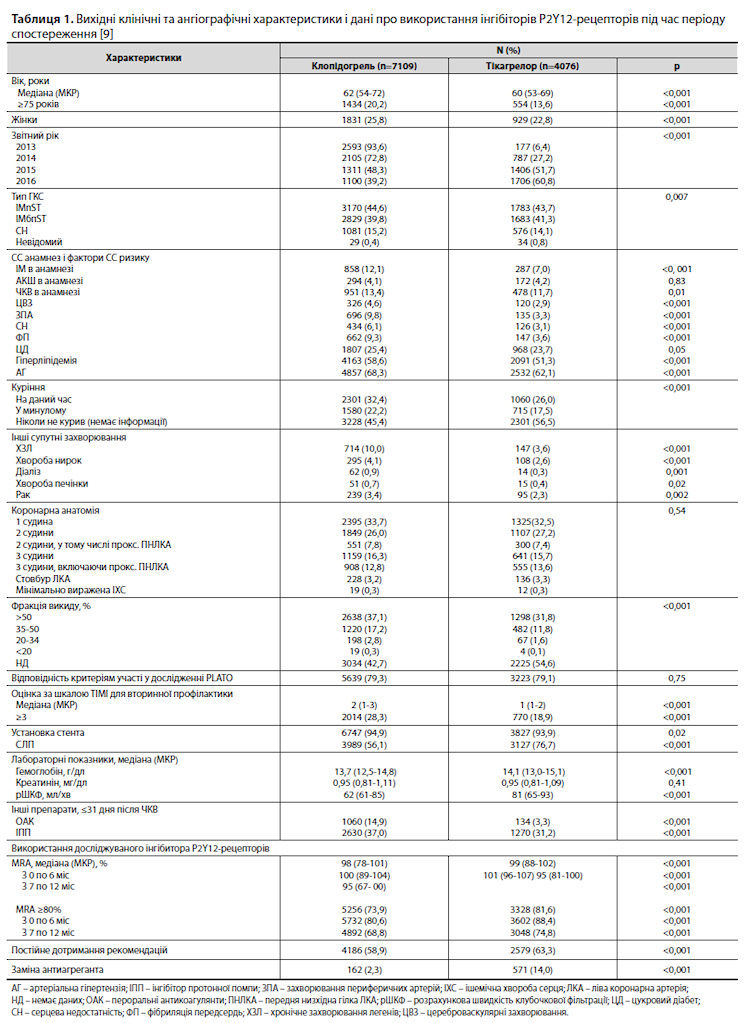
Результати дослідження Вихідні характеристики. З 1 квітня 2012 р. по 31 березня 2016 р. у цілому 13 897 пацієнтів пройшли ГКС з приводу ЧКВ в провінції Альберта, Канада. З них 11 185 пацієнтів (80,5%) реалізували як мінімум 1 рецепт на інгібітор P2Y12-рецептора протягом 31 дня після ЧКВ і відповідали всім критеріям участі в дослідженні. Клопідогрель був інгібітором P2Y12-рецепторів, що найчастіше призначався під час дослідження (7109 з 11 185 пацієнтів [63,6%]), проте використання тікагрелору неухильно росло і в другій половині дослідження препарат використовувався у 3112 з 5523 пацієнтів (56,3 %) (табл. 1) [9].
Медіана віку (МКР) учасників становила 61 (54–71) рік; 2760 (24,7%) учасників були жінками, у 4953 (44,3%) при надходженні до стаціонару був діагностований ІМ з підйомом сегмента ST. Медіана (МКР) часу, через який пацієнти реалізували свій перший амбулаторний рецепт на інгібітор P2Y12-рецепторів, становила 3 (1–4) дні після індексного ЧКВ і 1 (0–3) день після виписки з лікарні. У таблиці 1 представлені вихідні характеристики пацієнтів, які отримували інгібітори P2Y12-рецепторів. Пацієнти, які отримували тікагрелор, були статистично значно молодшими, серед них було мало жінок, і крім того вони демонстрували меншу частоту попереднього ІМ, інших серцево-судинних (СС) захворювань, факторів СС ризику і супутніх захворювань порівняно з пацієнтами, які отримували клопідогрель. Також пацієнти в групі тікагрелору частіше отримували стенти з лікарським покриттям (СЛП) та рідше отримували рецепт на пероральний антикоагулянт протягом 31 дня після ЧКВ порівняно з групою клопідогрелю [9]. Події МАСЕ. У нескорегованих аналізах амбулаторне використання тікагрелору було пов'язане з більш низьким ризиком MACE, ніж застосування клопідогрелю (ВР 0,84; 95% ДІ 0,74– 0,95) (табл. 2). Нескореговані показники смертності також були нижчі в групі тікагрелору, у той час як міжгрупові відмінності з частоти госпіталізації з приводу ГКС, коронарної реваскуляризації чи комбінаціі смерті, ГКС та ішемічного інсульту не виявлені. Після багатофакторного коригування, що включає показники вихідного рівня, перераховані в таблиці 1, і дані про прихильність до лікування, відмінності між тікагрелором і клопідогрелем по частоті подій MACE (скореговане ВР [сВР] 0,97; 95% ДІ 0,85– 1,10) та іншим СС результатам втратили статистичну значущість (табл. 2) [9]. Безпека. У нескорегованих аналізах тікагрелор не був пов'язаний із статистично значимо більшим ризиком великої кровотечі порівняно з клопідогрелем (ВР 1,09; 95% ДІ 0,93–1,27). Однак оцінка за допомогою повністю скоригованої моделі показала, що застосування тікагрелору було пов'язане з більш високим ризиком великої кровотечі порівняно з клопідогрелем (сВР 1,51, 95% ДІ 1,29–1,78) (табл. 2), що в основному було зумовлено збільшенням частоти шлунково-кишкових (сВР 2,02; 95% ДІ 1,52–2,68) і легеневих кровотеч (сВР 1,49; 95% ДІ 1,15–1,93) у групі тікагрелору. Крім того, тікагрелор був пов'язаний із статистично значимо більшим ризиком звернення у ВНД з приводу задишки як до, так і після коригування з урахуванням наявних чинників (сВР 1,98; 95% ДІ 1,47–2,65) (табл. 2) [9]. Зв'язок МАСЕ з прихильністю до лікування, постійним дотриманням рекомендацій і заміною антиагреганта. Пацієнти, які отримували тікагрелор, демонстрували більш високу прихильність до терапії інгібітором P2Y12-рецептора протягом цього дослідження, порівняно з групою клопідогрелю (3328 [81,6%] vs 5256 [73,9%]; р<0,001). У другому півріччі лікування відзначалося зниження медіани MRA в обох групах; постійне дотримання рекомендацій щодо приймання інгібітора P2Y12-рецепторів протягом року лікування продемонстрували 2579 пацієнтів у групі тікагрелору (63,3%) і 4186 – у групі клопідогрелю (58,9%) (р<0,001) (табл. 3). При цьому показники частоти подій МАСЕ на тлі прийому тікагрелору і клопідогрелю істотно не розрізнялися, незалежно від прихильності до лікування, постійності дотримання рекомендацій та заміни антиагреганта (табл. 3). У повній когорті частота MACE була очікувано нижчою у пацієнтів з рівнем прихильності до терапії інгібітором P2Y12-рецептора .80% порівняно з прихильністю < 80% (сВР 0,79; 95% ДІ 0,69–0,90) [9]. Заміна інгібітора P2Y12-рецептора сталася у 571 пацієнта у групі тікагрелору (14,0%) і 162 пацієнтів, які отримували клопідогрель (2,3%) (табл. 1), і не була пов'язана з підвищеним ризиком MACE (сВР 0,56; 95% ДІ 0,25–1,25 – при первинному використанні клопідогрелю; сВР 0,88; 95% ДІ 0,65–1,20 – при первинному використанні тікагрелору) (табл. 3). Протягом 30 днів після відвідування ВНД у зв’язку з задишкою, 28 з 112 пацієнтів, які приймали тікагрелор (25,0%), змінили антиагрегант; у групі клопідогрелю аналогічна заміна сталася в 1 випадку (1 з 115 пацієнтів, 0,9%, р<0,001). Аналогічним чином, більшість пацієнтів, які отримували тікагрелор, змінили антикоагулянт протягом 30 днів після епізоду великої кровотечі (18 з 255 пацієнтів [7,1%] vs 2 з 439 [0,5%] відповідно; р<0,001) [9]. Аналіз чутливості (з використанням даних пацієнтів з таким самим вихідним рівнем ризику, propensity score– matched analysis) також не виявив статистично значущої різниці між тікагрелором і клопідогрелем по частоті подій МАСЕ (ВР 1,00; 95% ДІ 0,86–1,17), але підтвердив вищий ризик великої кровотечі (ВР 1,52; 95% ДІ 1,24–1,87) і задишки (ВР 2,42; 95% ДІ 1,70–3,45) при використанні тікагрелору. Відмінності за частотою МАСЕ та її компонентів також були відсутні після коригування з урахуванням індексу кардіоспецифічної коморбідності [9]. Результати аналізів частоти МАСЕ, великої кровотечі і задишки у підгрупах, виділених з урахуванням віку пацієнтів, наявності/відсутності цукрового діабету, величини розрахункової швидкості клубочкової фільтрації, групи ризику, показали результати, зіставні з результатами, отриманими в загальній вибірці пацієнтів.
Обговорення і висновки У цьому великому, сучасному популяційному когортному дослідженні за участю пацієнтів, які перенесли ЧКВ з приводу ГКС, амбулаторне застосування тікагрелору не було пов'язане з більш низьким ризиком MACE порівняно з клопідогрелем, але асоціювалося з підвищеним ризиком великої кровотечі і задишки. Водночас, прихильність до лікування будь-яким інгібітором P2Y12-рецепторів була пов'язана з 21% зниженням відносного ризику MACE порівняно з відсутністю подібної прихильності [9]. Відмінність результатів роботи Turgeon et al. від результатів попередніх досліджень клопідогрелю і тікагрелору обумовлена різною методологією, різними вибірками пацієнтів, а також останніми досягненнями інтервенційної кардіології. Рандомізоване клінічне дослідження PLATO – основне дослідження тікагрелору при ГКС, було міжнародним дослідженням, у яке увійшли пацієнти з усіма можливими підтипами ГКС, з різними стратегіями лікування, при цьому ЧКВ виконувалися в основному з використанням металевих стентів та СЛП першого покоління, до того ж результати дослідження PLATO включали і внутрішньолікарняні результати [3]. Велике наглядове реєстрове дослідження SWEDEHEART [14], чиї результати також розходяться з результатами дослідження Turgeon et al., не було обмежене пацієнтами з ГКС, які пройшли ЧКВ, у звіті про нього не вказаний відсоток пацієнтів, які отримали СЛП другого покоління, а інформація про тривалість застосування препаратів не підтверджувалася аналізом прихильності до лікування на основі відомостей про реалізацію рецептів і результатів опитування пацієнтів. Як і в дослідженні Turgeon et al., у SWEDEHEART [14] не враховувалися внутрішньолікарняні результати і враховувалися лише ті пацієнти, які дожили до виписки зі стаціонару. Дослідження Turgeon et al., у свою чергу, було обмежено хворими з ГКС, які перенесли ЧКВ, дожили до виписки зі стаціонару, вперше почали прийом інгібітора P2Y12-рецепторів і при цьому в більшості своїй отримали СЛП другого покоління, які мають покращений профіль безпеки, включаючи більш низький ризик тромбозу стента [15]. Важливість останнього фактора підтверджується тим, що в когортному дослідженні Dutch CHANGE DAPТ за участю пацієнтів з ГКС, які пройшли ЧКВ з імплантацією виключно СЛП другого покоління, статистично значущі відмінності за частотою MACE між тікагрелором і клопідогрелем також були відсутні [16]. У сукупності, ці дослідження показують, що в епоху СЛП другого покоління підвищена антитромбоцитарна активність тікагрелору може не призводити до підвищення ефективності ПАТ, особливо після виписки пацієнтів зі стаціонару. Другим важливим результатом дослідження Turgeon et al. було підвищення ризику великої кровотечі на тлі прийому тікагрелору. З огляду на те, що пацієнти, які перенесли АКШ під час індексної госпіталізації, виключалися з дослідження Turgeon et al., отриманий результат узгоджується з підвищеним ризиком не пов'язаних з АКШ кровотеч у групі тікагрелору дослідження PLATO [3]. Крім того, вибірка пацієнтів у дослідженні Turgeon et al. складалася з осіб з більш високим ризиком кровотеч порівняно з учасниками клінічних досліджень, що підтверджується більш високою частотою великих кровотеч у групі тікагрелору порівняно з показником з PLATO (6,8 vs 4,5%), незважаючи на більш суворе визначення кровотечі, що використовується Turgeon et al., і виключення кровотеч (у тому числі перипроцедурні кровотечі), які сталися під час індексної госпіталізації [3]. Аналогічним чином, пацієнти у групі тікагрелору в 2 рази частіше зверталися у ВНД з приводу задишки порівняно з хворими з групи клопідогрелю. Хоча задишка, викликана тікагрелором, зазвичай є тимчасовим і легким явищем, у багатьох пацієнтів вона персистує і знижує якість життя, що збільшує навантаження на систему охорони здоров'я, знижує прихильність до лікування і нерідко призводить до передчасного скасування препарату [3–6, 17]. І, нарешті, дослідження Turgeon et al. показало, що прихильність до прийому інгібітору P2Y12-рецепторів була більш тісно пов'язана з ризиком MACE, ніж вибір конкретного антиагреганта. Цей висновок підтримує попередні спостереження, згідно з якими передчасне скасування інгібітору P2Y12-рецепторів асоціюється з підвищеним ризиком смерті, повторної госпіталізації і тромбозу стента [18, 19]. Деякі фактори, пов'язані з більш низькою прихильністю до прийому інгібіторів P2Y12-рецепторів, включаючи більш виражену коморбідність і використання пероральних антикоагулянтів, були більш поширені у групі пацієнтів, які отримували клопідогрель у дослідженні Turgeon et al. Це частково могло пояснити менший рівень прихильності і постійності дотримання рекомендацій з лікування серед пацієнтів, які отримували клопідогрель, порівняно з хворими у групі тікагрелору. Отримані результати підкреслюють, як важливо регулярно питати пацієнтів, чи приймають вони призначені препарати відповідно до рекомендацій лікаря, а також виявляти і усувати фактори, що впливають на прихильність, у тому числі високу вартість препаратів, побічні ефекти, а також незручності, пов'язані з кількістю таблеток або частотою прийому препарату. При інтерпретації результатів дослідження Turgeon et al. слід враховувати низку обмежень, включаючи наглядовий характер дослідження; виключення випадків, які розвинулися під час індексної госпіталізації; а також спосіб оцінки тривалості лікування, прихильності і постійності дотримання рекомендацій (заснованій на припущенні, що пацієнти приймають усю отриману за рецептом кількість лікарського препарату), який може призвести до завищення показника прихильності до лікування.
Висновок Таким чином, Turgeon et al. встановили, що у великій репрезентативній популяційній когорті пацієнтів, які пройшли ЧКВ з приводу ГКС (як правило з використанням СЛП другого покоління), застосування тікагрелору не було пов'язане зі зниженням ризику МАСЕ порівняно з клопідогрелем, але сприяло підвищенню ризику великих кровотеч і частоти звернення до ВНД з приводу задишки. Також було показано, що для зниження ризику МАСЕ у зазначеній вибірці пацієнтів прихильність до лікування інгібітором P2Y12-рецепторів була важливіша ніж вибір конкретного антиагреганта. Література 1. Mehta S., Bainey K., CantorW. et al; members of the Secondary Panel. 2018 Canadian Cardiovascular Society / Canadian Association of Interventional Cardiology focused update of the guidelines for the use of antiplatelet therapy. Can J Cardiol. 2018; 34 (3): 214-233. 2. Levine G., Bates E., Bittl J. et al. 2016 ACC / AHA guideline focused update on duration of dual antiplatelet therapy in patients with coronary artery disease : a report of the American College of Cardiology / American Heart Association Task Force on Clinical Practice Guidelines : an update of the 2011 ACCF / AHA / SCAI guideline for percutaneous coronary intervention, 2011 ACCF / AHA guideline for coronary artery bypass graft surgery, 2012 ACC / AHA / ACP / AATS / PCNA / SCAI / STS guideline for the diagnosis and management of patients with stable ischemic heart disease, 2013 ACCF / AHA guideline for the management of ST-elevation myocardial infarction, 2014 AHA / ACC guideline for the management of patients with non -ST-elevation acute coronary syndromes, and 2014 ACC / AHA guideline on perioperative cardiovascular evaluation and management of patients undergoing noncardiac surgery. Circulation. 2016 року; 134 (10 ): e 123-e155. 3. Wallentin L., Becker R., Budaj A. et al; PLATO Investigators. Ticagrelor versus clopidogrel in patients with acute coronary syndromes. N Engl J Med. 2009 року; 361 (11): 1045-1057. 4. Storey R., Becker R., Harrington R. et al. Characterization of dyspnoea in PLATO study patients treated with ticagrelor or clopidogrel and its association with clinical outcomes. Eur Heart J. 2011 року; 32 (23): 2945-2953. 5. Storey R., Bliden K., Patil S. et al; ONSET / OFFSET Investigators. Incidence of dyspnea and assessment of cardiac and pulmonary function in patients with stable coronary artery disease receiving ticagrelor, clopidogrel, or placebo in the ONSET / OFFSET study. J AmColl Cardiol. 2010 року; 56 (3): 185-193. 6. Bonaca M., Bhatt D., Cohen M. et al; PEGASUS-TIMI 54 Steering Committee and Investigators. Long-term use of ticagrelor in patients with priormyocardial infarction. N Engl J Med. 2015; 372 (19): 1791-1800. 7. Kennedy-Martin T., Curtis S., Faries D. et al. A literature review on the representativeness of randomized controlled trial samples and implications for the external validity of trial results. Trials. 2015; 16 (1): 495. 8. Turgeon J., Wang T., Li S. et al. Clinical trial participation aftermyocardial infarction in a national cardiovascular data registry. JAMA. 2014; 312 (8): 841-843. 9. Turgeon R., Koshman S., Youngson E. et al. Association of Ticagrelor vs Clopidogrel With Major Adverse Coronary Events in Patients With Acute Coronary Syndrome Undergoing Percutaneous Coronary Intervention. JAMA Intern Med. Published online January 13, 2020. 10. Ghali W., Knudtson M. Overview of the Alberta provincial project for outcome assessment in coronary heart disease : on behalf of the APPROACH investigators. Can J Cardiol. 2000; 16 (10): 12251230. 11. Hess L., Raebel M., Conner D., Malone D. Measurement of adherence in pharmacy administrative databases : a proposal for standard definitions and preferred measures. Ann Pharmacother. 2006; 40 (78): 1280-1288. 12. Andrade S., Kahler K., Frech F., Chan K. Methods for evaluation of medication adherence and persistence using automated databases. Pharmacoepidemiol Drug Saf. 2006; 15 (8): 565-574. 13. Rasmussen J., Chong A., Alter D. Relationship between adherence to evidence-based pharmacotherapy and long-term mortality after acutemyocardial infarction. JAMA. 2007; 297 (2): 177-186. 14. Sahlen A., Varenhorst C., Lagerqvist B. et al. Outcomes in patients treated with ticagrelor or clopidogrel after acutemyocardial infarction : experiences from SWEDEHEART registry. Eur Heart J. 2016 року; 37 (44): 3335-3342. 15. Palmerini T., Biondi-Zoccai G., Della Riva D. et al. Stent thrombosis with drug-eluting and bare-metal stents : evidence from a comprehensive network meta-analysis. Lancet. 2012; 379 (9824): 1393-1402. 16. Zocca P., Van der H eijden L., Kok M. et al. Clopidogrel or ticagrelor in acute coronary syndrome patients treated with newer-generation drug-eluting stents : CHANGE DAPT. EuroIntervention. 2017; 13 (10): 1168-1176. 17. Gaubert M., Laine M., Richard T. et al. Effect of ticagrelor-related dyspnea on compliance with therapy in acute coronary syndrome patients. Int J Cardiol. 2014; 173 (1): 120-121. 18. Spertus J., Kettelkamp R., Vance C. et al. Prevalence, predictors, and outcomes of premature discontinuation of thienopyridine therapy after drug-eluting stent placement : results from the PREMIER registry. Circulation. 2006; 113 (24): 2803-2809. 19. Airoldi F., Colombo A., Morici N. et al. Incidence and predictors of drug-eluting stent thrombosis during and after discontinuation of thienopyridine treatment. Circulatio n. 2007; 116 (7): 745-754. Автор огляду: Наталя Генш  Medicine Review 2020; 1 (56): 14 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2024. Усі права захищені.
|
мапа сайту корисні посилання |