Уменьшение риска поражения ЖКТ при антитромбоцитарной терапии. Консенсус ACC/ACG/AHA (2008)Эксперты Американского общества кардиологов (American College of Cardiology, ACC), Американского общества гастроэнтерологов (American College of Gastroenterology, ACG) и Американской ассоциации сердца (American Heart Association, AHA) разработали консенсус по оптимизации длительной терапии антитромбоцитарными средствами в свете проблемы повышенного риска желудочно-кишечных осложнений при лечении этими препаратами [1]. При этом авторы акцентируют внимание на том, что большое количество этих осложнений обусловлены не столько влиянием антиагрегантов, сколько суммированием неблагоприятных побочных эффектов в случае, если антитромбоцитарные препараты принимаются вместе с нестероидными противовоспалительными препаратами (НПВП). Анализируются также и другие факторы, увеличивающие вероятность реализации нежелательных побочных эффектов антитромбоцитарных препаратов. В консенсусе рассматриваются основные особенности применения антитромбоцитарных препаратов в контексте возможных желудочно-кишечных осложнений (прежде всего геморрагического характера), возможности снижения риска развития таких осложнений, показания к отмене этих препаратов из соображений безопасности, а также стратегия профилактики и лечения уже имеющихся желудочно-кишечных побочных эффектов. Актуальность Антитромбоцитарные препараты оказывают благоприятное влияние на выживаемость и настоятельно рекомендуются всеми авторитетными клиническими руководствами для очень многих категорий сердечно-сосудистых больных, в связи с чем являются неотъемлемой составляющей комплексной терапии и профилактики различных заболеваний. К настоящему времени накопилось большое количество убедительных доказательных данных, свидетельствующих о значительных преимуществах антитромбоцитарной терапии у сердечно-сосудистых больных. Регулярный прием антитромбоцитарных средств у пациентов высокого риска уменьшает риск сердечно-сосудистых осложнений на 25% (Antithrombotic Trialists’ Collaboration). Препараты этого класса рекомендуются для первичной и вторичной профилактики кардиоваскулярных событий у самого широкого круга больных, причем как в ургентных ситуациях (при развитии острого коронарного синдрома (ОКС), при необходимости проведения чрескожного коронарного вмешательства (ЧКВ), особенно при стентировании), так и для длительной (пожизненной) терапии [2-8]. В последние годы список показаний к применению антитромбоцитарных средств постоянно растет, увеличивается количество пациентов, принимающих ацетилсалициловую кислоту (АСК) в качестве монотерапии или в комбинации с другими антитромбоцитарными препаратами (как правило, с клопидогрелем), кроме того, недавно американские и европейские эксперты значительно увеличили рекомендуемую длительность двойной антитромбоцитарной терапии АСК и клопидогрелем для пациентов, перенесших стентирование коронарных артерий [3, 5, 6]. Однако для антиагрегантов, как и для любых других лекарственных средств, существуют предостережения относительно возможных побочных эффектов. В частности, одной из наиболее распространенных проблем являются желудочно-кишечные осложнения, которые чаще всего проявляются в виде поражения слизистой оболочки желудочно-кишечного тракта (ЖКТ), нередко и геморрагий (кровотечений, кровоизлияний). При сопутствующей терапии некоторыми другими препаратами (прежде всего, такими как НПВП, кортикостероиды, антикоагулянты) риск таких осложнений существенно возрастает. У некоторых пациентов (например, с уже имеющимся активным поражением ЖКТ или высоким риском желудочно-кишечных кровотечений), к сожалению, приходится отказываться от применения таких препаратов, но в большинстве случаев это нецелесообразно. Однако мы обязаны сделать все возможное, чтобы снизить риск побочных эффектов до минимума. Это предполагает хорошее знание механизмов поражения ЖКТ под воздействием различных препаратов, выбор средств с наилучшим профилем безопасности, использование рациональной схемы терапии и изучение стратегий специфической медикаментозной протекции. На решение этой задачи и направлен консенсус ACC/ACG/AHA (2008) [1]. Учитывая огромную распространенность применения антитромбоцитарных средств (прежде всего АСК) во всем мире, эксперты считают необходимым повышать грамотность врачей в отношении наиболее вероятных побочных эффектов такого лечения. Особый акцент при этом следует сделать на ситуации, когда пациент принимает и антитромбоцитарные препараты (для профилактики сердечно-сосудистой патологии), и НПВП (для лечения хронических воспалительных заболеваний, прежде всего опорно-двигательного аппарата). Такая клиническая ситуация встречается в практике врача очень часто, особенно у пациентов пожилого возраста. Эксперты ACC/ACG/AHA оценивают АСК и НПВП как наиболее используемые в США медицинские препараты (как по назначениям врачей, так и с оглядкой на неучтенный пул пациентов, занимающихся самолечением), особенно среди лиц пожилого возраста [1]. Еще в 1995 г. в исследовании N.J. Talley et al. было показано, что в популяции людей 65 лет и старше около 70% регулярно принимают НПВП как минимум еженедельно, а 34% – ежедневно; в том же исследовании АСК как минимум еженедельно принимали 60% всех лиц этого возраста. К тому же за прошедшие с того времени почти полтора десятка лет потребление АСК во всем мире значительно выросло, кроме того, появились и все более активно назначаются и другие антитромбоцитарные препараты (прежде всего, клопидогрель). Следует полагать, что в других странах, в том числе и в Украине, ситуация примерно такая же. К сожалению, кардиологи не всегда принимают во внимание наличие у пациентов хронических заболеваний суставов и, соответственно, тот факт, что параллельно с препаратами кардиологической группы такие пациенты зачастую на протяжении многих лет принимают и НПВП. В связи с этим консенсус ACC/ACG/AHA (2008) [1] преследует цель повысить настороженность врачей в отношении ассоциированных рисков желудочно-кишечных осложнений у больных, принимающих и антиагреганты, и НПВП. Использование даже низких (кардиопротективных, то есть 75-325 мг/сут) доз АСК ассоциируется с повышением риска желудочно-кишечных поражений в 2-4 раза (J. Weil et al., 1995; N.D. Yeomans et al., 2005). Однако этот риск является относительно небольшой платой за те значительные клинические преимущества, которые АСК обеспечивает в отношении профилактики ишемических, тромботических, тромбоэмболических событий и улучшения выживаемости кардиологических больных. Гораздо более опасным является случай сочетанного применения АСК с НПВП. Поражение верхних отделов ЖКТ отмечается примерно у 1 из 20 всех пациентов, принимающих НПВП, и у 1 из 7 пожилых больных (C. Bombardier et al., 2000). К таким осложнениям относятся диспепсия (боль и дискомфорт в области желудка), усугубление симптоматики гастроэзофагеального рефлюкса, пептические язвы слизистой оболочки (бессимптомные или симптомные, в том числе осложненные кровотечением или перфорацией). Ежегодно у больных, принимающих НПВП, регистрируется от 2 до 4,5% желудочно-кишечных осложнений, при этом риск серьезных осложнений (таких как кровотечения, перфорации язв или обструкции кишечника) достигает 0,2-1,9% (C. Bombardier et al., 2000; J.J. Ofman et al., 2002). Различные обсервационные исследования указывают на то, что одновременное применение НПВП и низких доз АСК дополнительно увеличивает риск желудочно-кишечных поражений. Чем старше пациент, тем этот риск выше: в исследовании N.S. Abraham et al. (2008) такая комбинация у пожилых больных обусловливала возрастание риска желудочно-кишечных поражений в 3,8-5,6 раз по сравнению с монотерапией АСК. Установлено, что при комбинировании НПВП и АСК ежегодный риск побочных эффектов со стороны верхних отделов ЖКТ достигает 5,6%, причем использование ЦОГ-2-селективных НПВП в данном случае не обеспечивает дополнительной гастропротекции и в комбинации с АСК оказывает такое же неблагоприятное действие на ЖКТ, что и неселективные НПВП (A. Lanas et al., 2000; C.J. Hawkey et al., 2007). Вместе с тем различные авторы подтверждают, что в последние годы отмечается снижение количества госпитализаций по поводу желудочно-кишечных побочных эффектов НПВП-терапии. Это объясняется несколькими факторами: использованием более низких доз НПВП, внедрением в практику ЦОГ-2-селективных НПВП, применением гастропротективной терапии ингибиторами протонной помпы (ИПП). Следовательно, риск поражений ЖКТ может быть снижен при соблюдении ряда предосторожностей. Ниже тезисно представлены основные рекомендации ACC/ACG/AHA по профилактике и лечению этих осложнений; комментарии экспертов к этим рекомендациям также вкратце изложены далее. Практические рекомендации по профилактике и лечению желудочно-кишечных осложнений, связанных с применением антитромбоцитарной терапии, согласно консенсусу ACC/ACG/AHA (2008) [1] 1. Использование любых НПВП, в том числе ЦОГ-2-селективных, в комбинации с кардиопротективными дозами АСК повышает риск желудочно-кишечных осложнений и требует назначения гастропротективной терапии. 2. Применение даже низких (кардиопротективных) доз АСК ассоциировано с повышением риска желудочно-кишечных осложнений в 2-4 раза. Эти побочные эффекты дозозависимы, поэтому в рутинной практике для длительной или постоянной терапии с целью профилактики сердечно-сосудистых осложнений не рекомендуется назначать дозы свыше 81 мг/сут. Для пациентов с повышенным риском поражения ЖКТ необходимо использовать гастропротективную терапию. 3. Комбинирование АСК и/или клопидогреля с антикоагулянтами (нефракционированным гепарином, низкомолекулярными гепаринами, варфарином) ассоциировано со значительным увеличением риска геморрагических осложнений, значительная доля которых относится к кровотечениям из верхних отделов ЖКТ. Поэтому такие комбинации могут использоваться только при строгих показаниях и должны сопровождаться назначением ИПП. Если варфарин используется в комбинации с двойной антитромбоцитарной терапией (АСК + клопидогрель), следует удерживать международное нормализованное отношение в рамках 2,0-2,5. 4. В целях снижения риска рецидива язвенного кровотечения не рекомендуется заменять АСК на клопидогрель; в этом случае более предпочтительной стратегией является комбинирование АСК и ИПП. 5. ИПП являются предпочтительными лекарственными средствами для лечения и профилактики НПВП- и АСК-ассоциированных желудочно-кишечных осложнений. 6. Перед началом длительной антитромбоцитарной терапии у пациентов с пептической язвой в анамнезе рекомендовано обследование с целью выявления инфекции H. pylori; в случае ее наличия показана эрадикация. 7. В случае развития язвенных кровотечений на фоне антитромбоцитарной терапии решение о целесообразности отмены препаратов необходимо принимать в индивидуальном порядке, взвесив соотношение между рисками геморрагических осложнений терапии и тромботических/тромбоэмболических событий, обусловленных ее прекращением. 8. У пациентов высокого кардиоваскулярного риска, получающих двойную антитромбоцитарную терапию, могут использоваться эндоскопические методы обследования и лечения. Для оптимального решения насущных вопросов по особенностям ведения такого пациента необходимо тесное сотрудничество кардиолога и врача-эндоскописта. Основные механизмы поражения ЖКТ
НПВП Неблагоприятное влияние НПВП на состояние ЖКТ обусловлено как локальным повреждением слизистой оболочки, так и системным воздействием на синтез простагландинов. Тканевые простагландины синтезируются из арахидоновой кислоты двумя путями – с помощью циклооксигеназы-1 (ЦОГ-1) и циклооксигеназы-2 (ЦОГ-2). Путь, опосредованный ЦОГ-1, является основным в нормальных здоровых тканях и обеспечивает выработку простагландинов, которые отвечают за различные благоприятные физиологические эффекты – цитопротекцию в ЖКТ, нормальную перфузию почек, активность тромбоцитов и т.д. В частности, в ЖКТ стимулируется синтез и секреция слизи и бикарбоната натрия, пролиферация эндотелия желудка и кишечника. Таким образом, ЦОГ-1 играет роль фермента, участвующего в обеспечении нормальной (физиологической) функциональной активности клеток. Напротив, посредством ЦОГ-2, который активируется преимущественно в пораженных (воспаленных) тканях, образуются простагландины, способствующие усилению явлений воспаления (болезненность, отек, местное повышение температуры тканей). Противовоспалительное, обезболивающее, жаропонижающее действие НПВП обусловлено ингибированием второй изоформы ЦОГ, однако большинство НПВП не являются ЦОГ-2-селективными и в той или иной степени угнетают также ЦОГ-1. Это становится причиной развития неблагоприятных эффектов, прежде всего повышения уязвимости слизистой оболочки ЖКТ, возрастания риска ее эрозирования и изъязвления под воздействием эндогенных факторов (желудочных и кишечных ферментов, соляной кислоты, желчи), что в связи с параллельным поражением функции тромбоцитов чревато также повышением вероятности геморрагических осложнений – кровоизлияний в стенки ЖКТ, язвенных кровотечений. В результате, среди наиболее распространенных осложнений приема НПВП находятся пептические язвы желудка и кровотечения из верхних отделов ЖКТ. Тем не менее в экспериментах на животных было установлено, что для того чтобы развились ЦОГ-ассоциированные желудочно-кишечные осложнения, необходимо ингибирование обеих изоформ ЦОГ (J.L. Wallace et al., 2000). Ингибирование ни ЦОГ-1, ни ЦОГ-2 в отдельности не вызывает таких побочных эффектов. Поэтому ни использование низких (кардиопротективных, но не агрессивных для ЖКТ, то есть ниже 325 мг/сут) доз АСК, ни прием ЦОГ-2-селективных НПВП (коксибов) не решает эту проблему, если эти препараты используются одновременно. Суммирование эффектов ЦОГ-2-селективных НПВП и АСК, которая действует преимущественно на ЦОГ-1, приводит к повышению риска поражения ЖКТ, что сравнимо с неблагоприятным воздействием на ЖКТ традиционных НПВП. Эта особенность остается недооцененной практическими врачами, подчеркивают эксперты ACC/ACG/AHA [1], а между тем в исследовании E.R. Cox et al. (2004) было показано, что не менее половины всех пациентов, принимающих в качестве НПВП только коксибы, также получают АСК.
Тиенопиридины Клопидогрель и другие тиенопиридины не влияют на слизистую ЖКТ непосредственно, однако воздействуют на агрегацию тромбоцитов, а это, в свою очередь, имеет большое значение для высвобождения различных тромбоцитарных факторов роста, участвующих в ангиогенезе. Нормальный ангиогенез является одним из ключевых механизмов, обеспечивающих заживление повреждений слизистой оболочки ЖКТ, поэтому как тромбоцитопения, так и угнетение функции тромбоцитов ухудшают репарационные способности ЖКТ. Таким образом, хотя клопидогрель и другие тиенопиридины не агрессивны по отношению к ЖКТ, они способствуют повышению его уязвимости к повреждениям, развивающимся под действием других лекарственных средств, собственных эндогенных факторов или инфекции H. pylori. Профилактика и лечение желудочно-кишечных осложнений при длительном приеме антитромбоцитарных препаратов и НПВП К основным мероприятиям профилактики таких осложнений следует отнести использование по возможности низких дозировок антитромбоцитарных средств и НПВП, осторожное комбинирование различных препаратов этих групп, особенно на фоне антикоагулянтной терапии, применение ИПП и методов эрадикации H. pylori. С точки зрения проблемы безопасности терапии снижение дозы АСК до минимально активных (75-81 мг/сут) является простым и эффективным способом снижения риска побочных осложнений. На сегодняшний день оптимальная дозировка АСК не определена, поскольку различные исследования не продемонстрировали четких преимуществ какой-то конкретной дозы. Существуют только отдельные данные о предпочтительности использования нагрузочных доз АСК в острых ситуациях (при ОКС, в случае ЧКВ). Однако для длительной антитромбоцитарной терапии используются различные дозировки в рамках кардиопротективного спектра (от 75 до 325 мг/сут). Вместе с тем известно, что побочные эффекты АСК являются дозозависимыми. Увеличение дозы даже в пределах 75-325 мг/сут способствует возрастанию риска осложнений, но не увеличивает эффективность профилактического действия АСК в отношении сердечно-сосудистой заболеваемости и смертности (H.T. Sorensen et al., 2000; CURE, 2003). И хотя доказательные данные по этому поводу несколько противоречивы, эксперты ACC/ACG/AHA полагают, что имеет смысл по умолчанию придерживаться максимально низких дозировок АСК (не более 81 мг/сут), если нет особых показаний к увеличению дозы препарата (при ОКС, ЧКВ и т.д.). Особенно актуально это для пациентов с высоким риском поражения ЖКТ. В настоящее время проводится исследование CURRENT/OASIS-7 (Clopidogrel Optimal Loading Dose Usage to Reduce Recurrent EveNTs/Optimal Antiplatelet Strategy for InterventionS-7), в котором сравниваются преимущества и неблагоприятные эффекты низких (75-100 мг/сут) и высоких (300-325 мг/сут) доз АСК; результаты этого исследования помогут более определенно судить о целесообразности снижения дозировок АСК из соображений безопасности. Особых предосторожностей требует одновременный прием антитромбоцитарных средств (АСК, клопидогреля) с НПВП или с антикоагулянтными препаратами. В первом случае (в комбинации с НПВП) увеличивается риск поражения слизистой оболочки ЖКТ, часть из которых может проявляться в виде кровотечений; во втором случае (в комбинации с антикоагулянтами) – прежде всего резко возрастает общий риск геморрагических осложнений, в том числе желудочно-кишечных. Таким образом, обе клинические ситуации неблагоприятны с точки зрения повышения риска кровотечений из верхних отделов ЖКТ, что убедительно подтверждают многочисленные клинические исследования. В то же время в ряде ситуаций сложно избежать такого комбинирования препаратов, по крайней мере, на протяжении нескольких недель (месяцев); для таких пациентов необходимо тщательно взвесить все преимущества и риски и всеми доступными способами минимизировать вероятность развития побочных эффектов. Эксперты ACC/ACG/AHA предостерегают от использования стратегии замены АСК на тиенопиридин (например, на клопидогрель) из соображений безопасности. В исследовании CAPRIE антитромбоцитарная терапия клопидогрелем в дозе 75 мг/сут обусловливала несколько меньшую частоту развития серьезных желудочно-кишечных кровотечений, чем АСК (0,52 vs 0,72%; p<0,05), как и более низкую вероятность госпитализаций по поводу этих осложнений (0,7 vs 1,1%; p=0,012). Однако следует отметить, что различия были небольшими, а сравнение проводилось с максимальными кардиопротективными дозами АСК – 325 мг/сут. Учитывая то, что побочные эффекты АСК дозозависимы, следует полагать, что применение АСК в низких дозах (75-81 мг/сут) не должно по своей безопасности существенно отличаться от применения клопидогреля. И хотя результаты этого исследования стали основанием для того, чтобы эксперты ACC/AHA ранее рекомендовали использование клопидогреля в том случае, если АСК обусловливает желудочно-кишечные кровотечения [2, 3, 6], в новом консенсусе ACC/ACG/AHA [1] отмечено, что такая стратегия нерациональна. Авторы консенсуса учли результаты не только CAPRIE, но и исследования A. Lanas et al. (2006), в котором было показано, что тиенопиридины (клопидогрель и тиклопидин) в стандартных дозах обусловливают такой же риск серьезных кровотечений из верхних отделов ЖКТ, что и АСК в дозе 100 мг/сут. Более целесообразным для профилактики или лечения АСК-обусловленных поражений ЖКТ является присоединение к терапии АСК гастропротективных средств – ИПП. Такой вывод был сделан в связи с результатами проспективного рандомизированного двойного слепого исследования F.K. Chan et al. (2005), в котором у пациентов, перенесших АСК-обусловленные желудочно-кишечные поражения, сравнивались две стратегии дальнейшей антитромбоцитарной терапии – назначение клопидогреля и применение комбинации АСК и эзомепразола. Оказалось, что в группе клопидогреля за 12 месяцев наблюдения произошло гораздо больше случаев рецидивов желудочно-кишечных осложнений по сравнению со стратегией комбинирования АСК и ИПП (8,6 vs 0,7%). Похожие результаты продемонстрировало также исследование аналогичного дизайна и с теми же препаратами, выполненное K.C. Lai et al. (2006), – 13,6% случаев рецидивов осложнений со стороны ЖКТ в группе клопидогреля и 0% в группе АСК + эзомепразол. В связи с результатами этих и ряда других исследований ИПП признаны предпочтительными лекарственными средствами, показанными для профилактики и лечения НПВПи АСК-ассоциированных поражений ЖКТ. Кроме того, большое значение также имеет своевременная диагностика и лечение инфекции H. pylori. Авторы консенсуса рекомендуют использовать следующий алгоритм гастропротекции при длительной антитромбоцитарной терапии.
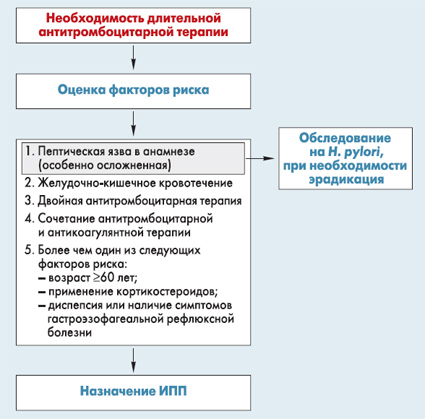
Не рекомендуется для профилактики и лечения желудочно-кишечных осложнений антитромбоцитарной терапии использовать такие препараты, как синтетические простагландины (мизопростол), алюминийсодержащие антациды (сукральфат), антагонисты Н2-рецепторов. Мизопростол в различных исследованиях эффективно устранял поражения ЖКТ, обусловленные ульцерогенным действием АСК, однако вызывал ряд собственных побочных эффектов, особенно диарею. В исследовании F.E. Silverstein et al. (1995) препарат только из-за диареи пришлось отменить в течение первого же месяца использования у 20% пациентов. Сукральфат достаточно эффективен для профилактики и лечения язв двенадцатиперстной кишки, обусловленных приемом НПВП, однако не влияет на язвы желудка. В большинстве случаев не воздействуют на язвы желудка и антагонисты Н2-рецепторов. Поэтому наиболее эффективными, безопасными и удобными в рутинной клинической практике средствами для лечения и профилактики АСК- и НПВП-обусловленных желудочно-кишечных осложнений в настоящее время признаны ИПП. Эффективность различных препаратов этой группы (ланзопразола, омепразола, эзомепразола и др.) для данной категории пациентов подтверждают различные клинические исследования (F.K. Chan et al., 2005; K.C. Lai et al., 2006; A. Lanas et al., 2007; M.W. Chin et al., 2007; J.S. Berger et al., 2008, и др.). Наконец, важным фактором, способствующим поражению верхних отделов ЖКТ вследствие повышения уязвимости слизистой оболочки, является инфекция H. pylori. В исследовании A. Lanas et al. (2002) было показано, что инфекция H. pylori является независимым фактором риска для развития кровотечений верхних отделов ЖКТ у пациентов, принимающих низкие дозы АСК. Похожие данные были получены и другими авторами (W.A. Stack et al., 2002; N.D. Yeomans et al., 2005). В связи с этим даже у пациентов, которым назначены низкие дозы АСК, следует провести обследование на наличие H. pylori, если в анамнезе у таких больных имеются язвенные поражения, в том числе неосложненные и успешно пролеченные. Если инфекция H. pylori подтверждена, рекомендована эрадикация возбудителя, хотя доказательные данные по поводу того, уменьшает ли эта стратегия риск АСК-индуцированных поражений ЖКТ, на сегодняшний день противоречивы. Поэтому, даже если эрадикация успешна, таким пациентам все равно показан профилактический прием ИПП – это достоверно уменьшает риск желудочно-кишечных кровотечений на фоне приема АСК. Кроме того, для лечения геморрагических осложнений из верхних отделов ЖКТ могут использоваться эндоскопические методы остановки кровотечения, такие как наложение клипс (но не термокоагуляция). К вопросу об отмене антитромбоцитарной терапии Еще одним важным аспектом проблемы желудочно-кишечных осложнений антитромбоцитарной терапии является решение вопроса об отмене препаратов из-за побочных эффектов. В настоящее время практические врачи охотно отменяют АСК и другие антитромбоцитарные средства при развитии лекарственно-индуцированного поражения ЖКТ, особенно в случае появления острых пептических язв и кровотечений из верхних отделов ЖКТ. Эксперты ACC/ACG/AHA считают, что в большинстве таких ситуаций отказ от антитромбоцитарной терапии нецелесообразен. Учитывая значительные клинические преимущества антитромбоцитарных препаратов для профилактики сердечно-сосудистых событий и прогноза пациентов, не стоит сразу же отказываться от этого лечения у всех больных с признаками неблагоприятного влияния на ЖКТ, даже при развившемся остром язвенном кровотечении. Следует брать во внимание то, что гемодинамические и гемокоагуляционные изменения, последовательно развивающиеся во время кровотечения и сразу после его остановки, способствуют тромбозам и тромбоэмболиям. Поэтому если поспешно отменить антитромбоцитарную терапию на фоне развившегося кровотечения, риск тромботических осложнений сразу же значительно возрастает. При появлении признаков поражения ЖКТ на фоне приема антиагрегантов необходимо тщательно взвесить все преимущества и риски для конкретного пациента, максимально оптимизировать терапию (снизить дозу АСК, по возможности отказаться от сопутствующей терапии НПВП, обследовать пациента на предмет наличия инфекции H. pylori и выполнить эрадикацию, если это необходимо, а также назначить ИПП). В качестве альтернативы можно также попробовать заменить АСК на клопидогрель, хотя эта стратегия и не доказала своих преимуществ у пациентов с острым АСК-обусловленным кровотечением. Наряду с этим метаанализ рандомизированных исследований S. Dorward et al. (2006) убедительно продемонстрировал, что внутривенное назначение ИПП сразу после эндоскопического гемостаза в связис АСК-индуцированным язвенным кровотечением достоверно снижает риск повторного кровотечения и потребности в хирургическом вмешательстве. Однако, к сожалению, пока нет убедительных доказательных данных, подтверждающих возможность применения АСК на фоне поддержки ИПП в случае острого кровотечения, в связи с чем рекомендации пока что основываются преимущественно на консенсусе экспертов. Экспериментальные исследования указывают на то, что эффективность гемостаза зависит от двух основных факторов – кислотности содержимого желудка или кишечника и стабильности новообразованного тромба. И если ИПП успешно обеспечивают оптимальный уровень рН, то назначение АСК может нарушить стабильность тромба и тем самым значительно снизить или нивелировать благоприятное влияние ИПП на гемостаз. На сегодняшний день только одно небольшое рандомизированное исследование подтвердило безопасность раннего возобновления приема АСК в такой ситуации (J. Sung et al., 2008): хотя в группе АСК было больше рецидивов кровотечений по сравнению с плацебо (18,9 vs 10,9%, p=0,25), на фоне приема АСК умер 1 пациент (1,7%; причина смерти – кардиоваскулярное событие), в то время как в группе плацебо – 8 пациентов (14,5%; причины смерти – кардиоваскулярные события у 5, рецидив кровотечения у 2, пневмония у 1), p=0,01. Учитывая результаты этого исследования, авторы консенсуса [1], хотя пока не могут однозначно рекомендовать ту или иную стратегию, все же советуют проанализировать индивидуальные риски не только повторных кровотечений, но и сердечно-сосудистых событий, прежде чем принимать решение об отмене и возобновлении антитромбоцитарной терапии. Не менее сложным является и вопрос о возможности продолжать антитромбоцитарную терапию (особенно двойную) в случае, если пациенту показаны какие-либо методы обследования или лечения с помощью эндоскопии ЖКТ (колоноскопия, полипэктомия и т.п.). Большинство врачей в настоящее время предпочитают отменять антитромбоцитарную терапию на несколько дней, чтобы избежать геморрагических осложнений. Однако в консенсусе ACC/ACG/AHA [1] подчеркивается, что доказательные данные указывают на необходимость отдавать предпочтение эффективной и непрерывной профилактике ишемических событий даже в такой ситуации. Причем эта рекомендация была сделана американскими гастроэнтерологами еще в 2002 г. и прописана в руководстве Американского общества по эндоскопическим методам обследования и лечения ЖКТ (American Society of Gastrointestinal Endoscopy) [9]. Тем не менее существует насущная необходимость еще раз напомнить об этом практическим врачам, поэтому в консенсусе ACC/ACG/AHA [1] этому вопросу уделяется особое внимание. Чтобы правильно оценить и сердечно-сосудистые риски, и риск геморрагических осложнений, эндоскопист и кардиолог должны тесно сотрудничать, принимая решение о целесообразности отмены антиагрегантной терапии или возможности ее продолжения во время эндоскопического вмешательства. Так, если пациент недавно перенес ОКС, особенно в случае ЧКВ со стентированием коронарной артерии, двойная антитромбоцитарная терапия показана в абсолютном большинстве случаев даже при эндоскопических вмешательствах. Заключение Таким образом, в консенсусе ACC/ACG/AHA [1] приводятся основные подходы к профилактике и лечению геморрагических осложнений со стороны верхних отделов ЖКТ на фоне длительной (постоянной) антитромбоцитарной терапии. Несмотря на распространенность и сложность этой проблемы, авторы документа неоднократно подчеркивают огромную важность антитромбоцитарной терапии для предупреждения ишемических событий и улучшения выживаемости больных. Взвешивая преимущества и риски, всегда необходимо помнить о приоритетности этой точки зрения. Поэтому даже при развитии каких-либо осложнений со стороны ЖКТ, в том числе геморрагического характера, более рационально не отказываться от антиагрегантов вообще, а тщательно проанализировать все возможные факторы, которые могут увеличивать риск побочных эффектов, и по возможности избавиться прежде всего от них (например, сопутствующий прием НПВП, кортикостероидов, антикоагулянтов, инфекция H. pylori). Кроме того, в профилактике и лечении АСК- и НПВП-индуцированных осложнений со стороны ЖКТ большую роль играют ИПП как основной инструмент современной гастропротекции. Для оптимального решения всех сложных вопросов, возникающих в этом контексте, необходимо сотрудничество различных специалистов – кардиологов, гастроэнтерологов, эндоскопистов, терапевтов (семейных врачей). Литература: 1. Bhatt D.L., Scheiman J., Abraham N.S. et al. ACCF/ACG/AHA 2008 expert consensus document on reducing the gastrointestinal risks of antiplatelet therapy and NSAID use: a report of the American College of Cardiology Foundation Task Force on Clinical Expert Consensus Documents. Circulation 2008; 118: 1894-1909; J Am Coll Cardiol 2008; 52: 1502-17. 2. Anderson J.L., Adams C.D., Antman E.M. et al. ACC/AHA 2007 guidelines for the management of patients with unstable angina/no-ST-elevation myocardial infarction: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Revise the 2002 Guidelines for the Management of Patients With Unstable Angina/Non-ST-Elevation Myocardial Infarction). J Am Coll Cardiol 2007; 50: e1-e157. 3. Antman E.M., Hand M., Armstrong P.W. et al. 2007 Focused Update of the ACC/AHA guidelines for the management of patients with ST-elevation myocardial infarction: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines: Developed in Collaboration With the Canadian Cardiovascular Society Endorsed by the American Academy of Family Physicians: 2007 Writing Group to Review New Evidence and Update the ACC/AHA 2004 Guidelines for the Management of Patients With ST-Elevation Myocardial Infarction, Writing the Management of Patients With ST-Elevation Myocardial Infarction, Writing on Behalf of the 2004 Writing Committee. Circulation 2008; 117; 296-329. 4. Bassand J.P., Hamm C.W., Ardissino D. et al.; Task Force for Diagnosis and Treatment of Non-ST-Segment Elevation Acute. Guidelines for the diagnosis and treatment of non-ST-segment elevation acute coronary syndromes. The Task Force for the Diagnosis and Treatment of Non-ST-Segment Elevation Acute Coronary Syndromes of the European Society of Cardiology. Eur Heart J 2007; 28 (13): 1598-660. 5. Van de Werf F., Bax J., Betriu A. et al. Management of acute myocardial infarction in patients presenting with persistent ST-segment elevation: The Task Force on the management of ST-segment elevation acute myocardial infarction of the European Society of Cardiology. Eur Heart J 2008; 29: 2909-2945. 6. King III S.B., Smith Jr. S.C., Hirshfeld Jr. J.W. et al. 2007 Focused Update of the ACC/AHA/SCAI 2005 Guideline Update for Percutaneous Coronary Intervention. A Report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. Circulation 2008; 117: 261-295. 7. American Diabetes Association: Standards of medical care in diabetes – 2008. Diabetes Care 2008; 31 (Suppl. 1): S12-S54. 8. Ryden L., Standl E., Bartnik M. et al. Guidelines on diabetes, pre-diabetes, and cardiovascular diseases: executive summary. The Task Force on Diabetes and Cardiovascular Diseases of the European Society of Cardiology (ESC) and of the European Association for the Study of Diabetes (EASD). Eur Heart J 2007; 28: 88-136. 9. Eisen G.M., Baron T.H., Dominitz J.A. et al. Guideline on the management of anticoagulation and antiplatelet therapy for endoscopic procedures. Gastrointest Endosc 2002; 55: 775-9. Автор обзора Анна Карташева Medicine Review 2009; 1 (06): 18-24 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2026. Усі права захищені.
|
мапа сайту корисні посилання |