Диагностика и лечение резистентной артериальной гипертензии. Новое научное соглашение AHA (2008)Весной 2008 г. в журнале Hypertension было опубликовано научное соглашение Американской ассоциации сердца (American Heart Association, AHA), касающееся вопросов диагностики, оценки, лечения такого сложного заболевания, как резистентная артериальная гипертензия (АГ) [1]. В опубликованном соглашении эксперты AHA обращают внимание на ключевые проблемы ведения больных с резистентной АГ – диагностику этой патологии и подходы к ее лечению. В диагностике особенно важным является определить причину резистентной гипертензии (а точнее – совокупность причин, поскольку в большинстве случаев резистентная АГ имеет полиэтиологическую природу), а также отдифференцировать ее от так называемой псевдорезистентности. В документе указывается на основные моменты, которые необходимо учитывать при этом. Точная диагностика помогает разработать успешные стратегии лечения. К сожалению, доказательные данные о резистентной АГ ограничены, поскольку эту категорию пациентов обычно не рассматривают в качестве самостоятельной подгруппы в клинических исследованиях. Кроме того, даже в специально организованных исследованиях очень сложно оценить эффективность трех, четырех и большего количества препаратов, назначаемых одновременно, а именно комбинированная терапия лежит в основе преодоления резистентности контроля артериального давления (АД). В связи с этим большинство доказательных данных, рассматривающихся в контексте резистентной АГ, на самом деле относятся к АГ вообще и плохо контролируемой АГ (по различным критериям) в частности, а рекомендации по лечению резистентной АГ в настоящее время носят в основном эмпирический характер. В представленном документе AHA [1] суммированы имеющиеся в настоящее время доказательные данные по этой проблеме, однако наиболее приемлемые стратегии ведения больных определены исходя преимущественно из консенсуса экспертов, признают авторы соглашения. Определение Как уже было сказано, клинических исследований, посвященных собственно резистентной АГ, очень мало, а извлечь из более широких исследований информацию о подгруппе больных с резистентной АГ в настоящее время непросто, учитывая то, что разные авторы по-разному трактуют понятия резистентности к лечению и не разграничивают причины плохого контроля АД. Поэтому очень важно прийти к общему соглашению относительно того, что следует подразумевать под резистентной АГ и какими основными признаками она должна обладать. В научном соглашении AHA [1] за основу определения резистентной АГ взята дефиниция 7-го доклада Национального комитета США по профилактике, выявлению, оценке и лечению АГ (Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure, JNC-7, 2003) [3]. Согласно этому определению резистентной АГ следует считать АД, которое остается выше целевого уровня на фоне применения не менее 3 антигипертензивных препаратов различных классов (в идеале все эти препараты должны использоваться в оптимальных дозах и один из них должен относиться к диуретикам). Даже если АД удается контролировать, но лишь с помощью 4 и более антигипертензивных препаратов, такая гипертензия все равно считается резистентной. Следует понимать, что понятие «резистентная АГ» не является синонимом к термину «неконтролируемая АГ». В ряде случаев неконтролируемую АГ можно определить как «псевдорезистентность», к которой относятся случаи низкой приверженности больных к лечению (ведущая причина плохого контроля АД), неправильного измерения АД, «гипертензии белого халата». На последнюю проблему авторы документа обращают особое внимание, указывая, что приблизительно одна пятая часть всех случаев АД, превышающего целевой уровень и расценивающегося как резистентная АГ, является «гипертензией белого халата» (M.A. Brown et al., 2001; R.C. Hermida et al., 2005). Дополнительные сложности привносит и плохой комплайенс, который свойственен очень многим больным АГ. Так, ретроспективный анализ G. Massaglia и соавт. (2005) показал, что приблизительно 40% пациентов с впервые диагностированной АГ самовольно прекращают принимать антигипертензивные препараты на протяжении первого же года с момента назначения лечения. Актуальность проблемы Авторы соглашения подчеркивают, что резистентная АГ – распространенная клиническая проблема, с которой приходится сталкиваться как врачам общей практики, так и различным специалистам (кардиологам, эндокринологам, хирургам). Вне зависимости от причин, обусловливающих резистентность гипертензии к лечению, наличие неконтролируемой АГ резко увеличивает кардиоваскулярный риск, способствует раннему и значительному поражению органов/тканей-мишеней. Точная заболеваемость резистентной АГ неизвестна, однако данные клинических исследований указывают на ее достаточно высокую распространенность (по различным сведениям – от 20 до 30% лиц с АГ [1]). В этом отношении интересными представляются данные исследования ALLHAT (2002), которое можно считать одним из наиболее релевантных, поскольку оно включило большое количество участников (более 33 тыс.) разного пола и различных рас, а продолжительность наблюдения в этом исследовании составила 5 лет. К концу исследования оказалось, что более чем половине участников требовалось 3 и более антигипертензивных средств для контроля АГ (только 49% успешно лечились 1 или 2 препаратами). При этом следует учитывать, что популяция пациентов исследования ALLHAT не соответствовала общей популяции таких больных в обществе, поскольку одним из критериев исключения из исследования было наличие в анамнезе АГ, сложно поддающейся лечению (требующей более 2 антигипертензивных препаратов для достижения АД <160/100 мм рт. ст.), то есть в ALLHAT не вошли многие пациенты с заведомо резистентной АГ. Это обозначает, что в реальной клинической практике следует ожидать еще большего количества лиц с плохо контролируемым АД, чем показали результаты ALLHAT. Особенно высок риск резистентной АГ у лиц с такими факторами риска, как пожилой возраст и ожирение. Авторы документа подчеркивают: «пожилой возраст и ожирение являются двумя наиболее существенными факторами риска, ассоциированными с резистентной АГ» [1]. В связи с глобальным постарением населения во всем мире и высокими темпами распространенности ожирения заболеваемость резистентной АГ постоянно возрастает, что диктует необходимость усиления внимания к этой проблеме. Наличие других факторов риска и сопутствующих заболеваний (сахарного диабета (СД), поражения почек, атеросклероза сосудов и др.) дополнительно увеличивает риск устойчивости гипертензии к лечению стандартными методами. По данным Фремингемского исследования (D.M. Lloyd-Jones et al., 2000) пожилой возраст был самым сильным предиктором плохого контроля АД: количество участников в возрасте старше 75 лет с поддающейся контролю АГ было в четыре раза меньше, чем таких участников в возрасте 60 лет и моложе. По данным тех же авторов от 2002 г. еще одним значительным предиктором устойчивости АГ к лечению следует считать избыточный вес: количество пациентов с индексом массы тела (ИМТ) >30 кг/м² с хорошо контролируемым АД было на треть меньше, чем таких же участников исследования с ИМТ <25 кг/м². В исследовании ALLHAT наиболее значимыми предикторами плохого контроля АГ (под которым подразумевалась необходимость в назначении 2 и более антигипертензивных препаратов) были определены пожилой возраст, высокое исходное АД, гипертрофия левого желудочка и ожирение, однако сильнее всего с резистентной АГ в рамках этого исследования было ассоциировано хроническое заболевание почек (сывороточный креатинин ≥ 1,5 мг/дл). Кроме того, плохому контролю АГ способствовали наличие СД, принадлежность к негроидной расе, женскому полу; хуже всего в ALLHAT АД контролировалось у женщин-афроамериканок (59%), лучше всего – у белых мужчин (70%). Прогноз пациентов с резистентной АГ до сих пор не оценивался, однако следует полагать, что он сравним с прогнозом лиц с длительно существующей плохо контролируемой АГ и ассоциирован с такими факторами кардиоваскулярного риска, как СД, хроническая болезнь почек, гипертрофия левого желудочка, обструктивное ночное апноэ). Для более точной оценки распространенности резистентной АГ и ее влияния на кардиоваскулярную заболеваемость и смертность необходимы специально спланированные крупные исследования. Диагностика При диагностике резистентной АГ необходимо прежде всего исключить так называемую псевдорезистентность. Чрезвычайно важно уточнять диагноз с помощью амбулаторного мониторирования АД, чтобы исключить «гипертензию белого халата», а также изучить вопрос приверженности пациента к лечению. Нельзя забывать и о таких простых вещах, как правильная техника измерения АД: некорректные результаты обследования пациента нередко создают ложное впечатление о плохом контроле АД и не дают возможности оценить эффективность лечения должным образом. Чаще всего к неправильной (обычно завышенной) оценке уровня АД ведут две распространенные ошибки: измерение АД сразу же после того, как пациент сел, не выдержав несколько минут для отдыха, без повторных измерений на обеих руках, а также использование слишком маленькой для данного пациента манжеты (по правилам воздушная муфта манжеты должна охватывать не менее 80% окружности плеча). Обязательной составляющей диагностики резистентной АГ, как и любых вариантов АГ, является выявление и документация повреждений органов/тканей-мишеней (ретинопатия, хроническое заболевание почек, гипертрофия левого желудочка и др.). Кроме того, диагностический алгоритм в случае резистентной АГ должен включать поиск причин вторичного повышения АД или недостаточного ответа на антигипертензивные препараты. К частым причинам такого рода относятся обструктивное ночное апноэ, паренхиматозные заболевания почек, стеноз почечных артерий, первичный альдостеронизм; к более редким – феохромоцитома, болезнь или синдром Кушинга, гиперпаратиреоидизм, коарктация аорты, опухоль головного мозга. Хотелось бы обратить особое внимание практических врачей на такие проблемы, как первичный альдостеронизм и обструктивное ночное апноэ. Эти нарушения и их роль в кардиоваскулярной заболеваемости и смертности, как правило, сильно недооцениваются, а между тем они имеют большое значение, в частности в структуре резистентной АГ. Так, авторы соглашения [1] считают, что может оказаться полезным внедрение такого подхода, как скрининг на первичный альдостеронизм. Есть основания полагать, что распространенность этой патологии гораздо выше, чем кажется, и что именно первичный альдостеронизм обусловливает значительную часть случаев резистентной АГ. В исследовании L. Mosso et al. (2003), включившем более 600 пациентов с АГ, распространенность первичного альдостеронизма составила 6,1%, при этом она зависела от выраженности гипертензии и среди лиц с тяжелой АГ (>180/110 мм рт. ст.) достигала 13%. В исследовании B.J. Gallay et al. (2001), проведенном в г. Сиэттл (США), первичный альдостеронизм был диагностирован у 17% пациентов с резистентной АГ. Ученые из Алабамского университета г. Бирмингема, США (D.A. Calhoun et al., 2002) по результатам своего небольшого исследования сделали вывод о том, что количество лиц с первичным альдостеронизмом среди больных резистентной АГ может достигать приблизительно 20%. Подтверждают этот вывод и результаты исследования норвежские ученые из г. Осло (I.K. Eide et al., 2004), данные которого свидетельствуют о наличии 23% лиц с первичным альдостеронизмом среди больных резистентной АГ. Для выявления первичного альдостеронизма рекомендуется определение соотношения альдостерон/ренин в плазме крови. Это одно из нововведений последних лет; раньше для того, чтобы заподозрить альдостеронизм, рекомендовалось ориентироваться на наличие гипокалиемии и признаков опухоли надпочечников. На сегодня известно, что у значительной части пациентов с первичным альдостеронизмом уровень калия в крови существенно не изменяется, а сложные визуализирующие обследования без особых показаний на то не могут использоваться в широкой клинической практике. Уровень соотношения альдостерон/ренин плазмы крови ≥ 20 является достаточно чувствительным и специфичным признаком гиперальдостеронизма, а после этого для подтверждения диагноза рентабельно использовать компьютерную томографию органов брюшной полости и другие необходимые методы обследования. Обструктивное сонное апноэ четко ассоциируется с АГ, в том числе является предиктором развития АГ у исходно нормотензивных пациентов (F.J. Nieto et al., 2000; P.E. Peppard et al., 2000). Предположительно, периодически возникающая гипоксия и/или увеличение резистентности верхних дыхательных путей, ассоциированные с обструктивным ночным апноэ, способствуют гиперактивации симпатической нервной системы, что обусловливает повышение АД. Недиагностированное и нелеченное обструктивное сонное апноэ может лежать в основе резистентности АГ к терапии. По данным E. Pimenta et al. [8], до 85% пациентов с резистентной АГ могут страдать обструктивным сонным апноэ. В настоящее время проблема сонного апноэ и ее влияние на контроль АД остаются недостаточно изученными, однако известно, что апноэ более распространено и более выражено у мужчин, чем у женщин, и что его наличие уменьшает вероятность успешного лечения АГ и способствует увеличению количества антигипертензивных препаратов, требующихся для достижения целевых уровней АД. Необходимо привести и данные, свидетельствующие о влиянии почечной патологии на развитие резистентной АГ. Хроническое заболевание почек, как известно, является и одной из важнейших причин, и нередким осложнением плохо контролируемой АГ. Ассоциацию между нарушением функции почек и резистентностью АГ можно объяснить прежде всего возрастанием уровня натрия в крови, задержкой жидкости в организме и соответствующим увеличением циркулирующего объема крови. Кроме того, наличие паренхиматозной патологии почек автоматически увеличивает требовательность к антигипертензивной терапии, определяя более низкие целевые уровни АД, чем в общей популяции. В одном из недавних исследований (M.G. Saelen et al., 2005) было показано, что при хроническом заболевании почек АД удавалось удерживать в рамках целевых цифр (<130/80 мм рт. ст.) менее чем у 15% пациентов, несмотря на использование в среднем 3 антигипертензивных препаратов. По данным исследования ALLHAT наличие хронического заболевания почек было четким предиктором недостижения целевых цифр АД. Важно также помнить о такой проблеме, как сахарный диабет. Не являясь непосредственной причиной развития резистентной АГ как осложнения основного заболевания, СД обусловливает значительное возрастание риска плохого контроля АД и сам по себе также требует более низких целевых уровней АД. Как и хроническое заболевание почек, СД в исследовании ALLHAT был предиктором недостижения целевых цифр АД. Многочисленные клинические исследования не раз подтверждали, что для успешного контроля АД у диабетиков чаще требуется комбинированная антигипертензивная терапия – например, по данным G.L. Bakris (2001), в среднем от 2,8 до 4,2 препарата. В научном соглашении AHA [1] приводятся также основные доказательные данные, касающиеся взаимосвязей между резистентной АГ и другими заболеваниями, такими как феохромоцитома, синдром Кушинга, стеноз почечных артерий и другие. Лечение В документе [1] подчеркивается, что лечение резистентной АГ должно включать: 1. выявление факторов риска резистентной АГ, обусловленных образом жизни, и проведение соответствующих мероприятий по модификации образа жизни; 2. диагностику и лечение основных заболеваний, которые могут быть причинами вторичной АГ, а также исключение медикаментов, побочным эффектом которых является повышение АД; 3. использование эффективных комбинированных стратегий терапии.
Факторы риска и модификация образа жизни К модифицируемым факторам риска резистентной АГ относятся ожирение, избыточное потребление поваренной соли, злоупотребление алкоголем.
Ожирение, как показано в ряде исследований, ассоциировано с более выраженной гипертензией и с ухудшением контроля АД (увеличением потребности в количестве антигипертензивных препаратов, возрастанием риска недостижения целевых цифр АД). Такая взаимосвязь объясняется сложными патофизиологическими механизмами, среди которых наибольшее значение имеют нарушение выведения натрия из организма, чрезмерная стимуляция симпатической нервной системы, активация ренин-ангиотензин-альдостероновой системы. В связи с этим избыточный вес тела тесно ассоциирован с резистентной АГ. Соответственно, снижение веса положительно сказывается и на уровне АД, и на количестве препаратов, необходимых для его контроля. Например, в исследовании L. Aucott et al. (2005) было показано, что снижение массы тела на 10 кг у лиц с ожирением приводит к уменьшению систолического АД в среднем на 6 мм рт. ст. и диастолического – на 4,6 мм рт. ст. Ранее проведенный метаанализ J.E. Neter et al. (2003) продемонстрировал, что наибольшие преимущества от снижения массы тела получают пациенты, которые уже получают антигипертензивную терапию. Чрезмерное потребление поваренной соли обусловливает непосредственное повышение АД за счет увеличения концентрации натрия и задержки жидкости в организме, а также снижение эффекта большинства использующихся в современной клинической практике антигипертензивных препаратов. Эта проблема наиболее выражена у пациентов с так называемой солечувствительностью (склонностью к задержке соли в организме и более выраженной реакции АД на эту задержку), к которым относятся пожилые люди, лица негроидной расы и особенно пациенты, страдающие хроническим заболеванием почек. Отказ от избытка соли в пище способствует снижению как систолического, так и диастолического АД (в среднем на 5-10 и 2-6 мм рт. ст. соответственно), причем лица с солечувствительностью получают от этого простого изменения в своем питании наибольшие преимущества (F.J. He et al., 2005; W.M. Vollmer et al., 2001). Кроме того, согласно общепринятым подходам к профилактике сердечно-сосудистых заболеваний, лицам с резистентной АГ следует рекомендовать улучшить рацион за счет снижения в нем количества жиров и увеличения содержания клетчатки. Эти рекомендации основываются на данных, полученных в результате многочисленных исследований, проводимых в последние годы и посвященных диете DASH (Dietary Approaches to Stop Hypertension, или диета, направленная на борьбу с АГ). На фоне этой диеты, включающей большое количество фруктов, овощей и маложирных молочных продуктов с уменьшенным содержанием как насыщенного, так и общего жира у пациентов с АГ было достигнуто снижение АД на 11,4/5,5 мм рт. ст. (L.J. Appel et al., 1997). Злоупотребление алкоголем увеличивает риск как АГ в целом, так и ее варианта, устойчивого к стандартной терапии. По заключению экспертов AHA суточное потребление алкоголя не должно превышать 2 стандартные американские порции, или 1 унцию этанола (что примерно соответствует 700 мл пива, 300 мл вина, 90 мл крепких спиртных напитков), для большинства мужчин и 1 стандартную порцию для женщин и мужчин с субтильной конституцией (соответственно спиртных напитков в перерасчете на этанол не более 0,5 унции). Очень важна также борьба с гиподинамией. Ряд клинических исследований подтверждает, что регулярная физическая активность сама по себе способствует некоторому снижению повышенного АД, в том числе в случае тяжелой и плохо контролируемой АГ. Согласно общепринятым подходам к профилактике сердечно-сосудистых заболеваний, пациентам необходимо рекомендовать активную физическую нагрузку на протяжении не менее 30 минут в день, по возможности ежедневно.
Лекарственнозависимая резистентная АГ
Кроме того, следует помнить о том, что резистентная гипертензия может быть результатом повышения АД в качестве побочного эффекта каких-либо лекарственных средств. К таким препаратам относятся ненаркотические анальгетики (как селективные ингибиторы циклооксигеназы 2, так и неселективные нестероидные противовоспалительные препараты (НПВП), в том числе аспирин), различные симпатомиметики (часто входят в состав деконгестантов, препаратов для снижения веса), стимуляторы центральной нервной системы (метилфенидат, дексметилфенидат, амфетамины, модафинил), пероральные контрацептивы, эритропоэтин, а также некоторые средства с компонентами растительного происхождения (солодка, хвойник). Известно и неблагоприятное действие кортикостероидов на уровень АД. Поэтому при наличии плохо контролируемого АД необходимо тщательно расспросить пациента о принимаемых им препаратах и средствах народной медицины и при необходимости исключить эти препараты. Так, применение НПВП является одной из наиболее распространенных причин небольшого, но вполне предсказуемого повышения АД, не объяснимого другими причинами. В метаанализе A.G. Johnson et al. (1994) было показано, что использование НПВП нередко обусловливает увеличение среднего АД приблизительно на 5 мм рт. ст. У некоторых лиц с индивидуальными особенностями обмена жидкости в организме и работы почек такой побочный эффект может быть достаточно выраженным, особенно у пожилых людей, лиц с СД или хроническим заболеванием почек. Некоторые другие исследования (A. Whelton et al., 2002; W.B. White et al., 2002) демонстрировали, что НПВП снижают антигипертензивную эффективность нескольких классов широко назначаемых препаратов, включая диуретики, ингибиторы ангиотензинпревращающего фермента (АПФ), блокаторы рецепторов ангиотензина II, β-блокаторы. В статье, посвященной обзору нового научного соглашения AHA и его доказательной базе, E. Pimenta et al. приводят также данные о влиянии гормональных препаратов на контроль АД [8]. Они указывают, что пероральные контрацептивы обусловливают небольшое повышение АД у большинства женщин, принимающих эти препараты, хотя собственно АГ по этой причине развивается у очень небольшого количества пациенток. По данным крупного исследования Nurses’ Health Study, в котором участвовало 68 297 здоровых нормотензивных медсестер, прием пероральных контрацептивов на протяжении 4 лет обусловил возрастание риска развития АГ на 80% по сравнению с женщинами, не принимавшими эти препараты (однако после прекращения приема контрацептивов этот риск полностью исчезал). Кроме того, прием пероральных контрацептивов у лиц с уже имеющейся АГ увеличивает вероятность плохого контроля АД, как показали другие клинические исследования. Интересно, что комбинированные гормональные препараты (эстроген+прогестин) чаще ассоциируются с ростом АД, чем прогестиновые монопрепараты. Наряду с этим гормональная терапия, показанная с терапевтическими целями при менопаузе, оказывает минимальное воздействие на уровень АД и не может считаться противопоказанной ни у нормотензивных женщин, ни при наличии АГ. В последнем случае, подчеркивают E. Pimenta et al. (2008), женщина с АГ, которая начала принимать гормональные препараты для коррекции менопаузальных нарушений, должна более тщательно следить за уровнем АД [8]. Таким образом, при диагностированной резистентной АГ рекомендуется отменить препараты, которые могут обусловливать лекарственнозависимое повышение АД, или перейти на минимально эффективную дозу этих препаратов.
Медикаментозное лечение резистентной АГ
К основным мероприятиям по оптимизации антигипертензивной терапии относятся следующие: поиск адекватной дозы диуретика, максимальное увеличение приверженности пациента к терапии, рекомендация принимать хотя бы один из назначенных антигипертензивных препаратов непосредственно перед сном. Особенно важно, чтобы пациент принимал диуретик (в достаточной дозе и правильном режиме). Одним из наиболее значимых патофизиологических механизмов в формировании резистентной АГ является неадекватное выведение жидкости из организма (по тем или иным причинам). Поэтому отсутствие или неэффективное использование диуретической терапии – одна из наиболее распространенных ошибок в лечении АГ и, соответственно, важная причина плохого контроля АД, подчеркивается в соглашении. Одной из первых задач врача при корригировании схемы лечения в случае недостаточного контроля АД должно быть выяснение следующих вопросов: получает ли пациент диуретик, в достаточной ли дозе тот назначен и не следует ли заменить тиазидный диуретик на петлевой, если обнаруживается, что функция почек снижена в значительной степени (клиренс креатинина <30 мл/мин [8]). В соглашении [1] приводится ряд доказательных данных, указывающих на то, что в различных ситуациях плохого контроля АГ в большинстве случаев добавление диуретика в схему терапии или увеличение его дозы приводило к существенному улучшению контроля АД. Вообще следует подчеркнуть, что с 2002 г., когда были получены результаты исследования ALLHAT, представления о роли диуретиков в антигипертензивной терапии значительно изменились. В 2003 г. результаты ALLHAT обусловили важнейшее положение нового доклада Национального комитета США по профилактике, выявлению, оценке и лечению АГ (JNC-7) о предпочтительности тиазидных диуретиков в лечении АГ: препараты этого ряда были названы средствами, с которых следует начинать лечение (за исключением особых клинических ситуаций, когда более показаны антигипертензивные препараты другого класса) и которые должны быть обязательной составляющей многокомпонентного антигипертензивного вмешательства [3]. Этот тезис отображен и в новом соглашении AHA по ведению больных с резистентной АГ [1]. При этом, согласно имеющейся доказательной базе, диуретики длительного действия имеют более выраженное влияние на плохо контролируемую АГ. Так, хлорталидон демонстрировал явные преимущества над гидрохлортиазидом (M.E. Ernst et al., 2006; D.A. Sica, 2006). В связи с этим при резистентной АГ эксперты AHA рекомендуют отдавать предпочтение хлорталидону. К сожалению, хлорталидон в отличие от гидрохлортиазида в настоящее время включен в очень немногие фиксированные комбинации антигипертензивных препаратов. То же самое касается петлевых диуретиков – по возможности следует делать выбор в пользу препаратов длительного действия, таких как торасемид, хотя фуросемид более доступен. Кроме стандартных антигипертензивных препаратов, в случае истинной резистентной АГ нередко показаны и другие средства, воздействующие на дополнительные патофизиологические механизмы. Так, совсем недавно были доказаны преимущества блокаторов рецепторов минералокортикоидов для таких больных (спиронолактон, амилорид, эплеренон). Причем авторы соглашения указывают на то, что даже если у пациента с резистентной АГ нет первичного альдостеронизма, препараты группы антагонистов альдостерона все же могут оказаться полезными для него. По всей видимости, благоприятный эффект при этом достигается за счет оптимизации диуреза вследствие воздействия на дополнительные патофизиологические механизмы, на которые не действуют тиазидные диуретики. В документе приводятся результаты небольшого исследования M.K. Nishizaka et al. (2003), в котором было показано, что у пациентов с резистентной АГ вне зависимости от исходного уровня альдостерона в крови добавление низких доз спиронолактона (12,5-50 мг/сут) к стандартной антигипертензивной терапии (в среднем 4 препарата, включая тиазидный диуретик и ингибитор АПФ или блокатор рецепторов ангиотензина II) приводило к дополнительному снижению систолического АД на 25 мм рт. ст. и диастолического – на 12 мм рт. ст. Похожие результаты были получены ранее в исследовании J. Ouzan et al. (2002), в котором спиронолактон, добавленный в схему лечения с как минимум двумя антигипертензивными препаратами (в большинстве случаев – с тиазидным диуретиком), способствовал дополнительному снижению АД на 24/10 мм рт. ст. у пациентов с неконтролированной АГ. Другие антагонисты альдостерона также демонстрировали подобные преимущества при плохом контроле АД. Так, в небольшом исследовании I.K. Eide et al. (2004) добавление комбинации амилорида (2,5 мг) и гидрохлортиазида (25 мг) к стандартной комбинированной терапии обусловливало дополнительное снижение АД на 31/15 мм рт. ст., а у нескольких пациентов дозы этих препаратов были удвоены, благодаря чему было получено снижение АД еще на 11/4 мм рт. ст. В исследовании С. Saha et al. (2005) пациентам, у которых АГ не контролировалась двумя антигипертензивными препаратами (один из которых был диуретиком), были дополнительно назначены амилорид 10 мг, спиронолактон 25 мг или комбинация обоих препаратов; в результате было достигнуто дополнительное снижение АД на 12,2/4,8 мм рт. ст. в группе амилорида, 7,3/3,3 мм рт. ст. – спиронолактона и 14,1/5,1 мм рт. ст. в группе комбинации амилорида и спиронолактона. Во всех приведенных исследованиях амилорид и спиронолактон проявили себя как достаточно безопасные и хорошо переносимые препараты. Однако следует помнить, что применение антагонистов альдостерона требует специального биохимического мониторинга, прежде всего контроля уровня калия в крови, учитывая риск развития гиперкалиемии на фоне такого лечения, особенно у пациентов пожилого возраста, лиц с СД и/или хроническим заболеванием почек, а также при использовании таких препаратов, как ингибиторы АПФ, блокаторы рецепторов ангиотензина II, НПВП. Но если почечная функция в норме и уровень калия в крови не повышен, добавление к стандартной комбинированной антигипертензивной терапии 25 мг спиронолактона 1 раз в сутки может оказаться решающим для достижения целевого уровня АД у пациента с резистентной АГ. Через две недели после назначения антагониста альдостерона необходимо повторить измерение АД и биохимический анализ крови, чтобы убедиться в эффективности и безопасности такого лечения. Большое внимание в документе [1] уделяется общим принципам комбинированной терапии в случае резистентной АГ. К сожалению, четкие доказательные данные в настоящее время имеются только относительно отдельных антигипертензивных препаратов и некоторых комбинаций двух различных препаратов. Однако доказательная база относительно комбинаций из 3 и более антигипертензивных средств резко ограничена, поэтому рекомендации по комбинированной антигипертензивной терапии, особенно в таких сложных случаях, как резистентная АГ, пока что носят преимущественно эмпирический характер и опираются в основном на консенсус экспертов. Эффективную и безопасную комбинацию из 4 и более препаратов достаточно сложно подобрать, поскольку необходимо учитывать индивидуальную восприимчивость пациента, риск развития побочных эффектов, наличие противопоказаний и ограничений к применению тех или иных препаратов, финансовую состоятельность пациента и другие факторы. Эмпирически был сделан вывод о том, что при комбинированной антигипертензивной терапии следует сочетать препараты из различных классов, действующих на разные патофизиологические механизмы. В этом отношении неплохо зарекомендовала себя комбинация тиазидный диуретик + ингибитор АПФ или блокатор рецепторов ангиотензина II + блокатор кальциевых каналов. Как правило, такая тройная комбинация достаточно эффективна и хорошо переносится. Кроме того, для такой схемы терапии проще подобрать фиксированные комбинированные препараты с 2 или 3 действующими веществами в одной таблетке, требующие однократного приема в сутки. Что касается режима приема препаратов, то в соглашении экспертов AHA [1] приводится новая рекомендация: по крайней мере, один из используемых антигипертензивных препаратов должен приниматься на ночь. Недавнее исследование R.C. Hermida et al. (2005) показало, что такая простая мера способствует улучшению 24-часового контроля гипертензии и снижению АД в особенно опасные ночные и ранние утренние часы. Таким образом, в случае резистентной АГ оптимальной представляется такая схема лечения, которая подразумевает двукратный прием препаратов в течение суток, один из которых должен быть незадолго до ночного сна. При резистентной АГ нередко приходится прибегать также к таким сильным вазодилататорам, как гидролазин или миноксидил. Они достаточно эффективно снижают АД, однако их применение часто сопровождается выраженными побочными эффектами, в связи с чем использование таких препаратов ограничено. Так, миноксидил обычно настолько сильно увеличивает частоту сердечных сокращений и задержку жидкости в организме, что для сглаживания его побочных эффектов часто требуется назначение таких препаратов, как β-блокаторы и петлевые диуретики. Учитывая необходимость использования большого количества антигипертензивных средств, особое внимание следует обратить на максимальное упрощение режима их приема. Врач должен помнить, что мультилекарственная комбинированная терапия – это палка о двух концах; чем больше препаратов назначается и чем сложнее схема их приема, тем меньше вероятность того, что больной будет соблюдать режим лечения. В связи с этим следует отдавать предпочтение фиксированным комбинациям (два или три разных действующих вещества в одной таблетке), а также препаратам длительного действия, требующим однократного приема в сутки. Следует поощрять как самостоятельный контроль АД пациентами с помощью домашних тонометров, так и регулярные посещения врача.
Алгоритм диагностики и лечения Суммируя вышесказанное, эксперты AHA рекомендуют следовать такому алгоритму ведения больного с резистентной АГ: 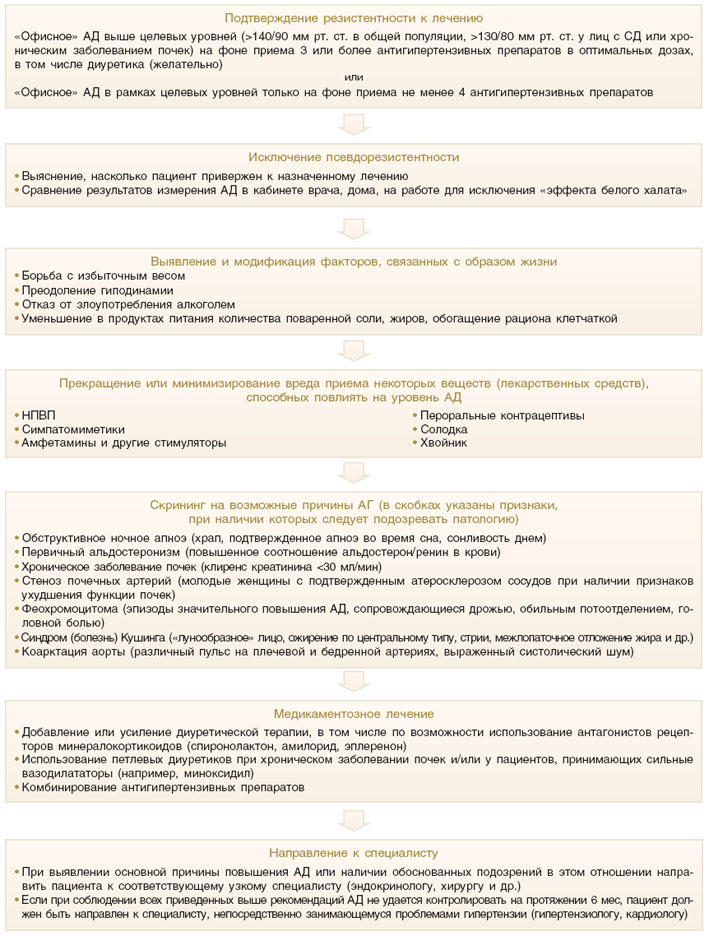
Авторы соглашения [1] делают заключение о том, что проблема резистентной АГ, к сожалению, в настоящее время остается малоизученной и требует организации специальных эпидемиологических и клинических исследований на достаточно больших когортах пациентов. Нет сомнений, что эта специфическая подгруппа больных АГ достаточно велика и требует особого внимания к себе с точки зрения профилактики, диагностики, лечения. Большие перспективы имеет и изучение генетической подоплеки резистентной АГ, а также фармакогенетических аспектов ее лечения, говорится в соглашении. Литература: 1. Calhoun D.A., Jones D., Textor S. et al. Resistant hypertension: diagnosis, evaluation, and treatment. A scientific statement from the American Heart Association Professional Education Committee of the Council for High Blood Pressure Research. Hypertension 2008; 51: 1403-1419. 2. Brookes L. New Guidelines for Resistant Hypertension From the AHA, Plus Targets, Treatments, and Marriage. Medscape Cardiology 2008 (http://www.medscape.com) 3. Chobanian A.V., Bakris G.L., Black H.R. et al; Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High lood Pressure. National Heart, Lung, and Blood Institute; National High Blood Pressure Education Program Coordinating Committee. Seventh report of the Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure. Hypertension 2003; 42:1206-1252. 4. Hajjar I., Kotchen T.A. Trends in prevalence, awareness, treatment, and control of hypertension in the United States, 1988-2000. JAMA 2003; 290: 199-206. 5. Lloyd-Jones D.M., Evans J.C., Larson M.G. et al. Differential control of systolic and diastolic blood pressure: factors associated with lack of blood pressure control in the community. Hypertension 2000; 36: 594-599. 6. Pickering T.G., Hall J.E., Appel L.J. et al. Recommendations of blood pressure measurement in humans and experimental animals. Part 1: blood pressure measurement in humans. A Statement for Professionals from the Subcommittee of Professional and Public Education of the American Heart Association Council on High Blood Pressure Research. Circulation 2005; 111: 697-716. 7. Brown M.J., Cruickshank J.K., Dominiczak A.F. et al.; Executive Committee, British Hypertension Society. Better blood pressure control: how to combine drugs. J Hum Hypertens 2003; 17: 81-86. 8. Pimenta E., Gaddam K.K., Oparil S. Mechanisms and Treatment of Resistant Hypertension. J Clin Hypertens 2008; 10(3): 239-244. 9. Calhoun D.A. Resistant or difficult-to-treat hypertension. J Clin Hypertens 2006; 8: 181-186. 10. Okonofua E.C., Simpson K.N., Jesri A. et al. Therapeutic inertia is an impediment to achieving the healthy people 2010 blood pressure control goals. Hypertension 2006; 47: 345-351. Автор обзора Александра Ратманова Medicine Review 2008; 3 (03): 06-13 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2026. Усі права захищені.
|
мапа сайту корисні посилання |