Комбинированная терапия артериальной гипертензии при сахарном диабете и альбуминурииОбзор исследования R. Fernandez, J.G. Puig, J.C. Rodriguez-Perez et al., on behalf of the TRAVEND Study Group. Effect of two antihypertensive combinations on metabolic control in type-2 diabetic hypertensive patients with albuminuria: a randomised, double-blind study. Journal of Human Hypertension 2001; 15, 849-856 [1]
Артериальная гипертензия (АГ) и сахарный диабет (СД) остаются одними из наиболее распространенных заболеваний во всем мире. Кроме того, распространенность их в современном обществе постоянно растет и, согласно прогнозам, будет продолжать увеличиваться в ближайшие годы. Обе эти патологии не только существенно увеличивают кардиоваскулярный риск, но и часто сочетаются друг с другом. Это способствует скорейшему развитию осложнений, прежде всего со стороны почек, а также других органов-мишеней. Кроме того, сочетание АГ и СД приводит к значительному возрастанию риска развития инсульта, ишемической болезни сердца, застойной сердечной недостаточности, других сердечно-сосудистых заболеваний и событий, значительно повышающих смертность среди пациентов. В силу общности ряда факторов риска и патофизиологических механизмов, АГ встречается у большинства (70-80%) больных СД [3]. Вероятность развития АГ на фоне диабета увеличивается в зависимости от типа СД, возраста и этнической принадлежности пациента, наличия ожирения и других компонентов метаболического синдрома [2]. И наоборот – у лиц с повышенным артериальным давлением (АД) вероятность развития СД в течение ближайших 5 лет в 2,5 раза выше, чем в общей популяции [5]. АГ на фоне диабета требует особого подхода к лечению. В связи с наличием у таких больных целого кластера метаболических нарушений (нарушенная толерантность к углеводам, инсулинорезистентность, гипергликемия, обычно также дислипидемия) необходимо подбирать схему терапии, которая не имеет неблагоприятных метаболических влияний и, по возможности, оказывает положительные эффекты на имеющиеся нарушения обмена веществ. При назначении антигипертензивных препаратов больному с СД врач должен принимать во внимание не только необходимость достижения более низких целевых уровней АД, чем в общей популяции лиц с АГ, но и «метаболический профиль» предписанных препаратов, то есть их влияние на нарушенный обмен веществ (негативное, нейтральное или благоприятное). Рекомендации, касающиеся особенностей стратегии лечения больных с АГ и СД, содержатся во всех современных практических руководствах. Европейское общество кардиологов и Европейское общество по гипертензии в 2007 г. опубликовали совместное руководство по лечению АГ [3], в котором для больных с сочетанием АГ и СД предписывается необходимость использования эффективных и хорошо переносимых антигипертензивных препаратов. При этом особый акцент делается на том, что в таких случаях чаще всего приходится прибегать к комбинированному лечению. Это обусловлено и более низким целевым уровнем АД у больных диабетом (<130/80 мм рт. ст.), и необходимостью избежать побочных эффектов метаболического характера (комбинированная терапия позволяет использовать более низкие дозы каждого из действующих веществ, тем самым снижая риск побочных эффектов). Согласно этим же рекомендациям, приоритетными препаратами для лечения АГ на фоне СД названы блокаторы ренин-ангиотензин-альдостероновой системы (РААС), то есть ингибиторы ангиотензинпревращающего фермента (АПФ) и блокаторы рецепторов ангиотензина II. Эти препараты доказали свои антигипертензивные и органопротективные (особенно – ренопротективные) эффекты и потому рекомендуются авторами руководства как одна из обязательных составляющих комбинированной антигипертензивной терапии, а также рассматриваются как предпочтительные в случае, если монотерапии для контроля АД достаточно. Наличие микроальбуминурии у больного с СД требует назначения этих препаратов даже на фоне нормального АД, поскольку блокаторы РААС четко подтвердили свои выраженные ренопротективные эффекты, независимо от антигипертензивного действия [3]. Подобные предписания рекомендуются также стандартами Американской диабетической ассоциации по лечению СД (2008), руководством по ведению АГ Британского общества по гипертензии (2004), 7-м докладом Национального комитета США по профилактике, выявлению, оценке и лечению АГ (JNC-7, 2003) и другими авторитетными документами международного значения [4-6]. Таким образом, и при СД, и при микроальбуминурии предпочтительными антигипертензивными препаратами являются блокаторы РААС. В случае сочетания АГ, СД и микроальбуминурии они также являются приоритетными. Остальные группы антигипертензивных препаратов (диуретики, блокаторы кальциевых каналов, β-блокаторы) продемонстрировали менее определенные результаты в различных исследованиях, поэтому в соответствующих руководствах указывается, что выбор между ними должен делаться исходя из самых различных факторов – доступности, переносимости препарата, индивидуальных показаний и противопоказаний. Особенно важно в клинической ситуации, при которой сочетаются АГ, СД и нефропатия, учитывать метаболические эффекты антигипертензивного препарата. В связи с этим хотелось бы обратить внимание наших читателей на одно из исследований последних лет, посвященных лечению больных, у которых имеются и АГ, и СД, и признаки нарушения функции почек (альбуминурия). Это исследование TRAVEND (2001), в котором сравнивались две фиксированные комбинации антигипертензивных препаратов – ингибитора АПФ и блокатора кальциевых каналов (трандолаприл + верапамил SR) и ингибитора АПФ и тиазидного диуретика (эналаприл + гидрохлортиазид) [1]. Целью исследования TRAVEND было определить влияние обеих комбинаций на метаболический контроль и функцию почек у больных с сочетанием АГ, контролированного СД 2 типа и альбуминурии. Материалы и методы Это было проспективное рандомизированное двойное слепое в параллельных группах контролированное исследование, в котором участвовали 103 пациента из 11 клиник Испании. В исследование включались лица с СД 2 типа, постоянной альбуминурией (30-3000 мг/сут) и АГ (АД>140/90 мм рт. ст.), которая не контролировалась каким-либо монокомпонентным антигипертензивным препаратом. Не включались в исследование лица со вторичной АГ, застойной СН (III-IV функциональные классы по NYHA), уровнем креатинина сыворотки крови более 3 мг/дл, пациенты с повышенной чувствительностью или непереносимостью ингибиторов АПФ и/или блокаторов кальциевых каналов, а также те, которые на момент начала исследования не принимали антигипертензивную терапию вовсе или принимали два и более антигипертензивных препарата. Большинство (66%) больных были мужского пола; средний возраст участников исследования составил 55 лет. После 4 нед отмывочного периода пациенты рандомизировались на две группы: участники одной из них (51 пациент) принимали трандолаприл 2 мг/сут и верапамил замедленного высвобождения (slow release, SR) 180 мг/сут; другой (52 пациента) – эналаприл 20 мг/сут и гидрохлортиазид 12,5 мг/сут. Кроме этого, пациентам было рекомендовано уменьшить потребление соли и углеводов с пищей, а также продолжать предписанное им ранее противодиабетическое лечение. Наблюдение за пациентами продолжалось 6 мес. В начале исследования, а также на 12-й и 24-й неделях оценивались уровни систолического и диастолического АД, суточная альбуминурия, гликемия, содержание гликозилированного гемоглобина; выполнялись также рутинные клинические обследования, биохимические и гематологические тесты, определялось наличие сопутствующей патологии и побочных эффектов лечения. Кроме того, в начале и в конце исследования проводилось суточное мониторирование АД. Результаты Исследование закончили 93 пациента. Из десяти выбывших только у двоих развились побочные эффекты (отеки), остальные прекратили участвовать в исследовании по другим причинам (нарушение протокола исследования – 5 человек; плохой контроль АД – 3 человека). Через 6 мес терапии в обеих группах выявлено достоверное сопоставимое снижение АД и альбуминурии. АД уменьшилось в среднем на 17/12 мм рт. ст. (16/11 в группе трандолаприл + верапамил SR и 18/13 в группе эналаприл + гидрохлортиазид, без статистически значимых различий между группами) – со 157,3±12,0/98,3±6,4 до 140,5±14,5/86,1±8,2 мм рт. ст. (p<0,001), причем такие результаты были достигнуты преимущественно в первые 4 нед приема препаратов. Имело место и достоверное и существенное снижение суточного, дневного и ночного систолического и диастолического АД по данным суточного мониторирования АД, но тоже без статистически значимых различий между группами. Альбуминурия снизиласьс 508,6±693,8 до 253,4±517,2 мг/сут (p<0,001). Статистически значимых различий между первой и второй группами по этому показателю также не было. Однако в отношении показателей, отражающих метаболический контроль, были получены интересные результаты, указывающие на отличия между изучаемыми комбинациями. Если в группе эналаприл + гидрохлортиазид содержание гликозилированного гемоглобина (НbА1с) за время исследования увеличилось (5,96±1,25% в начале исследования, 6,41±1,51% в конце), то в группе трандолаприл + верапамил SR оно существенно не изменилось (5,91±1,43% в начале исследования, 5,94±1,62% в конце) (рисунок). 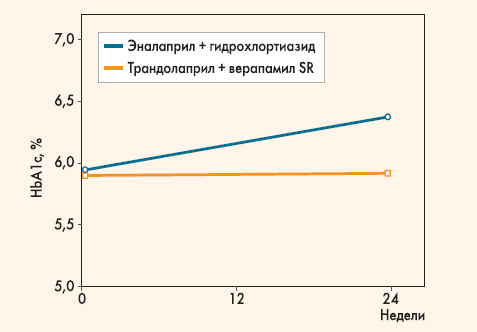
Рисунок. Изменения уровня гликозилированного гемоглобина на фоне лечением комбинациями эналаприл + гидрохлортиазид и трандолаприл + верапамил SR в исследовании TRAVEND (по R. Fernandez et al., 2001 [1]) Количество пациентов, у которых гликемия находилась в рамках целевых уровней (<126 мг/дл, или 7,0 ммоль/л), в группе трандолаприл + верапамил SR за время исследования возросло с 50 до 72,7%, а в группе эналаприл + гидрохлортиазид практически не изменилось (47,7% в начале исследования, 50% в конце). Для других показателей (масса тела, содержание в сыворотке крови креатинина, мочевой кислоты, калия, холестерина, триглицеридов, альбумина) за время лечения не было отмечено значимых изменений в обеих группах. Безопасность обеих комбинаций была оценена как удовлетворительная и сравнимая. Всего было зарегистрировано 59 случаев развития побочных эффектов у 31 пациента: 30 случаев развития побочных эффектов у 15 пациентов в группе трандолаприл + верапамил SR (29,4%) и 29 случаев развития побочных эффектов у 16 пациентов в группе эналаприл + гидрохлортиазид (30,8%). Чаще всего имели место симптомы слабой или умеренной выраженности, только два пациента (по одному в каждой группе) прекратили прием антигипертензивных препаратов по причине выраженных побочных эффектов (в обоих случаях из-за отеков). Исходя из вышесказанного, необходимо подчеркнуть следующее. Достоверные различия между группами были отмечены только для такого показателя, как гликозилированный гемоглобин (различия в уровне НbА1с составили 0,45%, p=0,04). Остальные показатели либо контролировались обеими комбинациями в равной мере (без статистически достоверных различий), либо не изменялись под действием ни одной из изучаемых комбинаций. Обсуждение Известно, что многие антигипертензивные препараты оказывают неблагоприятные метаболические влияния. Как показывают исследования последних лет, диуретики и β-блокаторы способны увеличивать риск развития СД (R. Donahue et al., 1990) и ухудшать гликемический контроль при уже имеющемся диабете (J.R. Sowers, 1995; G.L. Bakris et al., 2000). Неоднократно было показано, что тиазидные диуретики, по крайней мере в высоких дозах, могут ухудшать толерантность к глюкозе и увеличивать инсулинорезистентность (T. Pollare et al., 1989; N.M. Kaplan, 1992). Поэтому очевидно, что для длительной терапии АГ на фоне метаболических нарушений (прежде всего диабета) эти препараты не должны рассматриваться как средства первого выбора, хотя этот вопрос еще требует дальнейшего изучения. Напротив, блокаторы РААС (ингибиторы АПФ и блокаторы рецепторов ангиотензина II) неоднократно демонстрировали свои преимущества в отношении метаболических влияний. В этом смысле в последнее время ученые все чаще обращают внимание также на недигидропиридиновые блокаторы кальциевых каналов. В метаанализах D.D. Maki et al. (1995) и P. Weidmann et al. (1995) было показано, что у всех антигипертензивных препаратов долгосрочные благоприятные эффекты в отношении протеинурии пропорциональны их антигипертензивному действию, однако у ингибиторов АПФ и, возможно, у недигидропиридиновых блокаторов кальциевых каналов отмечаются также дополнительные преимущества, независимые от влияния этих препаратов на АД. Верапамил, в отличие от блокаторов кальциевых каналов дигидропиридинового ряда, расширяет не только афферентные, но и эфферентные артериолы почечных клубочков, и в связи с этим не повышает внутриклубочковое гидравлическое давление, что делает этот блокатор кальциевых каналов предпочтительным при наличии патологии почек (G.L. Bakris et al., 1996). Кроме того, этот препарат метаболически нейтрален и потому может достаточно безопасно использоваться при СД и других метаболических нарушениях (G.L. Bakris et al., 2006). Поэтому сочетание верапамила и ингибитора АПФ представляется логичной комбинацией в случае сочетания АГ, СД и нефропатии. Действительно, преимущества комбинирования верапамила с ингибиторами АПФ, в том числе и у пациентов с АГ, СД и нарушенной функцией почек, уже были неоднократно показаны в различных клинических исследованиях [7-10]. По результатам исследования G.L. Bakris et al. (1998) комбинация трандолаприл + верапамил SR у больных с АГ, СД 2 типа и нефропатией уменьшала протеинурию в значительно большей степени, чем верапамил SR и трандолаприл в качестве монотерапии (на 62,27 и 33% соответственно), причем независимо от антигипертензивного эффекта (он был сопоставим во всех трех группах). Изучение этой фиксированной комбинации в сравнении с другими антигипертензивными комбинациями показало ее преимущества – по отношению как к функции почек, так и к метаболическим процессам [7-10]. В мультицентровом рандомизированном двойном слепом исследовании H. Holzgreve et al. (2000) лечение больных АГ и СД 2 типа комбинацией трандолаприл + верапамил SR на протяжении 20 нед обеспечило стабилизацию уровня гликозилированного гемоглобина на уровне 7,9% и тем самым привело к лучшему гликемическому контролю по сравнению с комбинацией атенолол + хлорталидон (на фоне приема последней уровень НbА1с с начала исследования увеличился с 7,8 до 8,6%, p<0,001). По результатам небольшого сравнительного исследования комбинаций трандолаприл + верапамил SR и атенолол + хлорталидон у больных СД 2 типа установлено, что антигипертензивный эффект обеих комбинаций был сходным, однако при этом комбинация трандолаприл + верапамил SR привела к более выраженному уменьшению суточной экскреции альбумина с мочой, чем в группе атенолол + хлорталидон (33 vs 11%) (M. Schneider et al., 1996). Кроме того, в этом исследовании комбинация трандолаприл + верапамил SR подтвердила свою метаболическую нейтральность, в то время как на фоне приема комбинации атенолол + хлорталидон наблюдалось усугубление инсулинорезистентности, возрастало содержание триглицеридов в крови, уменьшались уровни холестерина липопротеинов высокой плотности и калия плазмы крови. Исследование TRAVEND предоставило новые аргументы в пользу того, что на фоне приема комбинации трандолаприла и верапамила SR достигается лучший метаболический контроль. Прием комбинации трандолаприл + верапамил SR по сравнению с комбинацией эналаприл + гидрохлортиазид. Выводы Таким образом, исследование TRAVEND показало, что длительная (на протяжении 6 мес) терапия комбинацией трандолаприла и верапамила SR не только приводит к достоверному и клинически значимому снижению АД и уменьшению альбуминурии (сравнимое с таковым в группе эналаприла и гидрохлортиазида), но и обеспечивает более надежный метаболический контроль. Это особенно важно в связи с тем, что, согласно данным крупного исследования EPIC-Norfolk (2001), повышение HbA1c всего на 1% ассоциировано с возрастанием риска смерти на 28% независимо от возраста, уровня АД и других факторов. В связи с этим авторы исследования [1] рассматривают комбинацию трандолаприл + верапамил SR как оптимальную при сочетании АГ, СД 2 типа и нефропатии. Несомненно, исследования в этом направлении должны продолжаться и охватывать все большее количество больных. Будущее антигипертензивной терапии – в поиске эффективных и безопасных комбинаций, поскольку успешно контролировать АД на монотерапии возможно только у очень малого количества пациентов. Актуальность комбинированного антигипертензивного лечения значительно возрастает при наличии сопутствующей патологии, особенно СД и нефропатии, которые ухудшают контроль АД, повышают кардиоваскулярный риск и несут угрозу быстрого поражения органов-мишеней. В этих сложных, но весьма распространенных клинических ситуациях при разработке оптимальных схем лечения необходимо учитывать не только силу антигипертензивного действия и переносимость препаратов, но и характер их влияния на нарушенный обмен веществ, что принципиально для долгосрочного лечения таких пациентов. Сочетание интенсивной антигипертензивной терапии и улучшенного гликемического контроля уменьшает сердечно-сосудистый риск, предупреждает поражение органов-мишеней, препятствует развитию и прогрессированию ретинопатии, нефро- и нейропатии. В этом отношении исследование TRAVEND является важным этапом соответствующего научно-практического поиска. Литература: 1. Fernandez R., Puig J.G., Rodriguez-Perez J.C. et al.; on behalf of the TRAVEND Study Group. Effect of two antihypertensive combinations on metabolic control in type-2 diabetic hypertensive patients with albuminuria: a randomised, double-blind study. Journal of Human Hypertension 2001; 15, 849-856. 2. Rosamond W. et al. Heart Disease and Stroke Statistics – 2008 Update. A Report From the American Heart Association Statistics Committee and Stroke Statistics Subcommittee. Circulation 2008; 117: e25-e146. 3. Mancia G., De Backer G., Dominiczak A. et al. Guidelines for the management of arterial hypertension: the task force for the management of arterial hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC). J Hypertens 2007; 25: 1105-87. 4. American Diabetes Association: Standards of medical care in diabetes – 2008. Diabetes Care 2008; 31 (Suppl. 1): S12-S54. 5. Chobanian A.V., Bakris G.L., Black H.R. et al.; Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure. National Heart, Lung, and Blood Institute; National High Blood Pressure Education Program Coordinating Committee. Seventh report of the Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure. Hypertension 2003; 42:1206-1252. 6. British Hypertension Society guidelines (BHS-IV). J Fam Pract 2004; 53: 528-50. 7. Reynolds N.A., Wagstaff A.J., Keam S.J. Trandolapril/verapamil sustained release: a review of its use in the treatment of essential hypertension. Drugs 2005; 65 (13): 1893-914. 8. Sharma S.K., Ruggenenti P., Remuzzi G. Managing hypertension in diabetic patients – focus on trandolapril/verapamil combination. Vasc Health Risk Manag 2007; 3 (4): 453-65. 9. Muijsers R.B., Curran M.P., Perry C.M. Fixed combination trandolapril/verapamil sustained-release: a review of its use in essential hypertension. Drugs 2002; 62 (17): 2539-67. 10. Widimsky J. The fixed combination of verapamil SR/trandolapril. Expert Opin Pharmacother 2000; 1 (3): 515-35. Автор обзора Дмитрий Игнатьев Medicine Review 2008; 3 (03): 82-85 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2025. Усі права захищені.
|
мапа сайту корисні посилання |