Безопасность антитромбоцитарной терапии: выбор ингибитора протонной помпыУбедительно доказанная эффективность антитромбоцитарной терапии сделала ее необходимым компонентом долгосрочного лечения больных, перенесших острый коронарный синдром (ОКС), и пациентов после чрескожного коронарного вмешательства (ЧКВ). Традиционно с этой целью применяются ацетилсалициловая кислота (АСК) и клопидогрель, комбинированное назначение которых снижает риск сердечно-сосудистых исходов, в том числе – риск повторного инфаркта миокарда, тромбоза стента и смерти. Однако двойная антитромбоцитарная терапия (ДАТ) обладает не только преимуществами, но и недостатками, среди которых наиболее значимы осложнения со стороны желудочно-кишечного тракта (ЖКТ), и прежде всего гастроинтестинальные кровотечения (ГИК). Как показали исследования, снизить риск ГИК, связанных с ДАТ, позволяет применение ингибиторов протонной помпы (ИПП), в связи с чем был опубликован документ, рекомендующий использовать препараты этой группы у пациентов, нуждающихся в проведении ДАТ и имеющих факторы риска развития кровотечений из верхнего отдела ЖКТ [1]. Однако вскоре после создания этой рекомендации появились новые сведения, свидетельствующие о возможных негативных результатах межлекарственного взаимодействия ИПП и тиенопиридинов [2], что создало определенные сложности в выборе препарата для защиты ЖКТ. ДАТ и риск желудочно-кишечных кровотечений Источником ГИК на фоне ДАТ могут стать различные анатомические объекты – чаще всего кровотечение бывает связано с наличием эзофагита (на фоне гастро-эзофагеального рефлюкса), эрозий и язв на слизистой желудка и тонкого кишечника, ассоциированных с хеликобактерной инфекцией, приемом АСК и нестероидных противовоспалительных препаратов (НПВП) [3, 4]. Тиенопиридины сами по себе не вызывают повреждения слизистой ЖКТ – развитию ГИК на фоне их применения способствует исключительно антитромбоцитарный эффект, реализуемый в местах уже имеющихся дефектов слизистой оболочки [5, 6]. Риск ГИК на фоне ДАТ повышается в присутствии ряда факторов, к которым относятся наличие в анамнезе ГИК или других осложнений язвенной болезни, возраст старше 60 лет, принадлежность к неевропеоидной расе, мужской пол, сахарный диабет, злоупотребление алкоголем в настоящее время и в анамнезе, сердечная недостаточность, почечная недостаточность, гастро-эзофагеальная рефлюксная болезнь, инфицирование H. pylori, применение антикоагулянтов, стероидов или НПВП [1, 7-10]; комбинация перечисленных факторов еще более повышает риск развития ГИК [5]. Риск геморрагических осложнений ДАТ наиболее высок в первые месяцы после коронарного события, но сохраняется и в более поздние сроки (по данным долгосрочных наблюдений). Результаты рандомизированных исследований показали, что монотерапия низкими дозами АСК повышает риск язвообразования в 2 раза по сравнению с отсутствием лечения [11], а ДАТ клопидогрелем и АСК повышает риск ГИК в 2-3 раза по сравнению с монотерапией АСК (хотя абсолютное увеличение риска колеблется в пределах 0,6-2,0%) [12]. В двух рандомизированных клинических исследованиях отношение рисков (ОР) для ГИК, связанных с ДАТ, составило 1,78 (95% доверительный интервал 1,25-2,54) и 1,96 (95% ДИ 1,46-2,63) [13, 14]. В исследовании VALIANT (VALsartan In Acute myocardial iNfarcTion) ОР для смерти от ГИК составило 2,5, показав тем самым, что ГИК являются значимым предиктором смерти кардиологических больных [10]. Риск ГИК, связанных с приемом тиенопридинов, может быть уменьшен путем подавления продукции соляной кислоты, что будет способствовать заживлению язв и эрозий слизистой оболочки, а также стабилизации тромбов [15]. Достичь этой цели позволяет применение ИПП. Защитные эффекты ИПП По данным ряда авторов, использование ИПП или блокаторов Н2-гистаминовых рецепторов по сравнению с отсутствием гастропротекторной терапии значительно снижает риск ГИК, связанных с ДАТ; причем согласно результатам обсервационных исследований ИПП предотвращают ГИК эффективнее, чем блокаторы Н2-гистаминовых рецепторов (отношение шансов 0,04 (95% ДИ 0,002-0,21) и 0,43 (95% ДИ 0,18-0,91) соответственно) [9]. В одном когортном исследовании исходная частота ГИК, связанных с приемом клопидогреля, равная 1,2% в год, была снижена на 50% одновременным приемом ИПП [16]. В этом же исследовании использование ИПП уменьшало абсолютный риск ГИК на 2,8% в год у больных с тремя и более факторами риска кровотечений. В крупном исследовании, сравнившем результаты лечения 2779 пациентов с эндоскопически подтвержденными ГИК и 5532 пациентов в группе контроля, комбинированное использование ИПП и тиенопиридина было связано с меньшим риском ГИК (ОШ 0,19; 95% ДИ 0,07-0,49), чем монотерапия тиенопиридином [17]. Общее положительное представление о возможностях комбинированного применения ИПП и ДАТ омрачили результаты фармакокинетических и фармакодинамических исследований, использовавших показатель степени агрегации тромбоцитов in vitro в качестве суррогатной конечной точки и показавших, что одновременное назначение ИПП и клопидогреля снижает антитромбоцитарный эффект последнего. Анализируя результаты этих исследований, необходимо принимать во внимание некоторые факты. Во-первых, убедительные доказательства негативного взаимодействия получены только для комбинации омепразола/эзомепразола и клопидогреля, в связи с чем регуляторные органы предостерегают врачей от совместного назначения этих препаратов, ссылаясь на возможное значительное снижение уровня активных метаболитов клопидогреля и его антитромбоцитарной активности на фоне применения этих ИПП [18]. Во-вторых, до сих пор не доказано, что связанные с применением ИПП изменения суррогатных конечных точек, зафиксированные в исследованиях in vitro, можно экстраполировать на клиническую эффективность клопидогреля [12]. Данные, полученные из обсервационных и одного рандомизированного клинического исследования, изучавших влияние взаимодействия ИПП и клопидогреля на сердечно-сосудистые исходы, оказались противоречивыми, хотя и показали, что клинически значимое взаимодействие возможно в некоторых подгруппах пациентов, например у больных с генетически обусловленным нарушением метаболизма клопидогреля [12]. ИПП и клопидогрель: пути биотрансформации и возможности для взаимодействия Клопидогрель является пролекарством, которое после абсорбции в ЖКТ попадает в печень, где проходит его двухэтапное превращение в активный метаболит. В процессе активации клопидогреля важную роль играют ферменты системы цитохрома Р450, и прежде всего CYP3A4 и CYP2С19. Одновременный прием препаратов, метаболизм которых также проходит с участием этих ферментов, может привести к снижению концентрации активных метаболитов клопидогреля и уменьшению выраженности его антитромбоцитарного эффекта. Еще одной причиной недостаточной эффективности клопидогреля может стать нарушение его биоактивации вследствие генетически обусловленного снижения активности фермента CYP2C19. Эффективность работы фермента определяется разновидностью кодирующих его аллелей. Аллель *1 отвечает за нормальную активность фермента, наличие в генотипе пациента аллелей CYP2C19*2 и СYР2С19*3 ассоциируется со снижением эффективности связанного с CYP2C19 метаболизма. В результате у гетерозигот по дефектному аллелю (промежуточный метаболизм клопидогреля) эффективность клопидогреля снижается на 2631%, у гомозигот (сниженный метаболизм) – на 46-55% [19], что ассоциируется с недостаточным угнетением агрегации тромбоцитов и увеличением частоты сердечнососудистых исходов [12]. Недостаток влияния на агрегацию тромбоцитов можно преодолеть назначением более высокой дозы клопидогреля, однако следует учитывать, что повышение эффективности в отношении кардиоваскулярных исходов на фоне терапии высокими дозами препарата сопровождается повышенным риском ГИК [20, 21]. Все используемые в настоящее время ИПП (омепразол, эзомепразол, пантопразол, рабепразол, лансопразол и декслансопразол) преобразуются в активные формы в кислой среде желудочного содержимого и метаболизируются системой цитохрома Р450 (в основном изоферментами CYP2C19 и CYP3A4), конкурентно ингибируя активность этих ферментов в отношении других лекарственных препаратов. Константы ингибирования метаболизма CYP3A4 для всех ИПП, определенные in vitro, превышают плазменные концентрации, достигаемые препаратами in vivo [22, 23]. Поэтому клинически значимой является конкуренция клопидогреля и ИПП только за CYP2C19-опосредованный метаболизм. Однако степень аффинности разных представителей группы ИПП к CYP2C19 различна, что и обусловливает разную степень взаимодействия этих препаратов с клопидогрелем [12]. Рабепразол: особенности метаболизма и влияние на эффективность клопидогреля Основным механизмом биотрансформации рабепразола является неферментная реакция восстановления до тиоэфирного соединения, в связи с чем окислительный метаболизм с участием изоферментов CYP2C19 и CYP3A4 играет незначительную роль в превращении этого ИПП. Результаты исследования in vitro показали, что рабепразол оказывает минимальное угнетающее воздействие на изофермент CYP2C19 [22], причем константа ингибирования CYP2C19 для рабепразола, определенная in vitro, оказалась значительно выше достигаемых им in vivo концентраций. Обнаруженная в исследованиях низкая аффинность рабепразола к изоферментам цитохрома Р450 объясняет незначительное вовлечение препарата в опосредованные этими ферментами межлекарственные взаимодействия, хотя число посвященных этому вопросу исследований на данный момент невелико [22, 23]. Исследования по изучению влияния рабепразола на фармакодинамические и клинические эффекты клопидогреля показали результаты, свидетельствующие в пользу комбинированного назначения этих препаратов. В проспективном исследовании Hokimoto S. et al. [24] приняли участие 170 пациентов после ЧКВ с имплантацией стента, принимающих ДАТ (АСК в дозе 100 мг/сут и клопидогрель в дозе 75 мг/сут). Решением лечащих врачей больные были распределены в группы рабепразола (n=37, доза 10-20 мг/сут) и контроля (n=133). Фармакодинамической конечной точкой исследования была назначена степень АДФ-индуцированной агрегации тромбоцитов через 10 мин после приема клопидогреля. Клиническими конечными точками исследования были неблагоприятные сердечно-сосудистые исходы (сердечно-сосудистая смерть, инфаркт миокарда, инсульт), госпитализация по поводу нестабильной стенокардии или желудочно-кишечного кровотечения в течение года наблюдения. При анализе результатов исследования учитывался полиморфизм CYP2C19. Исследования in vitro показали, что степень АДФиндуцированной агрегации тромбоцитов была выше в группе рабепразола (4315±1537), чем в группе контроля (3952±1506), однако разница была статистически незначимой. Влияние вариантов генетического кодирования CYP2C19 на антитромбоцитарный эффект клопидогреля в группах рабепразола и контроля отмечено не было. Различия в частоте сердечно-сосудистых исходов между группами отсутствовали. В группе рабепразола не было зарегистрировано ни одного эпизода ГИК, тогда как в группе контроля было отмечено два случая кровотечений из верхних отделов ЖКТ. Таким образом, в исследовании Hokimoto S. et al. рабепразол не оказывал выраженного влияния на эффективность ДАТ и не повышал риск кардиоваскулярных событий. Некоторое снижение антитромбоцитарной активности клопидогреля на фоне приема рабепразола, определенное in vitro, не влияло на клинические исходы, независимо от генотипа CYP2C19 [24]. В более раннем исследовании, проведенном той же группой авторов (n=127, 64% мужчин, средний возраст 68 лет), больные с ишемической болезнью сердца и стентом в коронарной артерии были разделены на подгруппы в соответствии с генотипом CYP2C19: 1 подгруппа – гомозиготы с нормальным метаболизмом (n=46, быстрый метаболизатор, генотип CYP2C19*1/*1), 2 подгруппа – гетерозиготы с промежуточным метаболизмом (n=52, промежуточный метаболизатор, генотип CYP2C19*1/*2 или 1/*3), 3 подгруппа – гомо- или гетерозиготы со сниженным метаболизмом (n=29, медленный метаболизатор, генотип CYP2C19*2/*2, *2/*3 или *3/*3) [25]. Все участники исследования принимали клопидогрель и были распределены в группы рабепразола (n=29) или контроля (n=98). Под действием клопидогреля степень АДФ-индуцированной агрегации тромбоцитов значительно снизилась в 1 подгруппе, в меньшей степени – во 2 подгруппе и минимально – в крови больных из 3 подгруппы (3250±1800 vs 4250±1300 vs 5010±1370 соответственно). В то же время степень АДФ-индуцированной агрегации достоверно не различалась между пациентами, принимавшими (4637±1800) и не принимавшими рабепразол (3980±1159) (рис.). Более того, не были зарегистрированы различия в уровне АДФ-индуцированной агрегации тромбоцитов между группами, принимавшими и не принимавшими рабепразол, при анализе с учетом генотипа CYP2C19. Что касается клинических событий, прием рабепразола и в этом исследовании не ассоциировался с повышенным риском кардиоваскулярных исходов (смерти и тромбоза стента). Таким образом, было показано, что прием рабепразола не снижает эффективность терапии клопидогрелем и не связан с повышенным риском смерти и тромбоза стента у пациентов с ишемической болезнью сердца после ЧКВ [25]. 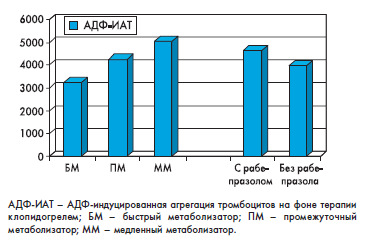 Рисунок. Степень АДФ-индуцированной агрегации
тромбоцитов Интересные результаты были получены в маленьком немецком исследовании, проведенном Kenngott S. et al. [26], в котором рабепразол (10 мг) не вызывал снижения антитромбоцитарной активности клопидогреля (определяемой in vitro по степени агрегации тромбоцитов) у пациента-гетерозиготы по CYP2C19 (с наличием в генотипе аллеля CYP2C19*2), у которого прием 20 мг омепразола приводил к значительному снижению эффективности данного тиенопиридина. Отсутствие взаимодействия между рабепразолом и клопидогрелем у пациента с доказанным взаимодействием между клопидогрелем и омепразолом поддерживает гипотезу, согласно которой конкуренция между ИПП и клопидогрелем не является классовым эффектом ИПП [26]. Было проведено несколько довольно крупных ретроспективных исследований, результаты которых подтверждают неспособность рабепразола ухудшать клинические исходы у больных, получающих ДАТ после ОКС. Одной из таких программ стало ретроспективное когортное исследование Hsiao F. et al. [27] с участием 9753 пациентов, в котором по сравнению с отсутствием в схеме лечения ИПП прием рабепразола не ассоциировался с повышением риска повторной госпитализации по поводу ОКС (ОР для рабепразола 0,60, 95% ДИ 0,17-2,17). Следует сказать, что в данном исследовании риск кардиоваскулярных исходов был низким для всех известных ИПП (ОР для омепразола 0,96, 95%ДИ 0,35-2,66; ОР для пантопразола 1,05, 95% ДИ 0,38-2,92; ОР для эзомепразола 0,31, 95% ДИ 0,10-0,99; ОР для ланзопразола 0,82, 95% ДИ 0,32-2,07) [27] (табл.). В другом похожем исследовании (Lin C. et al. [28], n=37099, пациенты после ОКС принимали только клопидогрель, первичная конечная точка – повторная госпитализация по поводу ОКС, вторичные конечные точки – госпитализация для проведения балонной ангиопластики и/или стентирования и/или коронарного шунтирования) риск повторной госпитализации в связи с ОКС повышал только омепразол (ОР 1,226; 95% ДИ 1,066-1,410, p=0,004); рабепразол и другие ИПП снова продемонстрировали отсутствие влияния на риск нежелательных исходов [28].
Таким образом, результаты доступных на сегодняшний день исследований рабепразола указывают, что: – наряду с другими ИПП рабепразол значительно снижает риск ГИК, опосредованных антиромбоцитарной терапией (Ng F. [9], Ray W. et al. [16], Lanas A. [17]); – рабепразол минимально воздействует на метаболизм и антиагрегантный эффект клопидогреля (Blume H. [22], Hokimoto S. et al [24, 25], Kenngott S. et al. [26]); – влияние рабепразола на активность клопидогреля не зависит от полиморфизма гена, кодирующего СYP2C19 (Hokimoto S. et al. [24, 25]); – рабепразол не оказывает влияния на клинические эффекты клопидогреля, не вызывает повышения риска основных кардиоваскулярных событий (Hokimoto S. et al. [24, 25], Hsiao F. et al. [27], Lin C. et al. [28]). Заключение Поставить точку в решении вопроса о безопасности одновременного применения ИПП и клопидогреля позволят только рандомизированные клинические исследования. На сегодняшний день потенциальные защитные эффекты ИПП должны учитываться при выборе стратегии лечения пациентов с высоким риском ГИК, требующих проведения антитромбоцитарной терапии. По мнению ряда авторов, в подобной ситуации следует отдавать предпочтение препаратам, минимально влияющим на активность CYP2C19, метаболизм и эффективность клопидогреля. Литература: 1. Bhatt D., Scheiman J., Abraham N., et al. ACCF/ACG/AHA 2008 expert consensus document on reducing the gastrointestinal risks of antiplatelet therapy and NSAID use: a report of the American College of Сardiology Foundation Task Force on Clinical Expert Consensus Documents. J Am Coll Cardiol. 2008;52:1502-17. 2. Public Health Advisory: Updated safety information about a drug interaction between Clopidogrel Bisulfate (marketed as Plavix) and Omeprazole (marketed шs Prilosec and Prilosec OTC). Available at: http://www.fda.gov/Drugs/DrugSafety/PublicHealthAdvisories/ucm19 0825.htm. Accessed May 28, 2010 3. Taha A., McCloskey C., Prasad R. et al. Famotidine for the prevention of peptic ulcers and oesophagitis in patients taking low-dose aspirin (FAMOUS): a phase III, randomised, double-blind, placebocontrolled trial.Lancet. 2009; 374: 119 -25. 4. Van H., Depre M., Wynants K. et al. Effect of clopidogrel on naproxeninduced gastrointestinal blood loss in healthy volunteers. Drug Metabol Drug Interact. 1998;14:193-205. 5. Fork F., Lafolie P., Toth E. et al. Gastroduodenal tolerance of 75 mg clopidogrel versus 325 mg aspirin in healthy volunteers. A gastroscopic study. Scand J Gastroenterol. 2000; 35: 464 -9. 6. Abraham N., Graham D. NSAIDs and gastrointestinal complications: new clinical challenges. Expert Opin Pharmacother. 2005; 6: 2681-9. 7. Hernandez-Diaz S., Rodriguez L. Association between nonsteroidal anti-inflammatory drugs and upper gastrointestinal tract bleeding/perforation: an overview of epidemiologic studies published in the 1990s. Arch Intern Med. 2000; 160: 2093-9. 8. Ng F., Chan P., Kwanching C. et al. Management and outcome of peptic ulcers or erosions in patients receiving a combination of aspirin plus clopidogrel. J Gastroenterol. 2008; 43: 679-86. 9. Ng F., Lam K., Wong S. et al. Upper gastrointestinal bleeding in patients with aspirin and clopidogrel co-therapy. Digestion. 2008; 77: 173-7. 10. Moukarbel G., Signorovitch J., Pfeffer M. et al. Gastrointestinal bleeding in high risk survivors of myocardial infarction: the VALIANT Trial. Eur Heart J. 2009; 30: 2226-2232. 11. Garcia Rodriguez L., Lin K., Hernandez-Diaz S., Johansson S. Risk of upper gastrointestinal bleeding with low-dose acetylsalicylic acid alone and in combination with clopidogrel and other medications. Circulation. 2011;123: 1108-1115. 12. Abraham N., Hlatky M. et al. ACCF/ACG/AHA 2010 Expert Consensus Document on the Concomitant Use of Proton Pump Inhibitors and Thienopyridines: A Focused Update of the ACCF/ ACG/AHA 2008 Expert Consensus Document on Reducing the Gastrointestinal Risks of Antiplatelet Therapy and NSAID Use A Report of the American College of Cardiology Foundation Task Force on Expert Consensus Documents. Circulation. 2010; 122: 2619-2633. 13. Yusuf S., Zhao F., Mehta S. et al. Effects of clopidogrel in addition to aspirin in patients with acute coronary syndromes without ST-segment elevation. N Engl J Med. 2001; 345: 494 -502. 14. Connolly S., Pogue J., Hart R. et al. Effect of clopidogrel added to aspirin in patients with atrial fibrillation. N Engl J Med. 2009; 360: 2066-78. 15. Ma L., Elliott S., Cirino G. et al. Platelets modulate gastric ulcer healing: role of endostatin and vascular endothelial growth factor release. ProcNatl Acad Sci U S A. 2001; 98: 6470 -5. 16. Ray W., Murray K., Griffin M. et al. Outcomes with concurrent use ofclopidogrel and proton-pump inhibitors: a cohort study. Ann Intern Med. 2010; 152: 337- 45. 17. Lanas A., Garcia-Rodriguez L., Arroyo M. et al. Effect of antisecretory drugs and nitrates on the risk of ulcer bleeding associated with nonsteroidal anti-inflammatory drugs, antiplatelet agents, and anticoagulants. Am J Gastroenterol. 2007; 102: 507-15. 18. http://www.fda.gov/Drugs/DrugSafety/PostmarketDrugSafety InformationforPatientsandProviders/DrugSafetyInformationforHeathc areProfessionals/ucm190784.htm 19. Holmes D., Dehmer G., Kaul S. et al. ACCF/AHA Clopidogrel Clinical Alert: Approaches to the FDA «Boxed Warning»: A Report of the American College of Cardiology Foundation Task Force on Clinical Expert Consensus Documents and the American Heart Association. J Am Coll Cardiol 2010; 56: 321-41. 20. Gladding P., Webster M., Zeng I. et al. The pharmacogenetics and pharmacodynamics of clopidogrel response: an analysis from the PRINC (Plavix Response in Coronary Intervention) trial. J Am Coll Cardiol Intv.2008; 1: 620-7. 21. Mehta S., Bassand ., Chrolavicius S. et al. Dose comparisons of clopidogrel and aspirin in acute coronary syndromes. N Engl J Med. 2010; 363: 930-42. 22. Blume H., Donath F., Warnke A., Schug B. Pharmacokinetic Drug Interaction Profiles of Proton Pump Inhibitors. Drug Safety, Volume 29 2006; 9(16): 769-784. 23. Конорев М.Р., Тябут Г.Д. Ингибиторы протонной помпы: свойства и применение. Медицинские новости. 2011 (9); 58-62. 24. Hokimoto S., Ogawa H. Is it Safe to use a Proton Pump Inhibitor With Clopidogrel? A Comparison of Clopidogrel With or Without Rabeprazole in Japan. 2010. AGA Abstracts T1145. http://download. journals.elsevierhealth.com/pdfs/journals/0016-5085/ PIIS0016508510623001.pdf) 25. Hokimoto S., Ogawa H., Yamamoto K. et al. Is Impact of Proton Pump Inhibitor on Platelet Reactivity to Clopidogrel A Class Effect? Abstract 5010. Circulation. 2009; 120: S1033. 26. Kenngott S., Olze R., Kollmer M. et al. Clopidogrel and proton pump inhibitor (PPI) interaction: separate intake and a non-omeprazole PPI the solution? Eur J Med Res. 2010 May 18; 15(5): 220-4. Abstract. 27. Hsiao F., Mullins C., Wen Y. et al. Relationship between cardiovascular outcomes and proton pump inhibitor use in patients receiving dual antiplatelet therapy after acute coronary syndrome. Pharmacoepidemiol Drug Saf. 2011 Oct; 20 (10): 1043-9. Abstract. 28. Lin C., Shen L., Wu F. et al. Cardiovascular Outcomes Associated with Concomitant Use of Clopidogrel and Proton Pump Inhibitors in Patients of Acute Coronary Syndrome in Taiwan. Br J Clin Pharmacol. 2012 Feb 24. doi: 10.1111/j.1365-2125.2012.04250. Автор обзора Галина Милюхина Medicine Review 2012; 2 (20): 42-45 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2024. Усі права захищені.
|
мапа сайту корисні посилання |