Тромбоэмболия легочной артерии на фоне нефротического синдромаТромбоэмболия легочной артерии (ТЭЛА) – грозное сердечно-сосудистое заболевание, которое является одной из основных причин в структуре кардиоваскулярной смертности. Эта патология занимает особое место в кардиологии и медицине в целом по ряду причин. Во-первых, ТЭЛА может быть осложнением самых различных заболеваний и патологических состояний, в том числе некардиологического характера. Во-вторых, патофизиологические механизмы и клинические проявления ТЭЛА многообразны и находятся в поле интересов разных специалистов – кардиологов, сердечно-сосудистых хирургов, пульмонологов, торакальных хирургов, гематологов, хирургов общего профиля, травматологов и др. В-третьих, в зависимости от обширности поражения и степени тяжести течение ТЭЛА может значительно варьировать – от молниеносного развития острого легочного сердца с фатальным исходом до вялотекущего недомогания с постепенным (порой на протяжении десятков лет) развитием хронической легочной гипертензии. Наконец, точная распространенность ТЭЛА и смертность от нее остаются неизвестными даже в развитых странах мира с хорошо налаженной системой медицинской статистики; диагноз тромбоэмболии чаще устанавливается постфактум, по результатам аутопсии, вне зависимости от причины смерти. В среднем распространенность ТЭЛА, по данным 25-летнего популяционного исследования ученых из Миннесоты (США), в настоящее время составляет примерно 1 на 1 тыс. населения [1], однако это достаточно приблизительная цифра, которая к тому же не учитывает национальные особенности в ряде регионов мира (например, в азиатских странах риск ТЭЛА ниже). Отсюда очевидно, насколько сложной проблемой является диагностика, лечение и профилактика ТЭЛА. К счастью, именно в области профилактики ТЭЛА имеется немало действенных подходов и стратегий. Хотя факторов риска развития ТЭЛА довольно много, большинство из них модифицируемы, то есть относительно легко выявляются и корригируются. Зная, какие заболевания и состояния наиболее опасны в отношении развития тромбозов и эмболий, врач может максимально снизить вероятность ТЭЛА у своих пациентов, а также своевременно заподозрить эту патологию даже, казалось бы, в не очень типичных случаях. Один из таких «нетипичных» клинических случаев хотелось бы представить в этом обзоре. Речь идет о развитии ТЭЛА у юной девушки (17 лет), и «нетипичность» состоит именно в возрасте пациентки. Легочная тромбоэмболия в молодом возрасте встречается редко, ее частота увеличивается с возрастом (если у детей до 15 лет ее распространенность оценивается примерно как 0,2 случая на 100 тыс. ежегодно, то в возрасте 85 лет и старше – 700 случаев на 100 тыс. ежегодно [1]). Однако следует помнить, что при наличии ряда заболеваний, патологических состояний и факторов риска вероятность ТЭЛА возрастает независимо от возраста. Как будет очевидно из приведенного ниже описания клинического случая, для развития ТЭЛА у пациентки были все предрасполагающие факторы, о которых следует помнить врачу любой специальности. Кроме того, обращаем внимание, что рассматриваемый клинический случай потребовал привлечения усилий самых разных специалистов – педиатров, кардиологов, нефрологов, пульмонологов, патоморфологов и пр. В одном из последних номеров New England Journal of Medicine T.B. Kinane, E.F. Grabowski, A. Sharma, K. Nimkin, M.E. King и L.D. Cornell (отделения педиатрии, радиологии, патологии Массачусетского госпиталя и Гарвардской медицинской школы) представили следующий клинический случай [2]. История болезни В педиатрическое отделение Массачусетского госпиталя поступила 17-летняя девушка с жалобами на боль в груди и кровохарканье. В анамнезе у пациентки бронхиальная астма легкой степени, в остальном девушка до недавних пор была здорова. На протяжении 3 последних лет она принимала оральные контрацептивы в связи с дисменореей. За 4 мес до описываемых событий у пациентки появились отеки нижних конечностей (стоп). При обследовании были выявлены протеинурия (3+), гематурия и гиперлипидемия. Через месяц была проведена биопсия почек, на основании результатов которой диагностирован мембранозный гломерулонефрит. Антител к вирусам гепатита В и С, РНК, топоизомеразе I, антигену Смита (antiSmith, или антитела к Sm-антигену), антигенам Ro/SS-A и La/SS-B, нативной ДНК, а также антинуклеарных антител обнаружено не было. Уровни С3 и С4-компонентов комплемента в сыворотке крови соответствовали норме. В связи с гломерулонефритом пациентке были назначены эналаприл и аторвастатин, а также рекомендовано уменьшение потребления жидкости. Однако через несколько недель после начала лечения аторвастатин был отменен в связи с появившимися мышечными болями. Кроме того, после биопсии почки пациентку беспокоила постоянная выраженная боль в спине и в области живота, причиной которой оказалась небольшая околопочечная гематома, как показало ультрасонографическое обследование. Несмотря на прием обезболивающих препаратов и на то, что гематома, по данным визуализирующих методов обследования, постепенно уменьшалась, в дальнейшем сильные боли в области спины и живота продолжали беспокоить, нарушая сон и ограничивая двигательную активность пациентки. В связи с этим больная была вынуждена соблюдать постельный режим. Наряду с этим периодически вновь появлялись отеки нижних конечностей. За две недели до поступления пациентки в клинику по поводу боли в груди и кровохарканья болезненные ощущения в области спины и живота несколько уменьшились, однако появилась боль в грудной клетке, иррадиирующая в шею и плечи и усиливающаяся при кашле и глубоком вдохе. За неделю до поступления в стационар больная обследовалась в другой клинике, где ей был установлен диагноз межреберной невралгии и назначены габапентин и трамадол. Тем не менее на протяжении последующей недели боль в груди усиливалась, появились кашель и кровохарканье, а также имел место эпизод одышки, которая прекратилась после использования альбутерола в виде ингаляции. За сутки до настоящей госпитализации пациентка обратилась в еще одну клинику в связи с нарастающей болью в груди, температурой тела 39,0 °С, тахикардией (156/мин) и тахипноэ (50/мин). Артериальное давление составляло 115/69 мм рт. ст., сатурация кислорода в крови – 98%. При осмотре дыхание поверхностное в связи с болью в грудной клетке, однако легкие чистые и физическое состояние в целом удовлетворительное. В приемном отделении больной была выполнена инфузия физраствора (2 л), далее пациентка поступила в педиатрическое отделение интенсивной терапии, где ей были назначены также эноксапарин и морфин. В связи с тем, что сатурация кислорода в крови периодически снижалась до 92-93%, проводилась оксигенотерапия. При обследовании обнаружены протеинурия (3+), гематурия (2+), удельный вес мочи 1,041. На рентгенограмме грудной клетки – участки затемнения в левом реберно-диафрагмальном углу. На следующий день после госпитализации была проведена трансторакальная эхокардиография (ЭхоКГ), которая выявила умеренную дилатацию правого желудочка, небольшой выпот в перикарде, а также сглаженные, парадоксальные движения перегородки; давление в легочной артерии составляло 60 мм рт. ст. Однако в полостях сердца тромбов обнаружено не было. С учетом полученных результатов были выполнены такие методы обследования, как спиральная компьютерная томография и ангиография легочной артерии, которые позволили визуализировать эмболы в обеих легочных артериях и множественные инфаркты обоих легких, а также небольшой, но двусторонний плевральный выпот. В ходе ультрасонографического исследования почек обнаружена гематома вокруг левой почки, хотя не были выявлены тромбы ни в нижней полой вене, ни в глубоких венах нижних конечностей. В связи с новыми данными обследования эноксапарин был заменен на нефракционированный гепарин, а пациентка направлена в отделение интенсивной терапии Массачусетского госпиталя. В момент поступления лечение больной включало применение гепарина, морфина, ранитидина, ингаляций альбутерола (по требованию), инфузий физраствора с декстрозой. Данные осмотра при поступлении: температура 38,3 °С, тахикардия 148/мин, артериальное давление 138/72 мм рт. ст., частота дыхания 34/мин, сатурация кислорода в крови 92%, пульсация яремной вены, дыхание ослабленное на вдохе, усиление II сердечного тона, грубый систолический шум внизу у края грудины, выбухание правого желудочка, пульсация легочной артерии во втором межреберном промежутке. Кроме того, правая боковая область живота была чувствительна, а отеки нижних конечностей распространились на голени. По данным электрокардиографии (ЭКГ): увеличена амплитуда зубца S в отведении I, в отведении III появился зубец Q и стал отрицательным зубец Т.По результатам лабораторных тестов: несколько снижен показатель гематокрита, гипопротеинемия с выраженной гипоальбуминемией, небольшой нейтрофильный лейкоцитоз, увеличено содержание тромбоцитов, немного увеличено активированное парциальное тромбопластиновое время, повышен уровень протромбина, значительно увеличено количество С-реактивного протеина, определялось наличие тропонина в крови, резко увеличено содержание мозгового натрийуретического пептида в крови (BNP), а также D-димера. Таким образом, данные первичного обследования указывали на нефротический синдром, перегрузку правых отделов сердца, нарушения гемокоагуляции. Кроме того, имел место такой признак, как повышение содержания D-димера, который хотя и не является специфичным для ТЭЛА, но все же высокочувствителен в отношении этой патологии. Нормальный уровень D-димера (менее 500 мкг/л) в плазме позволяет с точностью более 90% отвергнуть предположение о наличии ТЭЛА; у данной пациентки уровень этого показателя составлял 5656 мкг/л. Компьютерная томография грудной клетки подтвердила наличие крупных тромбов в просвете правой и левой легочных артерий (рис. 1А и 1В), а также сегментарных легочных артерий с обеих сторон (рис. 1С). При трехмерном воссоздании структуры легких во фронтальной плоскости в обоих легких определялись множественные периферические участки затемнения (инфаркты ткани легкого), а также небольшой двусторонний плевральный выпот (рис. 1D).
При решении вопроса о дальнейшей тактике ведения пациентки необходимо было прежде всего определиться с тем, целесообразно ли назначение тромболитической терапии и установление кава-фильтра. Разработка оптимальной стратегии лечения осложнялась наличием патологии почек и обусловленного ею нефротического синдрома. Кроме того, высокое давление в легочной артерии и дисфункция правого желудочка серьезно ухудшали прогноз. Так, по данным разных авторов (A. Ribeiro et al., 1997; S. Grifoni et al., 2000; A. Vieillard-Baron et al., 2001), смертность в таких случаях не превышает 1%, если работа правого желудочка не нарушена, однако при дисфункции правого желудочка может достигать 24%. Однако у пациентки отсутствовал еще один неблагоприятный прогностический фактор – системная гипотензия, поэтому риск ее смерти был оценен несколько ниже – приблизительно в 8% (при гипотензии он составил бы не менее 15%). Показана ли для данной больной тромболитическая терапия? Результаты большинства клинических исследований указывают на определенные преимущества тромболизиса в таких случаях, которые, однако, сопряжены с некоторым риском геморрагических осложнений (от 1 до 3%, по данным крупного регистра ICOPER, 1999). При этом даже успешная тромболитическая терапия практически не уменьшает риск смерти, однако она может улучшить функцию правого желудочка (S. Konstantinides et al., 1998; B. Dong et al., 2006). В связи с этим врачи первоначально предположили, что преимущества от проведения тромболитической терапии у данной пациентки сомнительны. Однако, несмотря на то что тромбов в нижней полой вене при ультрасонографическом обследовании не обнаружено (а дополнительное введение контрастных веществ для проведения ангиографии могло резко ухудшить функцию почек), риск поступления новых тромбов в малый круг кровообращения был расценен как очень высокий. При имеющейся выраженной правожелудочковой недостаточности каждая дополнительная ТЭЛА могла стать фатальной. Поэтому польза от тромболизиса, по мнению лечащих врачей, все же перевешивала возможный риск кровотечений. Исключение составляют случаи, когда в наличии имеются четкие доказательства отсутствия тромба в нижней полой вене. В данной клинической ситуации нельзя быть уверенным, что в нижней полой вене нет тромбов, поэтому было принято решение о проведении тромболизиса. Через 5 ч после госпитализации был отменен гепарин и начата тромболитическая терапия (100 мг тканевого активатора плазминогена на протяжении 2 ч). К счастью, геморрагических осложнений у пациентки не наблюдалось. После этого опять был назначен нефракционированный гепарин (1100 ЕД/ч внутривенно). Через 6,5 ч после тромболизиса на ЭхоКГ сохранялись признаки повышенного давления в легочной артерии, а также перегрузки и острого растяжения правого желудочка (рис. 2А). Кроме того, отмечался специфический признак, характерный для острой ТЭЛА, описанный M.V. McConnell и соавт. (1996): сохранение нормальной подвижности верхушечного сегмента правого желудочка во время сокращений при наличии гипокинезии других его сегментов (рис. 2В).
На 2-й день пребывания в клинике пациентке выполнена компьютерная томография органов грудной клетки и брюшной полости с контрастированием сосудов, по результатам которой не было обнаружено тромбов в глубоких венах нижних конечностей и таза. Однако экскреторная урография позволила выявить тромбы в просветах почечных вен с обеих сторон. На 4-е сутки пребывания в клинике была проведена магниторезонансная венография с контрастированием, данные которой позволили создать трехмерную реконструкцию состояния сосудов таза и живота во фронтальной плоскости. На этом изображении видно, что тромб из правой почечной вены частично перекрыл просвет нижней полой вены (рис. 3). Левая почечная вена плохо визуализируется – по всей видимости, из-за находящегося в ней тромба. В других венах брюшной полости и таза тромбов не обнаружено.
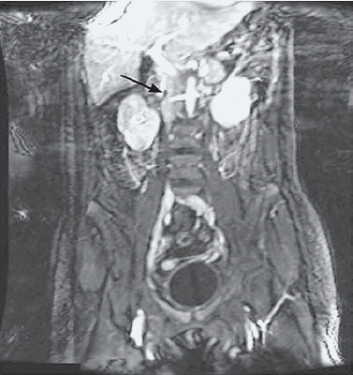 Рисунок 3. Результаты магниторезонансной венографии
Таким образом, источник эмболов был установлен. На протяжении первых суток после тромболизиса у пациентки сохранялась тахикардия (120-150/мин), систолическое артериальное давление было 130-150 мм рт. ст., больной требовалось проведение оксигенотерапии, чтобы поддерживать сатурацию кислорода в крови между 97 и 100%. На 5-е сутки после тромболизиса тахикардия исчезла, а сатурация кислорода в крови составляла 99% при вдыхании обычного атмосферного воздуха. В дополнение к гепарину больной был назначен варфарин. Вскоре прием гепарина отменили, и на 9-й день с момента госпитализации пациентка была выписана домой. На момент выписки она получала следующую терапию: варфарин 6 мг ежедневно, преднизолон 30 мг дважды в день, эналаприл 10 мг дважды в день, фуросемид 20 мг ежедневно, сульфат железа 325 мг ежедневно, ранитидин 150 мг ежедневно. Клинический диагноз при выписке: «Легочная тромбоэмболия на фоне нефротического синдрома». Обсуждение Как правило (в 70-90% случаев), ТЭЛА развивается в связи с миграцией эмболов из глубоких вен нижних конечностей и таза (рис. 4). С учетом общности патофизиологических механизмов развития, тромбоз глубоких вен нижних конечностей и тромбоз вен таза объединяются под названием «венозный тромбоэмболизм». Такая терминология оправдана из тех соображений, что при развитии ТЭЛА в первую очередь следует искать тромбы в венах нижних конечностей и таза – в абсолютном большинстве случаев это позволяет быстро и точно идентифицировать локализацию тромбоза, источника эмболов, и разработать оптимальную тактику лечения. Актуальность венозного тромбоэмболизма очень высока – так, в США количество лиц с этой патологией достигает 100 на 100 тыс. ежегодно, причем у трети (!) больных с манифестным венозным тромбоэмболизмом развиваются легочные тромбоэмболии той или иной степени тяжести [3].
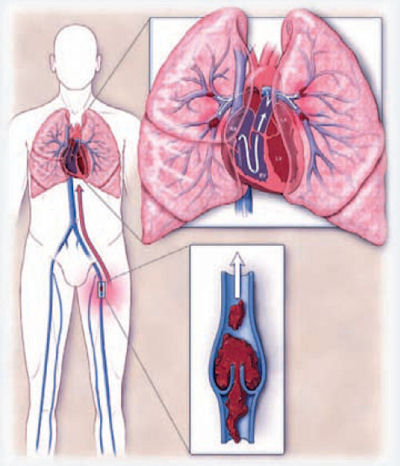 Рисунок 4. Типичная схема развития ТЭЛА: тромбоз в
Вместе с тем, помимо венозного тромбоэмболизма, существует немало различных заболеваний и состояний, которые могут стать непосредственной причиной или весомым предрасполагающим фактором к развитию ТЭЛА. Наиболее известны среди таких предрасполагающих патологий тяжелые травмы, особенно множественные переломы конечностей; хирургические вмешательства, в частности на органах малого таза; злокачественные новообразования; врожденные или приобретенные коагулопатии; хроническая сердечная недостаточность с застойными явлениями. Менее известны – такие факторы, как нефротический синдром, однако именно он стал первопричиной формирования тромбозов и эмболий у представленной пациентки, невзирая на ее юный возраст. Нефротический синдром сопровождает многие заболевания почек. Наиболее часто он развивается у маленьких детей, а у взрослых встречается преимущественно в молодом возрасте. Первичный нефротический синдром является следствием первичных заболеваний почек – в первую очередь гломерулонефрита. Вторичный нефротический синдром может возникать в результате разнообразных заболеваний или состояний, при которых почки вовлекаются в патологический процесс вторично (амилоидоз почек, сахарный диабет, нефропатия беременных, туберкулез, сифилис, малярия, системные заболевания соединительной ткани, ревматоидный артрит, геморрагический васкулит, миеломная болезнь, лимфогранулематоз, отравления тяжелыми металлами, медикаментозные поражения почек и др.). Нефротическому синдрому свойственна гиперкоагуляция крови, которая может варьировать от небольшого повышения свертывающей способности до развития диссеминированной внутрисосудистой коагуляции. Параллельно с нарушением белкового и липидного обмена при нефротическом синдроме очень часто развиваются изменения в свертывающей и противосвертывающей системах крови, результатом которых является снижение активности антикоагулянтных и фибринолитических факторов, а также активация кининкалликреиновой системы. Гиперкоагуляция усугубляет морфологические изменения в почках: способствует отложениям фибрина как в клубочковых капиллярах, так и в полости капсулы Шумлянского – Боумена, обусловливает локальную внутрисосудистую коагуляцию, приводит к нарушению микроциркуляции в клубочковых капиллярах и предрасполагает к более быстрому развитию гиалиноза и склероза клубочков с нарушением функции почек, вплоть до анурии. Кроме того, гиперкоагуляция имеет значение для системного кровотока, способствуя развитию тромбов, особенно в почечных венах. Этот локальный тромбоз может стать причиной ТЭЛА и сердечной недостаточности. Тромбоэмболии на фоне нефротического синдрома развиваются довольно часто – в 44% случаев у взрослых (тогда как у детей намного реже – примерно в 5% случаев) [4]. Следует помнить, что риск тромбоза и тромбоэмболии при нефротическом синдроме коррелирует с уровнем липидов в крови: чем выше содержание липопротеидов и холестерина, тем выше риск тромботических осложнений. Риск таких осложнений усугубляют и другие клинические проявления нефротического синдрома, особенно те, что ассоциированы с потерей белка: так, чем более выражены отеки, тем более значительна гипоальбуминемия, что также способствует гиперкоагуляции. Таким образом, развитие тромбоза почечных вен и ТЭЛА в представленной клинической ситуации объяснимо прежде всего наличием нефротического синдрома. Однако у этой пациентки было несколько факторов риска, способствовавших развитию тромбоза и тромбоэмболии: не только нефротический синдром с выраженной гиперлипопротеинемией и значительными отеками, но и длительная иммобилизация в связи с болью в спине и животе, а также прием оральных контрацептивов на протяжении 3 лет. Наличие нескольких факторов риска привело к кумулятивному возрастанию угрозы тромбоэмболических событий. Лечение и профилактика Обсуждая оптимальные подходы к ведению пациентки, специалисты отмечают, что лечение в данной клинической ситуации имеет ряд особенностей. Тромболизис в подобных случаях не имеет жизнеспасающего значения: хотя тромбоэмболия достаточно массивная (тромбы в главных и сегментарных легочных артериях), поражение сосудистого русла малого круга кровообращения не привело к существенным нарушениям системного кровообращения, даже не обусловило развития артериальной гипотензии, хотя правожелудочковая недостаточность имела место. В клинической картине доминировал синдром множественных инфарктов ткани легкого, а не синдром острого легочного сердца. Тромболизис показан при массивной тромбоэмболии и хотя, по мнению многих специалистов, может использоваться и при закупорке мелких артерий, если имеется нарушение функции правого желудочка, однако существует немало возражений против подобной тактики в случае отсутствия массивного поражения крупных легочных сосудов и нарушений системного кровообращения, поскольку у рассматриваемой категории больных риск геморрагических осложнений может свести на нет потенциальную пользу тромболитической терапии. Кроме того, легочные эмболы у данной пациентки существовали, по приблизительным оценкам, уже на протяжении 6 нед до поступления в стационар, поэтому острой необходимости в активном тромболизисе не было. Обычно тромболитическая терапия при ТЭЛА применяется у больных с массивной и субмассивной тромбоэмболией в пределах 2 нед с момента развития заболевания, хотя наибольший эффект от лечения наблюдается при проведении тромболизиса в течение ближайших 3-7 сут. Как видно из представленного клинического случая, у данной пациентки тромболитическая терапия закономерно не привела к заметному улучшению состояния, хотя, к счастью, и не вызвала геморрагических осложнений. Скорее всего, положительную роль в нормализации состояния и профилактике повторных эмболий сыграла антикоагулянтная терапия. Есть основания полагать, отмечают авторы публикации [2], что у подобного рода пациентов (с множественными тромбами и легочной гипертензией) может быть эффективной тактика длительной терапии низкими дозами тромболитиков. Разумеется, в этом отношении должны быть проведены соответствующие исследования и получены убедительные доказательства эффективности и безопасности такой терапии. Инфузия гепаринов (низкомолекулярных или нефракционированного) с последующим переводом на варфарин считается золотым стандартом лечения в острый период ТЭЛА. Однако от обычной антикоагулянтной терапии в данной клинической ситуации не стоит ожидать должной эффективности, поскольку на фоне выраженной гипоальбуминемии гепарин практически бессмысленно использовать, так как он на 80-90% связывается с альбумином крови. Поэтому в этой ситуации предпочтительны прямые ингибиторы тромбина, такие как бивалирудин, лепирудин, аргатробан. В частности, доктор Eric F. Grabowski (Cardiovascular Thrombosis Laboratory, Pediatric Hematology and Oncology, Массачусетский госпиталь) [2] советует использовать аргатробан, который связывается с альбумином плазмы крови всего на 55% и метаболизируется преимущественно в печени (лепирудин, напротив, выводится из организма главным образом почками и потому не рекомендуется при гломерулонефрите, как и бивалирудин, который вообще практически не связывается с белками плазмы крови). Такая же тактика (применение прямых ингибиторов тромбина) показана при развитии гепарининдуцированной тромбоцитопении. Варфарин на сегодняшний день остается препаратом выбора для профилактики рецидивов тромбозов и эмболий у больных, перенесших ТЭЛА. Поэтому после выписки из клиники пациентке необходим прием варфарина около 1 года с удержанием международного нормализованного отношения (МНО) в пределах 2-3 и после этого еще 6-12 мес с удержанием МНО в пределах 1,5-2. Прогноз для данной пациентки неоднозначен. Тем не менее риск повторного тромбоза у нее можно значительно снизить, исходя из того, что факторы, способствовавшие возникновению тромбоэмболии, выявлены и могут быть модифицированы (в отличие от случаев развития тромботических осложнений без видимых причин или в связи с немодифицируемыми факторами риска). Если бы в кровеносное русло попадали новые эмболы, несмотря на назначенную антикоагулянтную терапию, целесообразным было бы установить кава-фильтр в супраренальном сегменте нижней полой вены, хотя такая операция проводится достаточно редко в связи с возможными осложнениями в случае окклюзии кава-фильтра. Однако необходимость в этом не возникла. К тому же в исследовании H. Decousus et al. (1998) было показано, что хотя кава-фильтры уменьшают риск тромбоэмболий, они не влияют на общую выживаемость пациентов [8]. Оперативное удаление тромбов из легочных артерий и такие варианты терапии, как селективный тромболизис и механическое удаление тромба через катетер, авторы публикации [2] не обсуждали, поскольку консервативное лечение антикоагулянтами в итоге оказалось достаточно эффективным. Разумеется, для успешной профилактики дальнейших тромбозов и эмболий необходимо уточнение основного диагноза и назначение адекватной терапии гломерулонефрита, прежде всего с целью нормализации уровней липидов и белков в крови. Это достигается с помощью гиполипидемических препаратов (статинов), блокаторов ренин-ангиотензин-альдостероновой системы и др. К сожалению, у данной пациентки не было возможности использовать статины в связи с непереносимостью препаратов этой группы, а применение ингибитора ангиотензинпревращающего фермента эналаприла как нефропротекторного средства не было достаточно эффективным, чтобы предотвратить прогрессирование альбуминурии и развитие тромбоза почечных вен. Поэтому этой больной показано добавление в схему лечения блокатора рецепторов ангиотензина II, а при недостаточной эффективности (что не исключено ввиду довольно агрессивного течения заболевания) необходимо обратить внимание на усиление иммуносупрессивной терапии. Данной пациентке еще в больнице был назначен кортикостероид (преднизолон), хотя в большинстве случаев стандартная монотерапия кортикостероидом в подобных клинических ситуациях также оказывается неэффективной и в дальнейшем приходится комбинировать различные иммуносупрессоры друг с другом. Судьба пациентки Результаты биопсии почки не позволили сделать однозначных выводов о том, является ли мембранозный гломерулонефрит первичным или вторичным, а если он вторичный, то какова его природа. Существовали подозрения, что заболевание может быть вторичным в связи с системной красной волчанкой, которая еще не манифестировала. Разрешить эти сомнения могло только время, поэтому пациентка находилась под тщательным наблюдением на протяжении нескольких месяцев после выписки из клиники. Практически сразу после выписки пациентке был также дополнительно назначен блокатор рецепторов ангиотензина II (лозартан), а поскольку протеинурия и после этого сохранялась на достаточно высоком уровне (около 8 мг/сут), через 3 мес после выписки из клиники в схему лечения добавлен мощный иммуносупрессор – микофенолата мофетил. После этого протеинурия резко уменьшилась и оставалась на приемлемом уровне (ниже 1 г/сут) на протяжении полугода после выписки. На 8-м месяце после выписки у пациентки появились остроконечные кондиломы и был установлен диагноз папиломавирусной инфекции (инфицирование, по всей видимости, произошло несколькими годами ранее), в связи с чем дозу микофенолата мофетила пришлось снизить. Кондиломы при этом исчезли, и почечная функция оставалась удовлетворительной. Дозу микофенолата мофетила продолжали постепенно уменьшать, и через 15 мес после выписки препарат был отменен; преднизолон пациентка принимала на протяжении 20 мес после выписки. За это время состояние больной нормализовалось, протеинурия оставалась на уровне 0,2 мг/сут, уровни белка и липопротеинов в крови были приемлемыми, признаков системной красной волчанки не появилось. Терапия варфарином продолжалась 14 мес. Рецидивов тромбозов и эмболий не наблюдалось. В настоящее время девушка здорова, физически активна. Результаты обследования функции легких через 18 мес после выписки были нормальными. Литература: 1. Silverstein M.D., Heit J.A., Mohr D.N. et al. Trends in the incidence of deep vein thrombosis and pulmonary embolism: a 25-year populationbased study. Arch Intern Med 1998; 158: 585-593. 2. Kinane T.B., Grabowski E.F., Sharma A. et al. A 17-Year-Old Girl with Chest Pain and Hemoptysis. New England Journal of Medicine 2008; 358: 941-952. 3. Rosamond W. et al. Heart Disease and Stroke Statistics – 2008 Update. A Report From the American Heart Association Statistics Committee and Stroke Statistics Subcommittee. Circulation 2008; 117: e25-e146. 4. Mehls O., Andrassy K., Koderisch J. et al. Hemostasis and thromboembolism in children with nephrotic syndrome: differences from adults. J Pediatr 1987; 110: 862-867. 5. Kucher N., Goldhaber S.Z. Management of massive pulmonary embolism. Circulation 2005; 112: e28-e32. 6. Dong B., Jirong Y., Liu G. et al. Thrombolytic therapy for pulmonary embolism. Cochrane Database Syst Rev 2006; 2: CD004437-CD004437. 7. Lee B.H., Cho H.Y., Kang H.G. et al. Idiopathic membranous nephropathy in children. Pediatr Nephrol 2006; 21: 1707-1715. 8. Tapson V.F. Acute Pulmonary Embolism. New England Journal of Medicine 2008; 358: 1037-1052. 9. Geerts W.H., Pineo G.F., Heit J.A. et al. Prevention of venous thromboembolism: the Seventh ACCP Conference on Antithrombotic and Thrombolytic Therapy. Chest 2004; 126: Suppl: 338S-400S. 10. Nicolaides A.N., Fareed J., Kakkar A.K. et al. Prevention and treatment of venous thromboembolism: International consensus statement. Int Angiol 2006; 25: 101-161. Автор обзора: Елена Михайлова Medicine Review 2008; 2 (02): 50-55 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2026. Усі права захищені.
|
мапа сайту корисні посилання |